
- •Ход урока
- •I. Организационно-психологический этап
- •II. Ориентировочно-мотивационный этап
- •III. Операционно-познавательный этап
- •1. История мыла:
- •2. Строение мыла, «смс», свойства (вопросы освещают химики – теоретики)
- •3. Получение мыла (технологи).
- •4. Механизм моющего действия мыла и синтетических моющих средств.
- •Перспективы применения мыла.
- •IV. Контрольно-коррекционный этап
- •4. Рефлексия.
- •I. Организационно-психологический этап
- •II. Ориентировочно-мотивационный этап
- •III. Операционно-познавательный этап
- •IV. Контрольно-коррекционный этап
- •§ 41, № 3,5. Сделать презентацию по теме «Синтетические волокна».
2. Строение мыла, «смс», свойства (вопросы освещают химики – теоретики)
Представлено несколько упаковок различных сортов мыла. Прочитайте состав мыла и назовите его основную часть.
Лауретсульфат натрия, таловат натрия, кокоат натрия, натриевые (калиевые) соли жирных кислот, стеарат натрия, гликоль дистеарат и др.
Мыла – это натриевые или калиевые соли высших жирных кислот. Общая формула твердого мыла: R-COONa; жидкого мыла: R-COOK. Получают мыло в результате щелочного гидролиза:

H2O
to
Основной состав любого твердого мыла одинаков. Это натриевые соли высших карбоновых кислот, обычно получаемых из жиров природного происхождения. Отличия заключаются в добавках, которые вносят в мыло в зависимости от его назначения. Основное назначение мыла – гигиеническое.
При умывании мыло соприкасается с водой и происходит его гидролиз. Соли мыла образованы сильными основаниями (гидроксидами натрия и калия) и слабыми высшими карбоновыми кислотами.
Химики - практики
определяют среду раствора мыла с помощью
универсальной лакмусовой бумаги и
записывают уравнение гидролиза мыла:
C17H35COONa
+ H2O
![]() C17H35COOН
+ NaOH.
C17H35COOН
+ NaOH.
Обычно мыло утрачивает свою моющую способность в жёсткой воде, поскольку растворимые натриевые или калиевые соли высших карбоновых кислот выступают в обменную реакцию с растворимыми гидрокарбонатами щелочноземельных металлов, главным образом кальция:
2C17H35COONa
+ Ca(HCO3)2
![]() (C17H35COO)2Ca
(C17H35COO)2Ca![]() + 2NaHCO3.
+ 2NaHCO3.
Практики определяют жёсткую и мягкую воду при помощи раствора мыла. Там, где удалось получить пену, – вода мягкая.
СМС. На смену мылу пришли СМС – ПАВ, в которых длинный углеводородный радикал (как в мыле) соединён с сульфатной или сульфонатной группой. Их производство основано на продуктах переработки нефти.
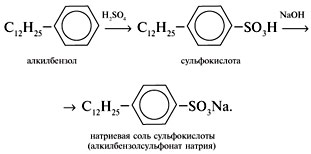
Алкилбензолсульфонат натрия – основной компонент многих детергентов (стиральных порошков). В отличие от нерастворимых стеаратов кальция и магния, которые образуются при стирке в жесткой воде и осаждаются на ткани, кальциевые и магниевые соли сульфокислот обладают более высокой растворимостью в воде. Следовательно, многие СМС одинаково хорошо моют как в мягкой, так и в жесткой воде.
3. Получение мыла (технологи).
В качестве сырья для получения мыла могут использоваться животные и растительные жиры (оливковое, кокосовое, пальмовое масло; говяжий, бараний, свиной, китовый, моржовый, тресковый жир), жирозаменители (синтетические жирные кислоты, канифоль, нафтеновые кислоты, талловое масло).
По способу получения мыла делят на клеевые, ядровые и пилированные, по целевому назначению - на хозяйственные, туалетные, технические и медицинские, по товарной форме - на твердые, жидкие и пастообразные.
Процесс получения мыл (мыловарение) состоит из варки мыла и придания ему товарного вида (охлаждение, формование, штамповка, упаковка). При варке мыла исходные жиры омыляют водным раствором щёлочи при кипячении с последующей нейтрализацией продукта омыления раствором Na2CO3 при кипячении и интенсивном перемешивании.
Варку мыла заканчивают обработкой мыльного раствора (мыльного клея) избытком щелочи или раствором хлорида натрия. В результате этого на поверхность раствора всплывает концентрированный слой мыла, называемый ядром. Полученное мыло называют ядровым, а процесс его выделения из раствора-высаливанием.
СМС. Еще в XIX веке русский химик Г.С.Петров действием серной кислоты на продукты переработки нефти получил синтетические моющие средства, которые прекрасно мылятся в жесткой воде. СМС, а попросту стиральные порошки, чаще всего содержат в своей основе не соли карбоновых кислот, а другие поверхностно-активные вещества, которые облегчают стирку и не боятся жесткой воды. Чаще всего в стиральных порошках и жидких смесях для стирки роль ПАВ играют соединения, в молекулах которых гидрофобный углеводородный радикал связан с гидрофильной сульфатной или сульфонатной группой. Синтетические моющие средства - это сложные смеси ПАВ с различными отбеливателями (химическими и оптическими), пенообразователями, умягчителями воды и биодобавками ферментов, разлагающих белковые или жировые загрязнения.
