
- •Лекция № 1 предмет органической химии
- •Теории химического строения
- •Основные положения теории бутлерова:
- •1. Положение о химическом строении.
- •2. Положение о зависимости свойств от химического строения.
- •3. Положение о взаимном влиянии атомов.
- •Классификация органических соединений
- •Электронные представления о природе химической связи
- •Электронная структура Схема основного электронного состояния
- •Образование ковалентной связи
- •Гибридизация электронов углерода. - и - связи.
- •Основные характеристики ковалентных связей
- •1. Полярность
- •2. Поляризуемость
- •3. Направленность связей
- •4. Длина связи
- •5. Энергия связи
- •6. Классификация органических реакций по механизму
- •Лекция № 2
- •Алифатические соединения (жирные, ациклические)
- •Способы получения предельных углеводородов
- •Лабораторные способы получения алканов
- •Пространственное строение предельных углеводородов
- •Физические свойства предельных углеводородов
- •Химические свойства предельных углеводородов
- •Получение и свойства алифатических радикалов
- •I тип. Реакция замещения
- •II тип. Реакции окисления
- •III тип. Реакции термического расщепления предельных углеводородов
- •IV тип. Изомеризация предельных углеводородов
- •Лекция 3 этиленовые углеводороды
- •Номенклатура
- •Способы получения
- •Физические свойства олефинов
- •Химические свойства олефинов
- •1. Реакции присоединения
- •Эффект Караша
- •Свойства карбкатионов
- •2. Реакции окисления
- •3. Реакции полимеризации
- •4. Реакции аллильного замещения
- •Отдельные представители
- •Лекция 4 диеновые углеводороды
- •Способы получения
- •Особенности электронного строения диенов с сопряженными связями
- •Физические свойства
- •Химические свойства
- •1. Реакции присоединения
- •2. Реакции окисления
- •3. Реакции полимеризации
- •Натуральный и синтетический каучук
- •Лекция 5 ацетиленовые углеводороды
- •Лабораторные методы получения ацетиленовых углеводородов
- •II. Реакции окисления
- •III. Реакции полимеризации и конденсации
- •Реакции замещения водорода металлом – образование ацетиленидов
- •Изомерия
- •Номенклатура
- •Способы получения
- •Электронное строение
- •Физические свойства
- •Химические свойства
- •I.Реакции нуклеофильного замещения
- •Реакции отщепления галогена
- •III. Реакции отщепления галогеноводорода
- •Лекция 7 галогенопроизводные непредельных углеводородов
- •I. Галогенопроизводные винильного типа. Получение
- •Особенности свойств
- •II. Соединения аллильного типа Получение
- •Получение
- •Отличие в физических и химических свойствах фторуглеводородов
- •Лекция 8 спирты (оксисоединения)
- •Свойства
- •Отдельные представители
- •Многоатомные спирты
- •Способы получения (кроме общих)
- •Физические свойства
- •Химические свойства
- •Рациональная система названий
- •Номенклатура iupac
- •Способы получения
- •Электронное и пространственное строение карбонильных соединений
- •Физические свойства
- •Химические свойства
- •Лекция 10
- •III. Реакции окисления и восстановления
- •Реакции восстановления
- •Классификация
- •Предельные одноосновные кислоты. Гомологический ряд
- •Изомерия
- •Номенклатура
- •Способы получения
- •1. Окисление углеводородов
- •3. Электронное строение
- •4. Физические свойства предельных одноосновных карбоновых кислот
- •5. Химические свойства карбоновых кислот
- •1) Кислотные свойства
- •4) Дегидратация кислот
- •5) Декарбоксилирование – отщепление со2.
- •Лекция 12 предельные двухосновные кислоты
- •Отличие в свойствах
- •Непредельные кислоты
- •Отличия в свойствах
- •Основные особенности геометрической изомерии
- •Номенклатура
- •Получение
- •Электронное строение нитросоединений
- •Физические свойства
- •Химические свойства
- •1.Определение и классификация
- •2. Изомерия, номенклатура
- •Номенклатура
- •Физические свойства
- •Химические свойства
- •Способы получения
- •Физические свойства
- •Химические свойства
- •Лекция 16 оптическая изомерия Оптическая активность
- •Динамическая стереохимия
- •Стереохимия нуклеофильного замещения
- •Стереохимия электрофильного присоединения
- •Стереохимия отщепления
Образование ковалентной связи
При сближении двух атомов, имеющих неспаренные электроны, происходит перекрывание электронных облаков неспаренных электронов, приводящее к образованию единой электронной орбитали с повышенной электронной плотностью между ядрами.
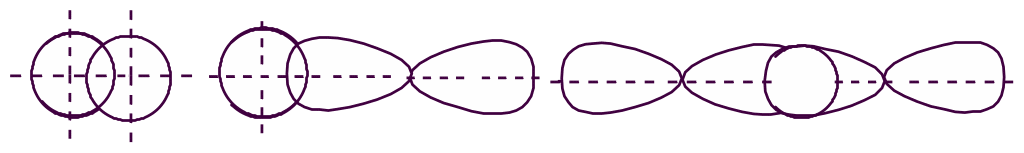

(1) (2) (3)
Рисунок 2
Возникающая между ядрами область повышенной электронной плотности обуславливает притяжение ядер и химическое связывание атомов. Таким образом, физический смысл образования ковалентной связи состоит в образовании из двух атомных орбиталей общей (связующей) орбитали с наибольшей электронной плотностью между ядрами, которую называют молекулярной орбиталью.
При рассмотрении характера связи и механизмов реакций удобно бывает пользоваться электронными формулами, где внешние электроны изображают в виде точек.
СН3-СН3 |
СН2=СН2 |
СН СН |
Н Н . . . . Н : С : С : Н . . . . Н Н |
Н Н . . . . Н : С : :С : Н |
Н : С ::: С : Н |
Разновидностью ковалентной связи является донорно-акцепторная, которая образуется за счет обобщения неподеленной пары электронов, принадлежащей одному из соединяющих атомов. Атом, дающий пару электронов, называется донором, атом, обобщающий ее – акцептором.
Донорами могут быть атомы O, N, S, имеющие неподеленные пары электронов, роль акцепторов выполняют атомы с незаполненной электронной оболочкой (с секстетом электронов) или протон.
При взаимодействии донора с протоном или молекулой, содержащей атом с секстетом электронов, образуется координационная связь, например
 +
+
Н H H
. . . . . .
Н :С:
N: + Н+:Сl-
H : C
: N : H
Cl-
:С:
N: + Н+:Сl-
H : C
: N : H
Cl-
. . . . . . . .
Н H H H
метиламин хлористый метиламмоний
При взаимодействии донора с атомом, имеющим секстет электронов, образуется семиполярная связь, например:
Н . . . . . . . . . . . . Н |
Н . . + Н:С: N::О: . . . . . . H :О:- . . |
нитрозометан |
нитрометан |
Семиполярную связь обычно изображают стрелочкой:
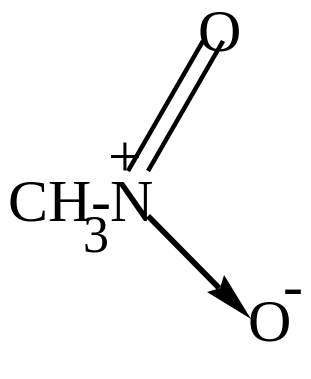
Донор отдает электрон и приобретает положительный заряд, акцептор принимает электрон и приобретает отрицательный заряд.

 Н:С: N::О:
+ О:
Н:С: N::О:
+ О: