
- •4.Константа электролитической диссоциации слабых электролитов. Закон разведения Оствальда.
- •5. Константа диссоциации воды. Ионное произведение воды. Водородный показатель рН.
- •6. Активность и коэффициент активности электролита. Средние ионные активности и коэффициенты активности. Средняя ионная моляльность, средний стехиометрический коэффициент.
- •7.Зависимость среднего ионного коэффнциента активности электролита от концентрации раствора и валентности ионов электролита. Ионная сила. Закон ионной силы.
- •8.Электролитическая теория сильных электролитов Дебая-Гюккеля, ионная атмосфера. Предельный закон Дебая-Гюккеля.
- •9.Удельная э/п р-ра,ее экс.Определение по сопротивл. Р-ра.Ед.Измер.В си.
- •12. Подвижность ионов.Ур-ние,связ. Подвижность(э/п)ионов при бескон.Разб.С пред.Эквив.Э/п р-ра(з-н Кольрауша).Опред.Степени дис.Слаб.Электрол.По э/п р-ра.
- •15.Кондуктометрия(кондукт.Титрование),опред.Растворимости и пр труднораствор.Соед,опред.РН р-ра.
- •16.Понятие о межфазной разности потенц.И строение двойного электр.Слоя на границе Ме-р-р.Нулевой р-р,потенц.Нулевого заряда.
- •17.Электр.Потенциал.Станд.Вод.Электрод.Зав-ть велич.Электр.Потенц.От прир.Электр.И от акт.Потенц.-опред.Ионов.Ур-ние Нернста.
- •18.Гальванический элемент. Процессы, протекающие на отрицательных и положительных электродах элемента. Правила записи гальванического элемента и электродных реакций.
- •31.Кинетика необратимых реакций третьего порядка
- •32.Кинетика Необратимые реакции n-ого порядка
- •34.Методы определения порядка реакции
- •37.Кинетика параллельных реакций первого порядка
- •1.Предмет электрохимии. Проводники первого и второго рода. Определение понятия электролит.
- •2.Основные положения теории электролитической диссоциации.Причины электролитической диссоциации электролитов при их растворении.
- •3.Сильные и слабые электролиты. Степень диссоциации, изотонический коэффициент.Уравнение связывающее степень диссоц. С изотон. Коэф.
- •46. Гетерогенный катализ
- •47.Мультиплетная теория гетерогенного катализа.
- •49.Цепные реакции.
18.Гальванический элемент. Процессы, протекающие на отрицательных и положительных электродах элемента. Правила записи гальванического элемента и электродных реакций.
Системы, состоящие из двух и более электродов, соединенные особым образом и способные производить электрическую работу, т. е. служить источником электрической энергии, называются гальваническими элементами.
Электрод, на котором протекает процесс окисления, называется анодом
Электрод, на котором протекает процесс восстановления, называется катодом
При записи гальванических элементов слева располагается электрод, имеющий более отрицательный потенциал; растворы обоих электродов отделяются друг от друга вертикальной пунктирной линией, если они контактируют друг с другом, и двумя сплошными линиями, если между растворами находится солевой мостик, например, насыщенный раствор КCl, с помощью которого устраняется диффузионный потенциал. Таким образом, справа всегда указывается положительно заряженный электрод, слева – отрицательно заряженный.
Пример:
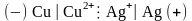
В результате работы
элемента на медном электроде будет
происходить процесс окисления:
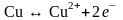
а
на серебряном электроде процесс
восстановления:
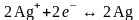
Реакции на катоде и аноде называются электродными реакциями.
Суммарный
химический процесс, протекающий
в гальваническом элементе, складывается
из электродных процессов и выражается
уравнением:
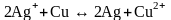
21.Зависимость величины электродных потенциалов от активности участников электродного процесса (для электродов I и II рода, газовых, амальгамных). для электродов I рода, обратимых относ. катиона:
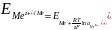
для
электродов I рода, обратимых относ.
аниона: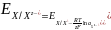
для газовых электродов:
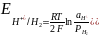
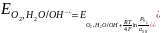
для амальгамных электродов:
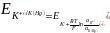
для электродов II рода:
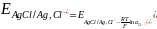
22.Основные типы гальванических цепей: химические и концентрационные. Диффузионный потенциал, причины его возникновения и способы устранения.
Химические цепи состоят из электродов, потенциалопределяющие реакции которых различны. Электрическая энергия возникает за счет энергии суммарной химической реакции.
Пример - серебряно-цинковый элемент:
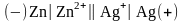 .
.
Концентрационные цепи состоят из электродов с одинаковыми потенциалопределяющими реакциями. Физические и химические свойства материала электродов одинаковы, но активности одного (или нескольких) участников реакции на каждом из электродов различны.
Пример:
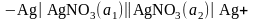 .
.
Диффузионный потенциал, разность потенциалов на границе двух соприкасающихся р-ров электролитов. Обусловлен тем, что скорости переноса катионов и анионов через границу, вызванную различием их элсктрохим. потенциалов в р-рах 1 и 2, различны. Снизить диффузионный потенциал до малой величины во мн. случаях можно, разделив р-ры 1 и 2 "солевым мостиком" из концентрир. р-ра соли, катионы и анионы к-рой имеют примерно равные числа переноса (КСl, NH4NO3 и др.).
23.Гальванические элементы с переносом и без переноса. Гальванические элементы классифицируются так же по наличию или отсутствию жидкостного соединения между двумя растворами гальванического элемента.
Цепь с переносом – это цепь с жидкостной границей. Например:
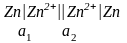
Цепь
без переноса – это цепь без жидкостной
границы. Например,
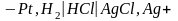
Поскольку электролит является общим для обоих электродов, диффузионный потенциал в таких цепях не возникает.
24.Компенсацинооый метод измерення ЭДС гальванического элемента. Элемент Вестона.
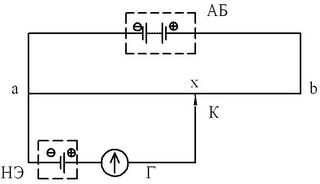
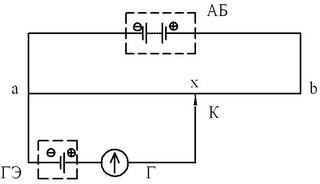
Принцип компенсационного метода измерения ЭДС состоит в урав-
новешивании измеряемой ЭДС ГЭ равным по величине и противополож-
ным по направлению падением напряжения U = IR на сопротивлении Ra-b
Нормальные элементы, гальванические элементы. обеспечивающие постоянную, точно воспроизводимую и слабо зависящую от температуры эдс.
Элемент Вестона:
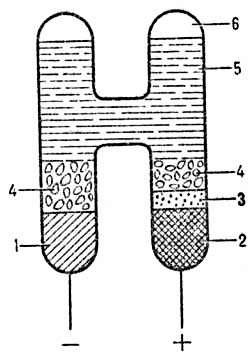
Конструкций нормального элемента Вестона: 1 - амальгама Cd (12,5% по массе); 2-Hg; 3-паста Hg2SO4 + + CdSO4.8/3H2O +Hg; 4-кристаллы CdSO4•8/3 Н2О; 5 -насыщ. раствор CdSO4.8/3H2O; 6- воздух.
2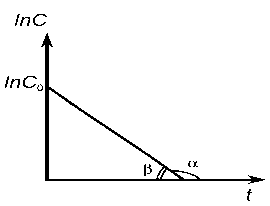 9.Необратимые
Реакции первого порядка.Кинетические
уравнения этих реакций.
9.Необратимые
Реакции первого порядка.Кинетические
уравнения этих реакций.
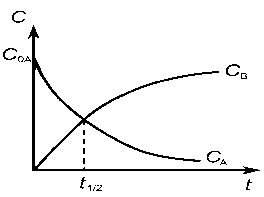 А
В.
А
В.
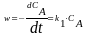 .,
.,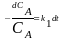 ,
,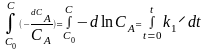 ,lnC
= lnC0
k1t,или
,lnC
= lnC0
k1t,или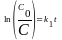 Отсюда
Отсюда
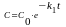 ,
т. е. концентрация вещества А
в ходе реакции уменьшается экспоненциально
продуктов нарастает тоже по экспоненте.
[, с1
или мин1].
,
т. е. концентрация вещества А
в ходе реакции уменьшается экспоненциально
продуктов нарастает тоже по экспоненте.
[, с1
или мин1].
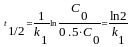 Зависимость
логарифма концентрации вещества А
от времени имеет линейный характер,
что следует из уравнения и представлена
(tg
=
k1
или k1
= tg ).
Зависимость
логарифма концентрации вещества А
от времени имеет линейный характер,
что следует из уравнения и представлена
(tg
=
k1
или k1
= tg ).
30.Необратимые реакции второго порядка.Кинетические уравнения этих реакций для(С0А=С0В,С0А≠С0В)
А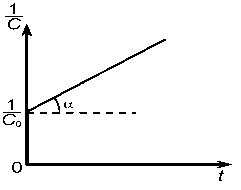 + В
D.
+ В
D.
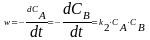 Если
начальные концентрации веществ А
и В
равны (С0А
= С0В
=
С0),
реакция может быть представлена в
виде2А
D.
Если
начальные концентрации веществ А
и В
равны (С0А
= С0В
=
С0),
реакция может быть представлена в
виде2А
D.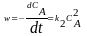 ,
,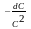 =
k2dt
,
=
k2dt
,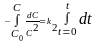 ,
,
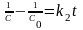 ,
[концентрация1·время1].
[л/(моль·сек)].:
,
[концентрация1·время1].
[л/(моль·сек)].: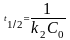 .
Зависимость обратной концентрации
вещества А
от времени имеет линейный характер Эта
зависимость дает возможность определить
k2
(k2
= tg)..В
случае, когда для реакции второго
порядка А + В D
(С0А С0В),
.
Зависимость обратной концентрации
вещества А
от времени имеет линейный характер Эта
зависимость дает возможность определить
k2
(k2
= tg)..В
случае, когда для реакции второго
порядка А + В D
(С0А С0В),
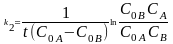 ,
,
