
- •270101 – Механическое оборудование и технологические комплексы предприятий строительных материалов, изделий и конструкций
- •Определение твердости по Бринеллю
- •Практика определения твердости по Бринеллю
- •Определение твердости по Роквеллу
- •Практика определения твердости по Роквеллу
- •Порядок выполнения работы
- •Контрольные вопросы.
- •Лабораторная работа №2 Влияние холодной пластической деформации на структуру и свойства стали
- •Пластическая деформация и рекристаллизация
- •Порядок выполнения работы
- •Лабораторная работа №3 Диаграммы состояния железо-углеродистых сплавов Компоненты и фазы в системе железо – углерод
- •Диаграммы состояния железо-углеродистых сплавов
- •Кристаллизация сплавов Fe-Fe3c
- •Вопросы для повторения раздела
- •Лабораторная работа №4 Изучение структуры и свойств углеродистых сталей в равновесном состоянии
- •Порядок выполнения работы
- •Контрольные вопросы
- •Лабораторная работа №5 Изучение структуры и свойств чугунов
- •Белые чугуны
- •Серые чугуны
- •Ковкие чугуны
- •Высокопрочные чугуны
- •Легированные чугуны
- •Контрольные вопросы
- •Лабораторная работа №6 Термическая обработка углеродистых сталей
- •Основные понятия
- •Влияние скорости охлаждения на структуру и свойства стали
- •Перлитное превращение
- •Промежуточное (бейнитное) превращение
- •Мартенситное превращение аустенита
- •Виды термической обработки
- •Отжиг стали
- •Рекрист.
- •Нормализация стали
- •Закалка стали
- •Отпуск стали
- •Порядок выполнения работы
- •Контрольные вопросы
- •Контрольные тесты
- •Ответы на тест
- •Библиографический список
- •270101 – Механическое оборудование и технологические комплексы предприятий строительных материалов, изделий и конструкций
- •308012, Г. Белгород, ул. Костюкова, 46
Порядок выполнения работы
В данной работе студенты знакомятся с изменением формы, размеров зерен и твердости металла, подвергнутого холодной пластической деформации и рекристаллизационному отжигу.
При выполнении работы необходимо выполнить следующее.
-
Привести краткое изложение основных теоретических положений.
-
По образцам лабораторной коллекции изучить, зарисовать в табл. 4 и объяснить микроструктуру недеформированной части образца и частей образцов, подвергнутых холодной пластической деформации различной степени (рис. 10) и установить зависимость твердости поверхностей образца от степени пластической деформации.
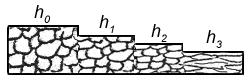
Рис. 10. Образец, подвергнутый холодной пластической деформации разной степени
Степень холодной пластической деформации подсчитывается в процентах как отношение
![]()
где h0 – толщина образца до холодной пластической деформации, мм;
hi – толщина образца после холодной пластической деформации, мм;
Результаты записать в табл. 4.
Таблица 4
|
Степень пластической деформации ε, % |
Твердость HRC |
Микроструктура |
|
|
|
|
-
По данным табл. 4 построить график HRС = f(ε). Сделать вывод.
Лабораторная работа №3 Диаграммы состояния железо-углеродистых сплавов Компоненты и фазы в системе железо – углерод
Железо – металл сероватого цвета. Атомный номер 26, атомная масса 55,85, атомный радиус 0,127 нм. Температура плавления железа 1539°С. Железо имеет две полиморфные модификации α и γ. Модификация α-железа существует при температурах ниже 910°С и выше 1392°С (рис. 11). В интервале температур 1392–1539°С α-железо нередко обозначают как δ-железо.
Углерод является неметаллическим элементом II периода IV группы периодической системы, атомный номер 6, плотность 2,5 г/см3, температура плавления 3500°С, атомный радиус 0,077 нм. Углерод полиморфен. В обычных условиях он находится в виде модификации графита, но может существовать и в виде метастабильной модификации алмаза.
Углерод растворим в железе в жидком и твердом состояниях, а также может быть в виде химического соединения – цементита, а в высокоуглеродистых сплавах и в виде графита.
В системе Fe-C различают следующие фазы: жидкий сплав (Ж), твердые растворы – феррит и аустенит, а также цементит и графит.
Феррит (Ф) – твердый раствор внедрения углерода в α-железе, имеющий объемноцентрированную кубическую решетку (ОЦК). Различают низкотемпературный α-феррит с растворимостью углерода до 0,02% и высокотемпературный δ-феррит с предельной растворимостью углерода 0,1%. Феррит имеет следующие механические свойства: σв = 250 МПа, σт = 120 МПа, δ = 50%, ψ = 80%, НВ 800.
Аустенит (А) – твердый раствор внедрения углерода в γ-железе, имеющий гранецентрированную кубическую решетку (ГЦК). Предельная растворимость углерода в γ-железе – 2,14%. Он имеет твердость НВ 1600–2000; δ = 40…50%.
Цементит (Ц) – химическое соединение железа с углеродом (карбид железа Fe3C), содержит 6,67% С, имеет сложную ромбическую решетку с плотной упаковкой атомов. Температура плавления цементита точно не определена в связи с возможностью его распада и принимается равной 1550°С. Цементит магнитен и характеризуется высокой твердостью НВ 8000.
Графит представляет собой свободный углерод. Кристаллическая решетка графита гексагональная. Он мягок, электропроводен, химически стоек, малопрочен.
