
- •Фгбоу впо «орловский государственный аграрный университет»
- •Химические свойства кислот
- •Содержание
- •4.1.1.Неорганические кислоты………………………………………....15
- •Введение.
- •1.Определение кислоты.
- •1.1.Показатель рН: измерение кислотности.
- •2.Классификация кислот.
- •2.1.Неорганические кислоты.
- •2.2.Органические кислоты.
- •3. Химические свойства кислот.
- •3.1.Химические свойства неорганических кислот.
- •3.2.Химические свойства органических кислот.
- •4. Получение кислот.
- •4.1.Наиболее распространённые кислоты, часто используемые в хозяйстве:
- •4.1.1.Неорганические кислоты.
- •4.1.2.Органические кислоты.
- •Заключение.
- •Список литературы.
3.2.Химические свойства органических кислот.
-
Диссоциация кислот. В водном растворе карбоновые кислоты диссоциируют:
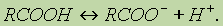
Однако это равновесие диссоциации сильно сдвинуто влево, поэтому карбоновые кислоты, как правило, слабые кислоты.
-
Образование солей. Карбоновые кислоты обладают всеми свойствами обычных кислот: реагируют с активными металлами, основными оксидами, основаниями:
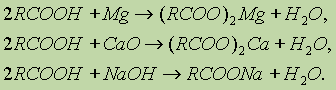
Карбоновые кислоты — слабые, поэтому сильные минеральные кислоты вытесняют их из соответствующих солей.
-
Образование функциональных производных. При замещении группы ОН в карбоновых кислотах различными группами (X) образуются функциональные производные кислот, имеющие общую формулу R—СО—X; здесь R означает алкильную либо арильную группу.
Хлорангидриды получают действием хлорида фосфора (V) на кислоты:
![]()
Сложные эфиры образуются при нагревании кислоты со спиртом в присутствии серной кислоты (обратимая реакция этерификации):
![]()
-
Ряд свойств карбоновых кислот обусловлен наличием углеводородного радикала. Так, при действии галогенов на свету образуются галогензамещенные кислоты:
![]()
Непредельные карбоновые кислоты способны к реакциям присоединения.
-
Окислительно-восстановительные реакции карбоновых кислот.
Карбоновые кислоты при действии восстановителей способны превращаться в альдегиды или спирты:
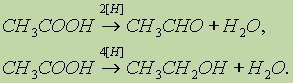
Насыщенные карбоновые кислоты устойчивы к действию концентрированных серной и азотной кислот. Исключение составляет муравьиная кислота:
![]()
Муравьиная кислота НСООН отличается рядом особенностей, поскольку в ее составе есть альдегидная группа:
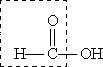
Муравьиная кислота — сильный восстановитель и легко окисляется до СО2. Она дает реакцию “серебряного зеркала”:
![]()
Кроме того, муравьиная кислота окисляется хлором:
![]()
4. Получение кислот.
Получение кислот производят с помощью следующих химических реакций: - взаимодействие кислотных оксидов с водой: SO3 + H2O = H2SO4;
CO2 + H2O = H2CO3; - взаимодействие с солями: NaCl + H2SO4(конц.) = HCl + Na2SO4 - при этой химической реакции образуется новая более слабая кислота (более слабая, чем серная, но тоже сильная) и другая соль; - взаимодействие неметаллов с водородом с последующим растворением их в воде:H2 + Cl2 = HCl (Надо помнить, что само по себе данное химическое соединение - газ хлороводород HCl кислотой не является. Для её образования необходимо полученный газ HCl растворить в воде). Аналогичным образом поступают с газом сероводородом:H2 + S = H2S; - оксиление некоторых простых веществ:P + 5HNO3 +2H2O = 3H3PO4 + 5NO (в этой химической реакции происходит окисление фосфора (P) азотной кислотой (HNO3) до ортофосфорной кислоты (H3PO4) с выделением оксида азота (NO)
-окисление альдегидов и первичных спиртов :
|
|
[O] |
|
[O] |
|
|
R-CH2-OH |
→ |
R-CH=O |
→ |
R-CO-OH |
|
спирт |
альдегид |
кислота |
||
— гидролиз галогензамещенных углеводородов, содержащих, три атома галогена у одного атома углерода. При этом образуются спирты, содержащие группы ОН у одного атома углерода — такие спирты неустойчивы и отщепляют воду с образованием карбоновой кислоты:
|
|
ЗNаОН |
|
|
|
|
R-CCl3 |
→ |
[R-C(OH)3] |
→ |
R-COOH + Н2О |
|
|
-3NaCl |
|
|
|
-получение карбоновых кислот из цианидов (нитрилов) — это важный способ, позволяющий наращивать углеродную цепь при получении исходного цианида. Дополнительный атом углерода вводят в состав молекулы, используя реакцию замещения галогена в молекуле:СН3-Вr + NaCN → CH3 - CN + NaBr
Образующийся нитрил уксусной кислоты (метилцианид) при нагревании легко гидролизуется с образованием ацетата аммония:
CH3CN + 2Н2О → CH3COONH4.
При подкислении раствора выделяется кислота:
CH3COONH4 + HCl → СН3СООН + NH4Cl.
-гидролиз сложных эфиров:
R-COOR1 + КОН → R-COOK + R'OH ,
R-COOK + HCl → R-COOH + KCl .
