
- •Глава 5. Липиды
- •5.1. Общая характеристика и классификация липидов
- •5.2. Липидные мономеры
- •2. Высшие алифатические спирты, альдегиды, кетоны.
- •5.3. Многокомпонентные липиды
- •5.4. Биологические функции липидов
- •Глава 6. Ферменты
- •6.2. Химическая природа и структура ферментов
- •6.3. Кофакторы ферментов Ионы металлов как кофакторы ферментов
- •Коферменты
- •6.4. Механизм действия ферментов
- •6.5. Свойства ферментов
- •6.6. Специфичность действия ферментов
- •6.7. Факторы, влияющие на скорость ферментативного катализа
- •Влияние температуры на активность ферментов
- •Влияние рН на активность ферментов
- •Влияние концентраций субстрата и фермента на скорость ферментативной реакции
- •Зависимость скорости реакции от времени
- •6.8. Регуляция активности ферментов
- •Активация ферментов
- •Ингибирование ферментов
- •Аллостерическая регуляций действия ферментов
- •6.9. Определение активности ферментов
- •6.10. Номенклатура и классификация ферментов
- •6.11. Локализация ферментов в организме и клетке
- •6.12. Применение ферментов
6.7. Факторы, влияющие на скорость ферментативного катализа
Скорость ферментативной реакции определяется количеством вещества, превращающимся в единицу времени, и зависит от температуры, рН среды, концентрации субстрата и фермента.
Скорость ферментативной реакции является мерой активности фермента. Активность фермента можно измерить только косвенно: по количеству превращаемого субстрата или получаемого продукта реакции в единицу времени.
Влияние температуры на активность ферментов
Зависимость каталитической активности от температуры (термолабильность) для большинства ферментов выражается типичной кривой, представленной на рис.16.
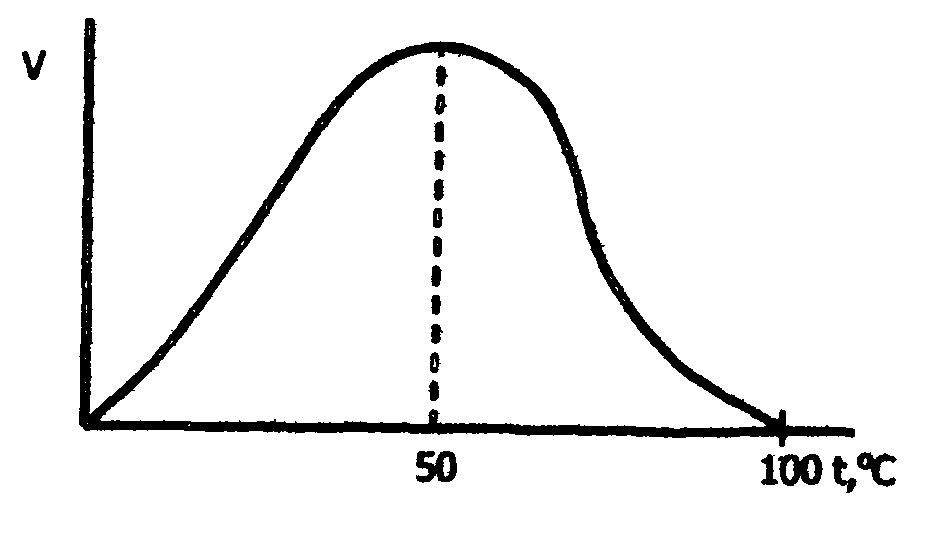
Рис. 16. Зависимость скорости ферментативной реакции от температуры
Скорость ферментативных реакций, как и любых других, при повышении температуры на каждые 10 °С увеличивается примерно в 2-4 раза (правило Вант-Гоффа), но это правило справедливо лишь в области температур до 50-60°С. При температуре выше 50°С начинается денатурация фермента, что означает уменьшение его количества и соответственно снижается скорость реакции. При температурах 80-100°С почти все ферменты утрачивают свою активность (исключение составляет только один фермент мышечной ткани - миокиназа, который выдерживает нагревание до 100°С). Оптимальной для действия ферментов животного происхождения является температура 40-50°С, а для растительного - 50-60°С. Однако есть ферменты с более высокими оптимальными температурами, например, у папаина (фермента растительного происхождения, ускоряющего гидролиз белка) он равен 80°С. В то же время у каталазы (фермента, ускоряющего распад перекиси водорода до воды и О2 ) оптимальная температура действия находится между 0 и 10°С, а при более высоких температурах происходит инактивация ферментов. При температурах 0°С и ниже большинство ферментов не разрушается, но их активность стремится к нулю.
Свойство термолабильности ферментов имеет важное значение для понимания процессов жизнедеятельности. При снижении температуры некоторые животные впадают в состояние спячки или анабиоза. При этом скорость ферментативных процессов уменьшается, что снижает расход накопленных организмом питательных веществ и замедляет обмен веществ. Искусственное охлаждение организма (гибернация) используется в клинике для проведения хирургических операций.
Влияние рН на активность ферментов
Зависимость скорости ферментативной реакции от концентрации водородных ионов носит колоколообразный характер (рис. 17). Каждый фермент имеет свой оптимум рН среды, при которой он максимально активен. Большинство ферментов имеет максимальную активность при физиологическом значении рН среды 6,0-8,0, однако некоторые ферменты хорошо работают или в кислой (пепсин), или в щелочной (аргиназа) среде. В табл. 8 приведены оптимумы рН ряда ферментов.
Влияние изменения рН среды на молекулу фермента состоит в изменении степени ионизации кислотных и основных групп активного центра фермента, что сказывается на третичной структуре белка и соответственно на формировании активированного фермент-субстратного комплекса. Кроме того, имеет значение состояние ионизации субстрата и кофермента.
Таблица 8
Оптимальное значение рН для некоторых ферментов
|
Название фермента |
Катализируемая реакция |
рН |
|
Пепсин |
Гидролиз белка |
1,5-2,5 |
|
Липаза (из семян клещевины) |
Гидролиз жиров |
4,7-5,0 |
|
Каталаза |
Разложение перекиси |
6,8-7,0 |
|
Уреаза |
Гидролиз мочевины |
7,0-7,2 |
|
Трипсин |
Гидролиз белка |
7,5-8,5 |
|
Аргиназа |
Гидролиз аргенина |
9,5-10,0 |
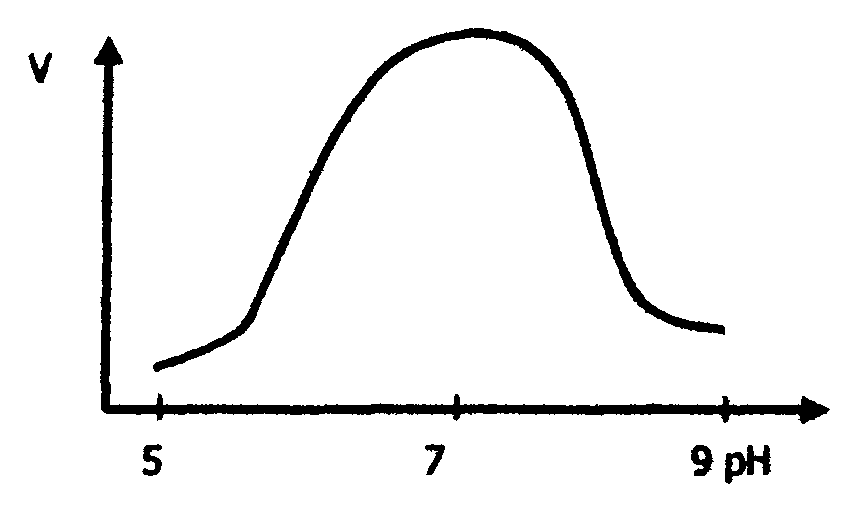
Рис. 17. Зависимость скорости ферментативной реакции от рН среды
Значение оптимумов рН для разных ферментов важно для практической медицины. Например, пепсин, гидролизующий белки в желудке, активно работает только в сильнокислой среде (см. табл.8). Поэтому для восстановления нарушенной активности эндогенного пепсина необходимы вещества, повышающие кислотность. Так, препарат пепсина принимают с соляной кислотой, создающей нужный рН.
