
- •2.Значение биохимии для диагностики заболеваний.
- •3. Значение биохимии для лечения. Выявление нарушенных звеньев метаболизма и создание соответствующих лекарственных препаратов, широкое использование природных препаратов.
- •4.Значение биохимии для профилактики заболеваний.
- •1 .Альфа спираль ( л.Поллинг) - виток составляет от 3 до 6 ак. Терминатором спирали является ак-пролин.
- •2.Бетта складчатый слой.
- •3.Петли полипептидной цепи (соединительные петли).
- •2.Способность белков связываться с лигандами,
- •3.Электрохимические свойства белков.
- •1. Концевыми соон и nh2 группами.
- •2.Боковыми группами:
- •1.Ионообменная хроматография.
- •2.Разделение белков на основании величины заряда - электрофорез белков. С помощью электрофореза в сыворотке крови выделяют как минимум 5 фракций: альбумины, альфа, альфа-2, гамма, бета - глобулины.
- •4.Коллоидные свойства белков.
- •5. Гидратация белков - способность белков связывать воду. Она осуществляется за счёт:
- •1 .Белковой частью (состоит из ак) - апофермент;
- •2.Небелковой частью - кофактор.
- •4.Специфичность действия ферментов. В основе специфичности действия ферментов лежит конформационное соответствие его активного центра молекуле субстрата. Различают следующие виды специфичности:
- •1.Обратимые - это соединения, которые нековалентно взаимодействуют с ферментом, при этом образуется комплекс, способный к диссоциации.
- •1 .Механизм окислительного фосфорилирования.
- •2.Альтернативные пути биологического окисления.
- •3.Свободно-радикальное окисление.
- •1.Мембрана митохондрий не проницаема для протонов.
- •2.Образуется протонный потенциал в процессе транспорта электронов и протонов.
- •3.Обратный транспорт протонов в матрикс сопряжен с образованием атф.
- •2. Вторичные радикалы (он, липидные радикалы – l,, lo,, loo,) Их образование происходит с участием железа (11). Это патологические продукты.
- •3. Третичные радикалы (антиоксиданты) - образуются под влиянием вторичных радикалов.
- •2.Она раздражает слизистую оболочку жкт, усиливая секрецию желёз.
- •3.Усиливает сокращение кишечника,
- •4.В толстом кишечнике под действием ферментов условно-патогенной микрофлоры клетчатка подвергается брожению с образованием глюкозы, лактозы и газообразных веществ.
- •1. Основной фосфоролитический путь
- •2.Неосновной амилолитический.
- •1.Надф*н2, который в отличии от надн2 не используется вдыхательной цепи митохондрий, а поступает клетке для реакций синтеза и восстановления веществ.
- •2.Рибозо-5-фосфата и др. Пентоз, которые используются в клетке для синтеза важнейших биологических молекул: днк, рнк, нтф (атф, гтф, цтф, ттф),н5коа, над, фад).
- •1. Транскетолазные реакции:
- •2. Трансальдолазная реакция:
- •1. Ув пищи,
- •2. Гликоген тканей
- •3. Глюконеогенез.
- •1.Липиды, их классификация и биологическая роль.
- •2.Превращение липидов в органах пищеварения.
- •1.Структурными липидами.
- •2.Резервными липидами.
- •3.Свободными липидами. — хиломикроны,
- •1. Эмульгируют пищевые жиры.
- •2. Активируют липолитические ферменты.
- •3. Выполняют роль переносчиков трудно растворимых в воде продуктов гидролиза жира и жирорастворимых витаминов a, d, е, к.
- •1.Транспортные липопротеины крови. Состав и биологическая роль. 2.Простагландины, простациклины, тромбоксаны, лейкотриены. Механизм их образования и биологическая роль.
- •3.Окисление глицерина и вжк в тканях.
- •1.Простагландины:
- •1.Биосинтез вжк в тканях, химизм реакций, биологическая роль. 2.Холестерин, биологическая роль, биосинтез, окисление. 3.Патология липидного обмена.
- •1.Наличие атф, со2, н2о, надф*н2, поступающий из гексозомонофосфатного пути превращения глюкозы.
- •2.Наличие специальных белков-переносчиков (hs -апб). 3.Наличие специальных ферментов синтеза.
- •1.Структурная. Свободный холестерин является, обязательным структурным компонентом мембран клеток.
- •2.Метаболическая. Холестерин является предшественником биологически активных веществ: витамина d3
- •1. Пища. За сутки в организм взрослого человека поступает 0,3гр. Холестерина.
- •1 .На этапе поступления жиров с пищей:
- •2.На этапе пищеварения.
- •2.На этапе пищеварения.
- •2.Бета -аминоизобутират.
- •1. Нарушение на этапе поступления белков. В норме в организм должно поступать 80 - юОгр белков. Обязательно поступление всех незаменимых ак.
- •2. Нарушение на этапе пищеварения:
- •3. Нарушение межуточного обмена - нарушение обмена аминокислот в тканях.
- •5. Праймеры - «затравка» для репликации. Это короткий фрагмент, состоящий из рибонуклеотидтрифосфатов (2 - 10). Образование праимеров катализируется праймазой.
- •1.Инициация репликации.
- •2. Репарация днк.
- •3. Транскрипция гена.
- •1.Рекогниция (распознавание) - узнавание между аминокислотами и их транспортной
- •3. Инициация - начало процесса трансляции.
- •4. Элонгация (продолжение) протекает циклически в виде последовательной смены трёх фаз:
- •5. Терминация (прекращение).
- •6. Броцессинг белка (созревание) совокупность химических модификаций
- •1. Регуляция происходит только на уровне транскрипции. Первичные транскрипты генов у них транслируются до завершения транскрипции.
- •1. Первые представления о гене.
- •2. Современные представления о природе биохимического полиморфизма.
- •3. Современные представления структурно-функциональной организации днк.
- •1. Выделение днк из биологического материала.
- •2. Амплификация - репликация на органическом участке молекулы днк. Производится за счёт работы ферментов и смены температурных режимов.
- •3. Детекция продуктов pcr (копий заданного участка) Схема pcr:
- •1. Структурные гены
- •2. Регуляторные элементы
- •1. Фенотипическое различие между клетками,
- •2. Индивидуальные различия между организмами одного вида. Каждый человек отличается от другого человека на 0,1% генома.
- •3. Широкое разнообразие белков. На основе 35000 генов синтезируются около 5000000 белков. В настоящее время нельзя сказать точно, что изучать важнее - геном или белковый состав организма.
- •1. Углеводный обмен:
- •Высококалорийное питание,
- •Преобладание консервированных продуктов в рационе, рафинированных или высокоочищенных продуктов,
- •Малое движение (гиподинамия).
- •Регулирует интенсивность свободно радикальных процессов. Препятствует активации перекисного окисления жиров, обеспечивая тем самым стабильность биологических мембран.
- •Витамин е повышает биологическую активность витамина а.
- •1. Участие в окислительно-восстановительных реакциях:
- •2. Синтез кортикостероидов
- •Высокая потребность,
- •Неустойчивость химической структуры,
- •Отсутствие депо.
- •1. Входит в состав тдф: тиамин(атф) ® тдф
- •2.Участвует в передаче нервного импульса.
- •I. Метилирование в12
- •2.Деметелирование в12 метилтетрогидрофолевая к-та ® тетрогидрофолевая к-та
- •II. Аденозилкобаламин в12
- •1. Является ко-ферментом карбоксилаз пвк, ацетил -коа, пропионил-коа.
- •2. Участвует в реакциях синтеза жирных кислот и стерина.
- •1. Входит в состав ко-фермента а, следовательно, участвует в синтезе ацетил-коа, различных ацил-коа, образующихся в результате следующих реакций:
- •2. Участвует в синтезе более 80 различных ферментов.
- •Витаминоподобные вещества.
- •1. Прямо воздействующие:
- •2. Структуры аналогичные витаминам:
- •1. Надпеченочная желтуха (гемолитическая).
- •2. Печеночная желтуха (токсические и вирусные и другие гепатиты).
- •3. Подпеченочная желтуха (механическая).
- •1. Транспортирует ионы меди, связывает и удерживает их в кровеносном русле
- •3. Обладает противовоспалительным действием
- •4. Является антиоксидантом, обезвреживает активные формы кислорода и пол.
- •IgD. Функция неизвестна.
- •1. Метаболиты: аминокислоты (25%), креатин (5%), полипептиды и нуклеотиды (3,5%)
- •2. Конечные азотистые продукты: мочевина(50%), мочевая кислота (4%), креатинин (2,5%), индикан и аммиак.
- •1.Экскреторная функция - это выделение мочевины, мочевой кислоты, креатина, лекарств, токсинов, избытка воды, микроэлементов, электролитов. Состоит из трёх фаз:
- •2.Регуляторная и гомеостатическая.
2. Участвует в синтезе более 80 различных ферментов.
Суточная потребность 10-15мг. Источники: печень, дрожжи, пчелиное молочко. Синтезируется микрофлорой кишечника. Гиповитаминоз характеризуется поражением -малых -артерий нижних конечностей. В эксперименте наблюдался некроз надпочечников.
Витаминоподобные вещества.
Синтезируются в организме, но в недостаточном количестве. Потребность в них измеряется в граммах. Например, витамин F, содержащий три незаменимые аминокислоты (ЛИНОЛЕВУЮ, ЛИНОЛЕНОВУЮ, АРАХИДОНОВУЮ). Его относят в настоящее время к витаминподобным веществам. Т.к. суточная потребность в нём до 10гр.
ПАБК (ПАРААМИНОБЕНЗОЙНАЯ К-ТА)
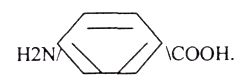
-
Участвует в образовании ФОЛИЕВОИ кислоты,
-
Участвует в образовании ряда ферментов,
-
Является фактором пигментации.
Недостаточность ПАБК проявляется в виде нарушения
пигментации. Суточная потребность не установлена. Источники: печень, дрожжи и другие продукты.
87.

-
Донор - СНЗ групп для образования ПУРИНОВЫХ и ПИРИМИДИНОВЫХ оснований.
-
Необходим для образования АЦЕТИЛ ХОЛИ НА.
Суточная потребность: 0,5 - 1 гр. Источники: желток яиц, печень, почки и др. продукты.
ОРОТОВАЯ КИСЛОТА ( является пиримидиновым основанием)

азотистых оснований, предшественников аминокислот. Содержится в дрожжах и печени.
ПАНГАМОВАЯ КИСЛОТА - производное глюкуроновой кислоты и диметилглицина. В организме быстро гидролизуется. ИНОЗИТ (производное циклогексана)
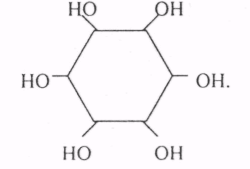
АНТИВИТАМИНЫ - это вещества, нарушающие усвоение витаминов или понижающие
биологическую активность витаминов.
По действию различают АНТИВИТАМИНЫ:
1. Прямо воздействующие:
белок яйца АВЕДИН + БИОТИН не усваиваются ТИАМИНАЗА - разрушение тиамина.
2. Структуры аналогичные витаминам:

СА включается в ферменты микроорганизмов, не отличающие их по структуре. Функции
ферментов нарушается, и микроорганизмы погибают.
МЕТОТРИКСАН - антивитамин фолиевой кислоты. Используется как противоопухолевый
препарат, снижает белок синтетические процессы в клетках.
ДИКУМАРИН - антивитамин К, снижающий свёртываемость крови.
ФТИВАЗИД, ТУБАЗИД - антивитамин В6.
СОСТОЯНИЕ ВИТАМИННОЙ ОБЕСПЕЧЕННОСТИ В СОВРЕМЕННЫХ УСЛОВИЯХ.
В результате многочисленных исследований витаминной обеспеченности было установлено, что глубокий дефицит витаминов наблюдается менее чем у 20% населения, а содержание витаминов ниже нормы наблюдается у 50 - 90% населения. Содержание витаминов определяется в крови. Дают нагрузку витамином с последующим его определением в моче. Если наблюдается дефицит витамина в организме, то в моче он не определяется даже после нагрузки. Недостаточная витаминная обеспеченность проявляется: (1) повышенная утомляемость; (2) повышенная сонливость; (3) повышенная восприимчивость к заболеваниям; (4) повышена частота сердечно-сосудистых заболеваний; (5) повышение тяжести переноса заболеваний. При этом отсутствует специфическая клиническая симптоматика, как при гиповитаминозах. Причины недостаточной витаминной обеспеченности:
1. Снижение затрат энергии в современных условиях, следовательно, необходимость снижение
потребления пищи.
88.
2. Повышение потребления рафинированных продуктов, калорийных, но бедных витаминами.
3. Использование консервированных продуктов длительного хранения. Выход:
1. Витаминизация пищи.
2. Поливитамины с не менее 8-9 компонентами.
Рацион современного человека, достаточный по калорийности, не может удовлетворить потребность организма в витаминах и микроэлементах.
Лекция № 29. Биохимия печени.
1. РОЛЬ ПЕЧЕНИ В ПИГМЕНТНОМ ОБМЕНЕ. БИОСИНТЕЗ И РАСПАД ГЕМА.
2. ПАТОЛОГИЯ ПИГМЕНТНОГО ОБМЕНА. ВИДЫ ЖЕЛТУХ.
Основным источником пигментов для организма являются гемсодержащие белки. Эти сложные белки объединяет их небелковая часть, которая представлена гемом.
ТЕТРАМЕТИЛДИВИНИЛДИПРОПИОНОВОКИСЛЫЙ ПОРФИН. Основную массу всех гемпротеинов организма человека составляет гемоглобин, находящийся в эритроцитах крови и клетках костного мозга (82%). 17% тема содержится в миоглобине скелетных мышц и миокарда. На долю клеточных гемпротоинов (ферменты, ПЕРОКСИДАЗЫ, ЦИТОХРОМЫ) приходится 1%.
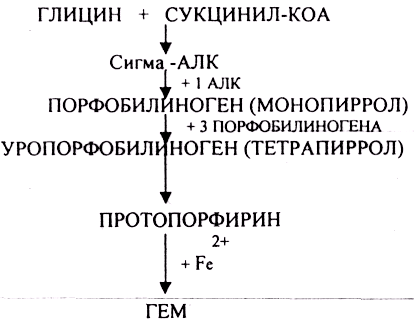
БИОСИНТЕЗ ГЕМА.
Исходным материалом в синтезе является глицин и активная форма янтарной кислоты и образующийся из них сигма -АМИНОЛЕВУМИНОВАЯ кислота (АЛК). В дальнейшем из двух молекул этой кислоты образуется МОНОПИРРОЛ. Далее при конденсации четырёх молекул монопиррола образуется ТЕТРАПИРРОЛ, дальнейшее превращение которого в гем предусматривает ДЕКАРБОКСИЛИРОВАНИЕ, окисление с последующим включением атома железа. Печень и костный мозг с ядросодержащими эритроцитами занимают центральное место в биосинтезе. В меньшей степени биосинтез возможен в почках и слизистой кишечника.
РАСПАД ГЕМА.
За сутки в организме взрослого человека в среднем с массой 70кг распадается около 9гр гемпротеинов, главным образом за счёт распада эритроцитов, в которых содержится гемоглобин. Средняя продолжительность жизни эритроцитов составляет 3,5-4 месяца. Разрушение эритроцитов происходит в кровяном русле или селезёнке, что ведёт к высвобождению гемоглобина, который связывается с альфа2 -ГЛОБУЛИНАМИ плазмы и в виде комплекса ГЕМОГЛОБИН-ГАПТОГЛОБИН попадает в клетки РЭС, главным образом селезёнки, печени и соединительной ткани. Гаптоглобин, отщепляясь, переходит в кровь, а гемоглобин, окисляясь, подвергается распаду с образованием желчных кислот БИЛИВЕРДИНА и БИЛЛИРУБИНА (очень токсичные вещества). Освобождающийся из гемоглобина гем повторно не используется. Железо утилизируется. Распад гемоглобина начинается с разрыва одного из метильных мостиков с образованием ВЕРДОГЛОБИНА. Это первая стадия распада, катализируемая ферментом ГЕМОКСИТЕНАЗОЙ, требующей присутствия кислорода и НАДФ*Н2.
В дальнейшем от молекулы ВЕРДОГЛОБИНА отщепляется ГЛОБИН и железо с образованием БИЛЛИВЕРДИНА, который в дальнейшем превращается при восстановлении в БИЛЛИРУБИН (коричневого цвета). Он тоже очень токсичен, поэтому из клеток РЕС он удаляется. В крови он соединяется с белком АЛЬБУМИНОМ, образуя комплексное соединение БИЛЛИРУБИН-АЛЬБУМИН. Его принято называть неконъюгированным биллирубином (НБ). Ранее его называли непрямым, поскольку он не мог быть открыт прямой реакцией с реактивом ЭРЛИХА, а открывается только при осаждении белка. Он имеет свойства: токсичен, гидрофобен. не способен фильтроваться почками, не даёт прямой реакции с реактивом ЭРЛИХА. Поступая в печень, НБ обезвреживается. Выполнив транспортную роль, с током крови уходит альбумин, а в клетках печени биллирубин будет конъюгироваться с глюкуроновой кислотой (УДФГК), при этом образуется МОНОДИБИЛЛИРУБИНГЛЮКУРОНИД. Глюкуроновая кислота присоединяется к СООН-группе остатков пропионовой кислоты. ГЛЮКУРОНИДЫ это уже обезвреженные формы биллирубина. Их называют КОНЪЮГИРОВАННЫМ БИЛЛИРУБИНОМ (КБ). Ранее его называли прямым биллирубином, т.к. он открывается прямой реакцией с ДИАЗО -реактивом ЭРЛИХА. Он имеет свойства: нетоксичен, гидрофилен, способен фильтроваться почками, дает прямую реакцию с реактивом ЭРЛИХА. КБ выделяется из печени в составе желчи в кишечник, где под влиянием ферментов слизистой оболочки кишечника и кишечной микрофлоры гидролитически распадается. Глюкуроновая кислота всасывается в кровь и через систему портальной вены поступает в печень, где снова принимает участие в интоксикации веществ. БИЛЛИРУБИН восстанавливается по некоторым двойным связям, превращаясь в МЕЗОБИЛЛИНОГЕН. Он частично в тонком отделе кишечника может всасываться в кровь и через портальную вену поступать в печень, где частично распадается с образованием моно-, ди-, трипирролов, которые выделяются почками в составе мочи. Незначительная часть МЕЗОБИЛИНОГЕНА, минуя печень, поступает в почки и выделяется в виде УРОБИЛИНОГЕНА. При суточном диурезе в норме 1,2 - 1,5л с мочой взрослого человека выделяется 1 - 4мг уробилиногена, который на свету превращается в уробилин. Основная часть мезобилиногена, продвигаясь с пищевым комком в толстый отдел кишечника под влиянием ферментов кишечной микрофлоры восстанавливаясь, превращается в СТЕРКОБИЛИНОГЕН - основной пигмент кала, который, выделяясь из организма, на свету превращается в стеркобилин. Было установлено, что за сутки с калом взрослого человека выделяется 240 - 300мг стеркобилина. Небольшая часть стеркобилиногена в толстом отделах кишечника в области геморроидальных вен, всасываясь в кровь, минуя печень, поступает в почки, где фильтруется и выделяется в составе мочи.
Т.о. основными компонентами доступных для исследования биологических сред являются:
1. Для крови: НБ - 75%, КБ - 25%. Суммарно этот показатель обозначается, как общий билирубин КРОВИ, который в норме для взрослого человека составляет 8 -20ммоль/л.
2. Для желчи - КБ.
3. Для мочи: УРОБИЛИНОГЕН (1 -4мг/сутки), СТЕРКОБИЛИН.
4. Для кала: СТЕРКОБИЛИНОГЕН (240 - 300мг/сутки).
ПАТОЛОГИЯ ПИГМЕНТНОГО ОБМЕНА.
Может наблюдаться при усиленном распаде эритроцитов, при нарушении функции печени и ЖВП. В результате этих нарушений у больных кожа и видимые слизистые оболочки окрашиваются в желтый цвет. Желтушность становится заметной если уровень общего билирубина в крови повышается в 2 -3 раза. Для проведения дифференциальной диагностики желтух необходимо исследовать кровь, мочу и кал на содержание в них желчных пигментов. Различают:
