
- •Федеральное агентство по образованию
- •Новгородский государственный университет
- •Квантовая оптика Сборник лабораторных работ по общему курсу физики
- •Содержание
- •Предисловие
- •1 Лабораторная работа № 4.8. Исследование вакуумного и газонаполненного фотоэлементов
- •Основные понятия и законы
- •1.2 Характеристики фотоэлементов с внешним фотоэлементом
- •1.3 Установки для исследования вакуумного и газонаполненного фотоэлементов
- •1.4 Порядок выполнения работы
- •1.5 Техника безопасности
- •1.6 Вопросы для самоподготовки
- •2. Лабораторная работа № 4.16. Исследование внутреннего фотоэффекта
- •2.1 Внутренний фотоэффект
- •2.2. Вентильный фотоэффект
- •2.3 Фотоэлементы и их характеристики
- •2.4 Описание экспериментальной установки и порядок выполнения работы
- •2.5 Техника безопасности
- •2.6 Вопросы для самоподготовки
- •3 Лабораторная работа № 4.13. Определение красной границы фотоэффекта и работы выхода электрона
- •3.1 Устройство и принцип работы монохроматора
- •3.2 Градуировка монохроматора
- •3.3 Исследование зависимости фототока от длины волны
- •4 Лабораторная работа № 4.9. Определение суммарного коэффициента поглощения тела оптическим пирометром
- •4.2.2 Законы теплового излучения
- •4.3 Методика исследования
- •4.3.1 Определение суммарного коэффициента поглощения
- •4.3.2 Измерение истинной температуры нити лампы накаливания
- •4.3.3 Электрическая схема установки
- •4.4 Порядок выполнения работы
- •5.2 Описание установки
- •5.3 Порядок выполнения работы
- •6.2 Описание установки 1
- •6.3 Порядок выполнения работы на первой установке
- •6.4 Электрическая схема второй измерительной установки и принцип ее работы
- •6.5 Порядок выполнения работы на второй установке
- •6.6 Техника безопасности
- •6.7 Вопросы для самоподготовки
- •7 Лабораторная работа №4.20. Исследование видимого спектра излучения атома водорода
- •Основные понятия и закономерности
- •7.2 Порядок выполнения работы
- •7.3 Контрольные вопросы
- •7.4 Техника безопасности
- •Библиография
- •Квантовая оптика
- •173003 В. Новгород, ул. Б. Санкт – Петербургская , 41
- •173003 В. Новгород, ул. Б. Санкт – Петербургская, 41
5.2 Описание установки
Для исследования спектра испускания водорода применяется гониометр типа Федорова. Этот гониометр представляет собой двухтрубный спектроскоп, принципиальная схема которого приведена на рисунке 5.3.
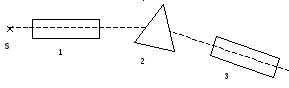
S – источник света; 1 – коллиматор; 2 – призма трехгранная;
3 – зрительная труба
Рисунок 5.3 – Принципиальная схема гониометра
Коллиматор – это труба со щелью на одном конце, ширину которой можно менять регулировочным винтом. На другом конце коллиматора расположена ахроматическая собирающая линза. Коллиматор создает параллельный пучок лучей, падающих на призму. Зрительная труба имеет объектив и окуляр, при помощи которого рассматривается спектр исследуемого вещества. Призма обладает относительно большой дисперсией, поэтому весь спектр одновременно в поле зрения не виден. Для определения длин волн, излучаемых исследуемым веществом, необходимо знать дисперсионную кривую прибора, т.е. графическую зависимость углового расположения спектральных линий в поле зрения окуляра от длины волны. Строится дисперсионная кривая при помощи линейчатых спектров элементов, длины волн которых известны (например, ртуть, гелий). По дисперсионной кривой можно определить длины волн всех спектральных линий водорода.
5.3 Порядок выполнения работы
-
Градуировка шкалы спектрометра.
-
Расположить гониометр перед окном ртутной лампы.
-
Включить вентилятор.
-
Включить ртутную лампу.
-
Добиться наибольшей четкости линий спектра ртути, уменьшая размер входной щели коллиматора.
-
Записать деления шкалы гониометра α, соответствующие наиболее ярким линиям спектра ртути (таблица 5.1).
-
На миллиметровой бумаге построить градуировочную кривую прибора
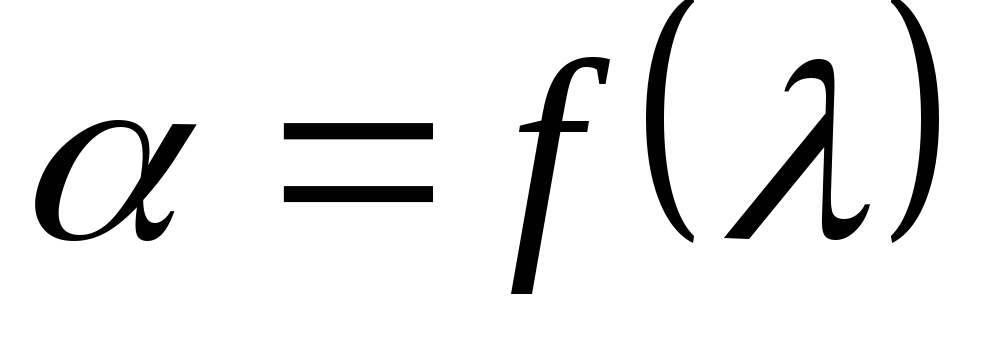 по табличным данным.
по табличным данным.
Таблица 5.1
|
λ, нм |
|
|
|
|
|
|
|
|
|
α, град |
|
|
|
|
|
|
|
|
-
Определение длин волн серии Бальмера и постоянной Ридберга.
-
Переставить гониометр к водородной трубке.
-
Включить водородную трубку.
-
Не изменяя положения зрительной трубы и коллиматора относительно призмы, добиться наблюдения линий серии Бальмера.
-
Записать показания шкалы гониометра, соответствующие видимым линиям спектра водорода (таблица 5.2).
Таблица 5.2
|
Линия |
Красная |
Зелено-голубая |
Синяя |
Фиолетовая |
|
n |
3 |
4 |
5 |
6 |
|
α, град |
|
|
|
|
|
λ, нм |
|
|
|
|
|
R, м-1 |
|
|
|
|
-
Определить длины волн спектральных линий водорода, пользуясь градуировочной кривой.
-
Произвести расчет постоянной Ридберга, используя формулу:
![]()
-
Найти среднее значение постоянной Ридберга.
-
Сравнить полученное значение с теоретическим.
-
Оценить погрешность результата.
5.4 Контрольные вопросы
-
Опишите модель атома по Резерфорду-Бору.
-
Сформулируйте постулаты Бора.
-
Выведите формулу для расчета энергии атома водорода.
-
Получите сериальную формулу Бальмера.
-
Каков физический смысл и числовое значение постоянной Ридберга?
-
Опишите процессы излучения и поглощения атома.
5.5 Техника безопасности
-
Без разрешения преподавателя или лаборанта установку не включать.
-
Избегать прямого попадания излучения ртутной лампы в глаза.
-
В установке используется напряжение 220 в, опасное для жизни. При включении соблюдать меры электробезопасности в соответствии с инструкцией для лаборатории оптики.
6 Лабораторная работа № 4.12. ИЗУЧЕНИЕ ОПЫТА ФРАНКА – ГЕРЦА
Цель работы: Целью работы является определение потенциала возбуждения атома ртути или другого исследуемого газа по вольт-амперным характеристикам.
6.1 Основные сведения
Немецкие физики Д. Франк и Г. Герц, изучая столкновение электронов с атомами методом задерживающего потенциала, экспериментально доказали дискретность энергий атомов, подтвердив постулаты Бора (см. раздел 5.2 данного пособия).
Опыты Франка и Герца заключались в следующем. Атомы газа, находящиеся в некотором сосуде, облучаются пучком сравнительно медленных электронов, ускоренных электрическим полем и получившим энергию:
![]() ,
(6.1)
,
(6.1)
где U – разность потенциалов, которую прошли электроны до взаимодействия с атомами.
Электроны сталкиваются с атомами газа и испытывают столкновения двух видов – упругие и неупругие.
При упругих столкновениях скорость электрона, взаимодействующего с атомом, практически не изменяется по величине, изменяется только ее направление. В этом случае электрон не передает энергию атому, так как его масса значительно меньше массы атома.
При неупругих столкновениях он передает атому почти всю свою энергию. Но в соответствии с постулатом Бора атом не может принять энергию в любом количестве. Атом принимает лишь определенную порцию энергии и при этом переходит в другое стационарное энергетическое состояние, которое называют возбужденным.
Если энергия электронов, бомбардирующих атом, меньше энергии, необходимой для возбуждения атома (энергии возбуждения), электроны испытывают только упругие столкновения. Как только энергия электронов станет равной энергии возбуждения, столкновения могут быть неупругими.
Если до неупругого соударения атом находился в основном (невозбужденном) состоянии с энергией W0 , то после него он переходит в первое возбужденное состояние с энергией W1 . Из этого состояния атом, спустя небольшой промежуток времени переходит в основное состояние, испуская фотон с энергией ħω1 , в точности совпадающей с энергией eU1 . которой обладает электрон перед неупругим столкновением с атомом. Разность потенциалов U1 . равная отношению энергии W1 – W0 . которую необходимо сообщить атому для перехода в первое возбужденное состояние, к заряду электрона, называется первым потенциалом возбуждения:
![]() .
(6.2)
.
(6.2)
Если электрону до столкновения сообщить достаточно большую энергию, он при неупругих столкновениях может перевести атом во второе, третье и более высокое возбужденное состояние с энергиями, соответствующими более высоким энергетическим уровням атома.
Для доказательства существования стационарных энергетических состояний атома, соответствующих дискретному ряду значений энергии, необходимо опытным путем установить, что неупругие столкновения электронов с атомами происходят только при строго определенных значениях кинетической энергии электронов.
Э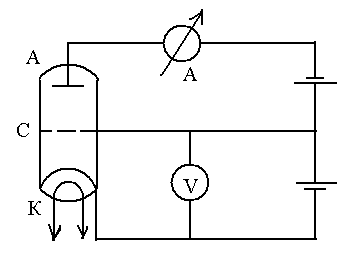 лектрическая
схема установки, использованной в опытах
Франка и Герца, представлена на рисунке
6.1.
лектрическая
схема установки, использованной в опытах
Франка и Герца, представлена на рисунке
6.1.
Рисунок 6.1. Электрическая схема опыта Франка и Герца
Между сеткой и катодом триода, наполненного парами ртути при давлении 10 мм Hg, подается ускоряющее напряжение Uкс , а между анодом и сеткой – тормозящее, то есть потенциал анода несколько ниже потенциала сетки. Исследуется зависимость тока Ia , протекающего через триод, от разности потенциалов между катодом и сеткой Uкс .
В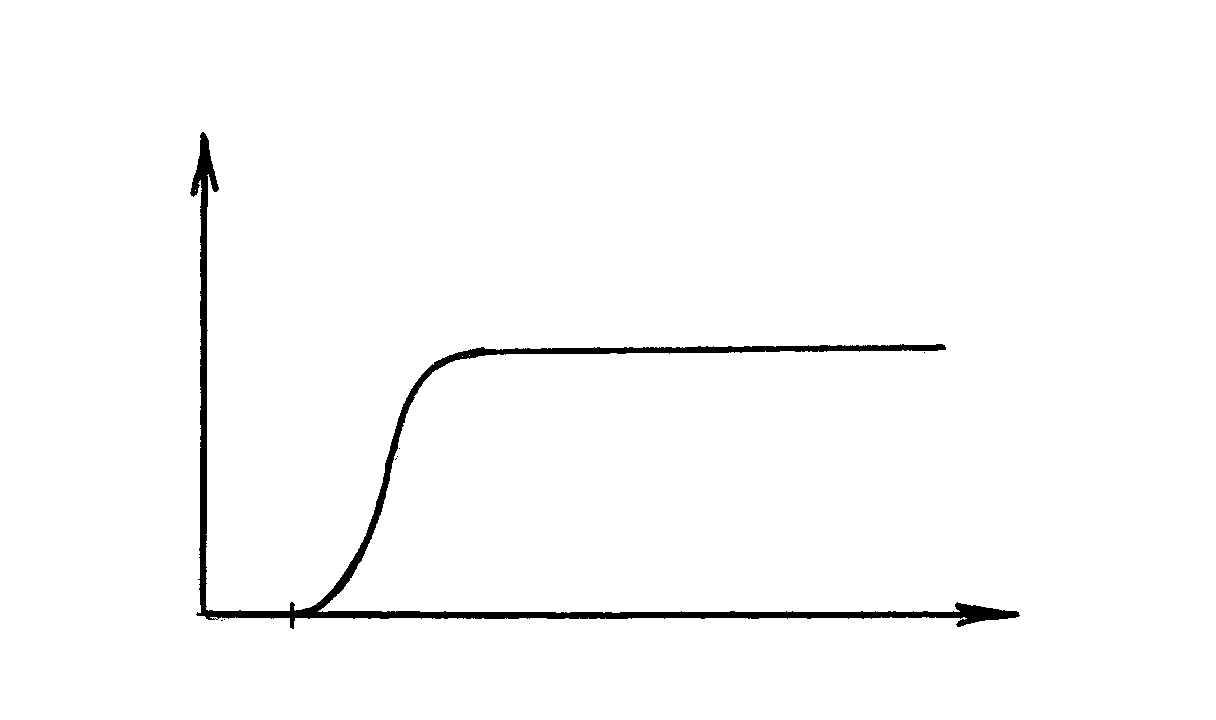 случае высокого вакуума анодный ток в
лампе создается электронами, вылетающими
из катода вследствие термоэлектронной
эмиссии. Зависимость анодного тока Ia
от ускоряющего напряжения Uкс
в этом случае имеет вид, представленный
на рисунке 6.2.
случае высокого вакуума анодный ток в
лампе создается электронами, вылетающими
из катода вследствие термоэлектронной
эмиссии. Зависимость анодного тока Ia
от ускоряющего напряжения Uкс
в этом случае имеет вид, представленный
на рисунке 6.2.
![]()
![]()
![]()
Рисунок 6.2. График зависимости анодного тока
от напряжения в вакууме
Ток равен нулю, пока U ≤ U1 ., где U1 – напряжение между сеткой и анодом – напряжение задержки: так как при этом на один медленный электрон не проходит тормозящее поле.
При U > U1 ток растет и при некотором значении ускоряющего напряжения, когда все электроны, вылетевшие с катода за единицу времени достигают анода, перестает расти – достигает насыщения.
В случае же наличия в лампе паров ртути характеристика имеет другой вид (рисунок 6.3), при некоторых напряжениях появляются максимумы. Первый максимум соответствует ускоряющему напряжению 4,9 В, второй – 9,8В, третий – 14,7 В.
Объяснить такую зависимость анодного тока от напряжения между катодом и сеткой можно следующим образом.
П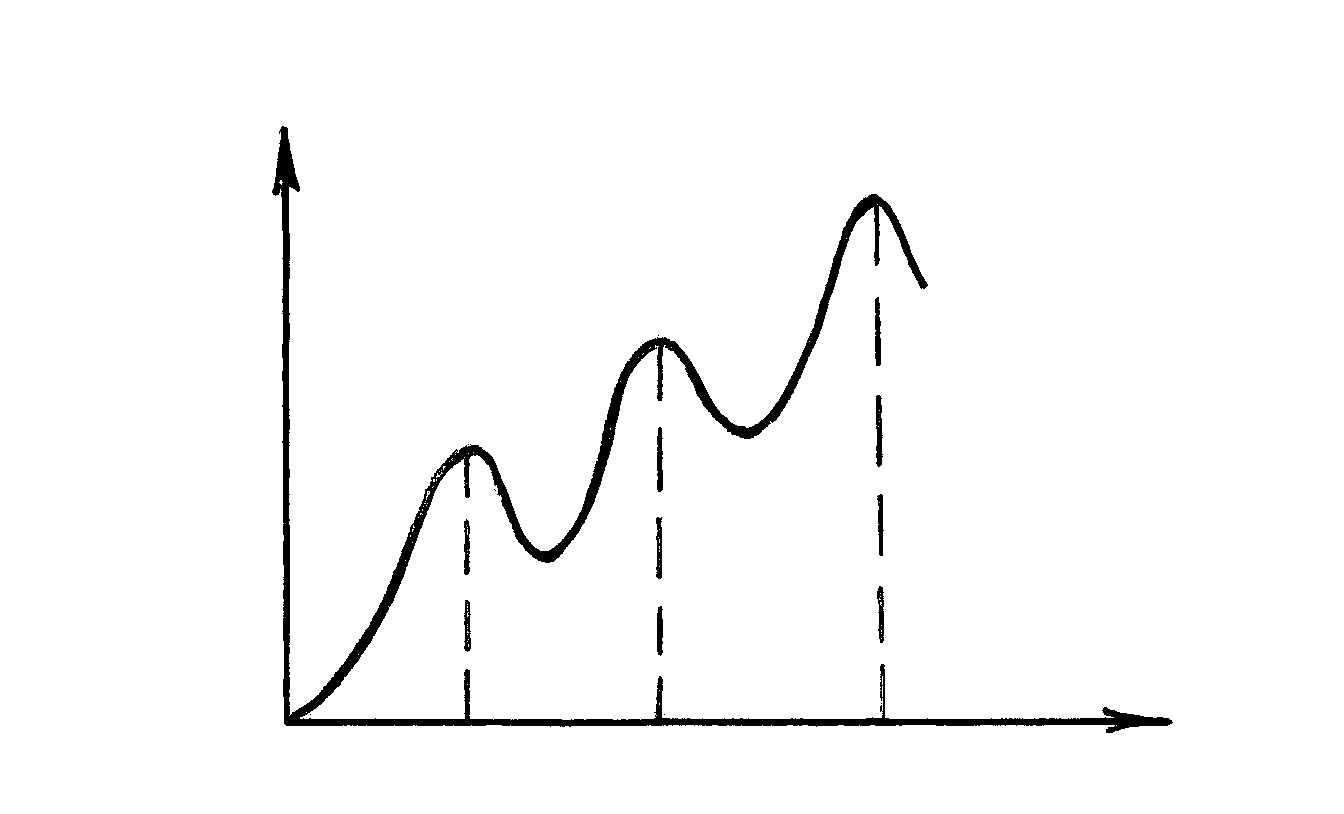 учок
электронов, обстреливающий атомы ртути
в лампе, образуется электронами,
вылетающими из катода в результате
термоэлектронной эмиссии. Если энергии
электронов меньше энергии возбуждения,
они испытывают упругие столкновения с
атомами ртути, а поэтому их энергия
после столкновения остается неизменной,
равной у сетки примерно eUкс
.
учок
электронов, обстреливающий атомы ртути
в лампе, образуется электронами,
вылетающими из катода в результате
термоэлектронной эмиссии. Если энергии
электронов меньше энергии возбуждения,
они испытывают упругие столкновения с
атомами ртути, а поэтому их энергия
после столкновения остается неизменной,
равной у сетки примерно eUкс
.
![]()
![]()
Рисунок 6.3. График зависимости анодного тока
от напряжения при заполнении лампы парами ртути
Как только энергия электрона станет равной энергии возбуждения, он испытывает неупругое столкновение с атомом ртути, в результате которого уменьшается его кинетическая энергия, он не сможет преодолеть задерживающее поле между сеткой и анодом, на анод не попадает, так как это поле возвратит его на сетку. В результате этот электрон не вносит вклад в анодный ток. Но так как неупругие столкновения начинают происходить только при получении электронами критической энергии, равной энергии первого возбуждения W1 – W0 , уменьшение числа электронов, попадающих на анод начнется с того момента, когда потенциал на сетке станет равным или больше первого потенциала возбуждения (для ртути 4,9 В). При этом анодный ток не падает до нуля, так как в объеме газа в этот момент существуют электроны, которые не испытали неупругого столкновения, и поэтому они могут преодолеть задерживающее поле и попасть на анод. Если потенциал на сетке увеличивать, то электрон может после первого неупругого столкновения с одним атомом ртути испытать второе, третье и т. д. неупругие столкновения с другими атомами ртути. Для ртути это происходит при потенциалах 9,8 В: 14,7 В (см. рисунок 6.3).
В данном опыте было обнаружено излучение света с λ = 2536 Ǻ (ультрафиолетовая часть спектра), которое начинается с того момента, как только потенциал на сетке станет равным 4,86 В. Этот факт находит объяснение только с позиции квантовой теории. При неупругом соударении с электроном атом ртути получает энергию, необходимую для перехода в первое возбужденное состояние, то есть состояние с энергией W1 . Через некоторое время (~ 10-8 с) атом переходит в основное состояние с энергией W0 , излучая избыток энергии в виде кванта света:
![]() .
.
Таким образом, Франк и Герц своими опытами подтвердили справедливость первого и третьего постулатов Бора, а также определили порцию энергии, принимаемой и отдаваемой атомом ртути:
![]() .
(6.3)
.
(6.3)
