
- •Тема 1.1. Основні закони хімії
- •Закон збереження маси речовини
- •Контрольні запитання:
- •Тема 1.2. Оксиди
- •Визначення. Класифікація оксидів.
- •Контрольні запитання:
- •Тема 1.3. Основи
- •Визначення. Класифікація основ.
- •Контрольні запитання:
- •Тема 1.4. Кислоти
- •Визначення. Класифікація кислот.
- •Контрольні запитання:
- •Тема 1.5. Солі
- •Визначення. Класифікація солей.
- •Контрольні запитання:
- •Тема 1.6. Хімічний зв'язок
- •Поняття про хімічний зв'язок. Типи хімічного зв’язку.
- •Контрольні запитання:
- •Тема 1.7. Електролітична дисоціація. Реакції йонного обміну
- •Контрольні запитання:
- •Тема 1.8. Окисно-відновні реакції
- •Контрольні запитання:
- •Тема 2.1. Загальна характеристика металів
- •Контрольні запитання:
- •Тема 2.2. Корозія металів
- •Корозія металів. Види корозії.
- •Контрольні запитання:
- •Тема 2.3. Лужні метали
- •Контрольні запитання:
- •Тема 2.4. Кальцій
- •Кальцій.**
- •Контрольні запитання:
- •Тема 2.5. Сполуки Кальцію
- •Контрольні запитання:
- •Тема 2.6. Алюміній
- •Контрольні запитання:
- •Тема 2.7. Залізо
- •Контрольні запитання:
- •Тема 2.8. Сульфур. Сірка.
- •Контрольні запитання:
- •Тема 2.9. Сполуки Сульфуру
- •Контрольні запитання:
- •Тема 2.10. Сульфатна кислота та її солі
- •Контрольні запитання:
- •Тема 2.11. Нітроген. Азот.
- •Контрольні запитання:
- •Тема 2.12. Аміак. Солі амонію.
- •Контрольні запитання:
- •Тема 2.13. Сполуки Нітрогену
- •Контрольні запитання:
- •Тема 2. 14.Фосфор
- •Фосфор.
- •Контрольні запитання:
- •Тема 2.15. Сполуки Фосфору
- •Контрольні запитання:
- •Тема 2.16. Карбон. Вуглець.
- •Контрольні запитання:
- •Тема 2.16. Сполуки Карбону
- •Контрольні запитання:
- •Тема 2.18. Силіцій.
- •Контрольні запитання:
- •Тема 2.19. Сполуки Силіцію.
- •Контрольні запитання:
- •Тема 3.1. Теорія будови органічних речовин о.М. Бутлерова
- •Контрольні запитання:
- •Тема 3.2. Алкани
- •Контрольні запитання:
- •Тема 3.3. Алкени
- •Контрольні запитання:
- •Тема 3.4. Алкіни
- •Контрольні запитання:
- •Тема 3.5. Алкадієни (дієнові вуглеводні)
- •Контрольні запитання:
- •Тема 3.6. Ароматичні вуглеводні (арени)
- •Контрольні запитання:
- •Тема 3.7. Природні джерела вуглеводнів
- •Контрольні запитання:
- •Тема 4.1. Одноатомні спирти
- •Контрольні запитання:
- •Тема 4.2. Багатоатомні спирти
- •Контрольні запитання:
- •Тема 4.3. Феноли
- •Контрольні запитання:
- •Тема 4.4. Альдегіди
- •Контрольні запитання:
- •Тема 4.5. Карбонові кислоти
- •Контрольні запитання:
- •Тема 4.6. Естери
- •2. Номенклатура:
- •Контрольні запитання:
- •Тема 4.7. Жири. Мило
- •Контрольні запитання:
- •Тема 5.1. Вуглеводи. Глюкоза
- •Контрольні запитання:
- •Тема 5.2. Сахароза
- •Контрольні запитання:
- •Тема 5.3. Крохмаль і целюлоза
- •Контрольні запитання:
- •Тема 5.4. Аміни
- •Контрольні запитання:
- •Тема 5.5. Амінокислоти
- •Контрольні запитання:
- •Тема 5.6. Білки
- •Контрольні запитання:
Контрольні запитання:
-
Які ступені окиснення характерні для Сульфуру?
-
Які фізичні і хімічні властивості характерні для сірководню?
-
Які оксиди утворює Сульфур? Охарактеризуйте їх.
-
Як в промисловості добувають сірководень, оксиди Сульфуру?Напишить рівняння відповідних реакцій.
-
Де використовуються сірководень, оксиди Сульфуру?
-
Яка сіль і якої масу утворюється при додаванні 4г натрій гідроксиду до розчину сульфатної кислоти масою 98г з масовою часткою кислоти 10%.
Література:
-
Данильченко В.Є., Фрадіна Н.В. Хімія. 10 – 11 класи: Навч. посібник. – Х.: Країна мрій™, 2003. - с. 6.
-
Хомченко Г.П. Химия. – М.: Высшая школа, 1981. – Ч. ІІ, Гл. 9, §§ 75-76, с. 89-91.
-
Стахеєв О.Ю. Хімія. Узагальнюючі схеми і таблиці. – Тернопіль.: «Богдан», 1998. – с. 25.
Тема 2.10. Сульфатна кислота та її солі
План
-
Сульфатна кислота.**
-
Контактний спосіб добування сульфатної кислоти.**
-
Сульфати.*
1![]() .
Молекулярна формула
- H2SO4
.
Молекулярна формула
- H2SO4
Структурна формула
Фізичні властивості: безводна сульфатна кислота – важка, безбарвна, оліїста рідина. Густина її концентрованого розчину (w(H2SO4) = 98%) за стандартних умов 1,84 г/см3. Вона нелетка, запаху не має. Надзвичайно гігроскопічна, активно вбирає вологу. Змішується з водою у будь-яких співвідношеннях. Розчинення сульфатної кислоти у воді супроводжується виділенням великої кількості теплоти. Сульфатна кислота – їдка рідина, роз’їдає папір, шкіру, тканини тощо.
Хімічні властивості багато в чому залежать від її концентрації.
Розбавлена сульфатна кислота виявляє всі хімічні властивості, характерні для кислот:
1) змінює колір індикатора – лакмус стає червоним, метиловий оранжевий – рожевим, фенолфталеїн залишається безбарвним;
2) як сильна двохосновна кислота у водному розчині повністю дисоціює на йони (ступінчасто):
![]()
тому здатна утворювати два ряди солей: середні солі – сульфати і кислі солі – гідрогенсульфати;
3) взаємодіє з основами:
Реакції між основами і кислотами, внаслідок яких утворюються сіль і вода, називаються реакціями нейтралізації. Вони належать до реакцій обміну.
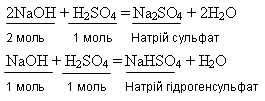
4) взаємодіє з оксидами металів:

5) взаємодіє із солями. Як сильна, нелетка і найстійкіша з відомих мінеральних кислот, вона здатна витісняти із солей слабкіші, або леткі, або навіть сильні кислоти, якщо вони менш стійкі:

Останнє рівняння відображує якісну реакцію на сульфатну кислоту та її солі.
6) взаємодіє з металами, що стоять у ряду активності металів лівіше водню:

Малоактивні метали (мідь, срібло, золото) з розбавленою сульфатною кислотою не реагують.
Концентрована сульфатна кислота – сильний окисник:
1) взаємодіє з малоактивними металами (крім золота та платини) з виділенням сульфур(IV) оксиду:

2) взаємодіє з активними металами з виділенням H2S і SO2 :
![]()
Із залізом, кобальтом, нікелем 100% сульфатна кислота не реагую, реагує тільки 70%:
![]()
3) взаємодіє з неметалами (P, C, S):

Застосування. Сульфатну кислоту застосовують для:
1) добування мінеральних добрив (суперфосфату, амоній сульфату);
2) виробництва купоросів (залізного, мідного);
3) одержання барвників, пластмас, штучного волокна, лікарських і вибухових речовин, летких кислот;
4) сушіння різних речовин (як водовідбираючий засіб), очищення нафтопродуктів та поверхонь металів від оксидів.
2. Найсучасніший спосіб добування сульфатної кислоти – це контактний. Як сировина використовується пірит, або залізний колчедан.
Він складається з таких стадій:
Перша стадія – випалювання колчедану і добування сульфур (IV) оксиду:
4FeS2 + 11O2 = 2Fe2O3 + 8SO2; ∆H = -13476 кДж
Процес відбувається у колчеданних печах, з яких виходить випалювальний газ. Він містить, крім SO2, різні домішки. Його очищують, висушують і подають у контактний апарат.
Друга стадія – окиснення сульфур (IV) оксиду і добування сульфур (VІ) оксиду:
![]()
Окиснення відбувається в контактному апараті за наявності каталізатора і високої температури, незважаючи на те, що реакція екзотермічна. Це пояснюється тим, що каталізатор стає активним лише при температурі 450ºC. Теплоту відводять і використовують для нагрівання випалювального газу, який в очисних спорудах встигає охолонути.
Третя стадія – поглинання сульфур (VІ) оксиду й утворення сульфатної кислоти.
В абсорбері сульфур (VІ) оксид поглинається концентрованою сульфатною кислотою (w(H2SO4) = 96-98%). Тут він взаємодіє з водою, що є в концентрованій сульфатній кислоті, утворюючи безводну, 100%-ву сульфатну кислоту – моногідрат:
![]()
Чистою водою поглинати сульфур (VІ) оксид не можна, бо утворюється стійкий „туман” із дрібних крапель сульфатної кислоти, який майже не конденсується.
Кінцевий продукт виробництва – олеум, тобто розчин сульфур (VІ) оксиду в моногідраті. Його розбавляють водою до потрібної концентрації.
3. Більшість солей сульфатної кислоти легко розчиняються у воді. Малорозчинними є плюмбум сульфат і кальцій сульфат, практично нерозчинними у воді та кислотах є барій сульфат і стронцій сульфат.
Якісна реакція на розчинні сульфати – взаємодія з розчинними солями Барію - BaCl2, Ba(NO3)2

Багато солей сульфатної кислоти кристалізуються із розчинів у вигляді кристалогідратів, які називаються купоросами.
Купороси – технічна назва кристалогідратів сульфатів деяких важких металів, тобто солей сульфатної кислоти, які містять кристалізаційну воду. В основному це солі Купруму, Феруму, Ніколу, Кобальту і Цинку:

Гіпс CaSO4 · 2H2O до купоросів не належить, оскільки Кальцій не є важким металом.
Гіпс CaSO4 · 2H2O так само, як і безводний кальцій сульфат CaSO4 використовують у будівництві, в медицині тощо.
Натрій сульфат Na2SO4 – у виробництві скла, а його кристалогідрат Na2SO4·10H2O – глауберову сіль використовують як проносний засіб у медицині.
Калій сульфат К2SO4 та амоній сульфат (NН4)2SO4 служать добривами.
Барій сульфат BaSO4 застосовують у виробництві паперу, гуми та білої мінеральної фарби, а також у медицині для рентгеноскопії шлунку („Барієва каша”).
