ФБТ БИ 1курс / 8хим
.docx|
Лабораторна робота 8 ДИСОЦІАЦІЯ ВОДИ, рН, ГІДРОЛІЗ СОЛЕЙ Мета роботи: навчитися оцінювати рН розчину за допомогою індикаторів та вимірювати за допомогою рН-метра, експериментально вивчити процеси гідролізу різних типів солей. Теоретичні відомості Дисоціація води. Іонний добуток води. Водневий показник (рН) та його значения в нейтральному, кислому та лужному середовищах. Гідроліз солей. Ступінь гідролізу. Порядок виконання лабораторної роботи
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Зм |
Арк. |
№ докум. |
Підпис |
Дата |
||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Розробив |
|
|
|
|
Літера |
Аркуш |
Аркушів |
|||||||||||||||||||||||||||||||||||||||||||||||||||
|
Перевірив |
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||
|
Т. Контр. |
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Н. Контр. |
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Затверд. |
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||
-
 Вплив
температури на ступінь гідролізу.
Розчиніть у 2 - 3 мл води трохи кристалів
ацетату натрію, додайте 2 - 3 краплі
фенофталеїну. Підігрійте одержаний
розчин. Що спостерігається? Поясніть
те, що спостерігається, навівши рівняння
реакції гідролізу в іонній та молекулярній
формах.
Вплив
температури на ступінь гідролізу.
Розчиніть у 2 - 3 мл води трохи кристалів
ацетату натрію, додайте 2 - 3 краплі
фенофталеїну. Підігрійте одержаний
розчин. Що спостерігається? Поясніть
те, що спостерігається, навівши рівняння
реакції гідролізу в іонній та молекулярній
формах.
Спостереження та досліди
Індикатори
Нейтральне:
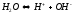
Кисле:
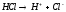
Лужне:
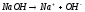
Метилоранж – індикатор на кисле середовище, набуває червоного кольору.
Фенолфталеїн – індикатор на лужне середовище, малиновий.
Лакмус – універсальний індикатор, але дорогий.
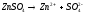 - гідроліз за катіоном.
Zn(OH)2
(слабка) H2SO4
(сильна)
- гідроліз за катіоном.
Zn(OH)2
(слабка) H2SO4
(сильна)
-
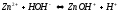 ,
pH<7, кисле
,
pH<7, кисле
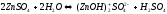

Сіль утворена слабкою основою та сильною кислотою, середовище кисле.
Гідроліз солей
-
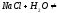 реакція
не відбувається.
реакція
не відбувається.
NaCl – сіль утворена сильною основою та сильною кислотою.
-
 -
гідроліз за аніоном; NaOH
– сильний, І стадія; H2CO3
– слабка;
-
гідроліз за аніоном; NaOH
– сильний, І стадія; H2CO3
– слабка;
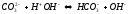 ,
pH>7, середовище лужне.
,
pH>7, середовище лужне. -
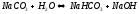
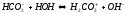
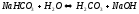
Сіль утворена сильною основою та слабкою кислотою, середовище лужне.
Вплив температури на ступінь гідролізу
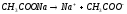 -
гідроліз за аніоном.
-
гідроліз за аніоном.
CH3COOH (слабка) NaOH(сильна)
І.
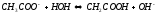 -
середовище лужне
-
середовище лужне
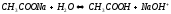 -
гідроліз ендотермічний
-
гідроліз ендотермічний
При підвищенні температури гідроліз посилюється, ступінь гідролізу β збільшується, рівновага зміщується до ОН-. Середовище
 стає
більш лужним.
стає
більш лужним.
Розчин солі ацетату натрію V
Додали індикатор, далі підігріваємо, оскільки гідроліз – ендотермічний процес за принципом Ле Шательє, при підвищенні температури зростає концентрація йонів. Індикатор набуває більш яскравого малинового забарвлення.
Висновок: ми вивчили реакції гідролізу різних типів солей.