
- •1. Нефтегазоносность Ближнего и Среднего Востока. Уникальные месторождения.
- •2.Формирование подземных вод осадочных бассейнов.
- •3. Методы подсчёта запасов газа.
- •Формула подсчета запасов растворенного газа(водонапорнвй режим)
- •4. Формы изображения химического состава вод, правила их химического наименования. Химическая классификация вод.
- •Химическая классификация вод Типы подземных вод в осадочных бассеинах по Зайцеву
- •Типы вод по Сулину
- •5. Проницаемость и пористость горных пород. Закон Дарси.
- •Пористость.
- •Закон Дарси
- •6.Структурно-картированное бурение (цели, задачи, технология).
- •7.Компонентный состав свободных и попутных газов.
- •8.Сибирская Платформа. Основные Черты Геологического Строения и Перспективы Нефтегазоносности.
- •Границы платформы
- •В строении платформы выделяются:
- •Выделяются следующие тектонические провинции:
- •9. Методика построения структурных карт.
- •10. Гидрогеологические критерии нефтегазоносности
- •Главнейших гидрогеологические показатели:
- •11. Сейсморазведка. Основные методы и их физическая сущность.
- •Основные методы
- •1. Метод отраженных волн
- •2. Метод преломленных волн
- •12. Построение профильных геологических разрезов глубокозалегающих пластов по скважинам.
- •3 Метода исследования разреза по скважине:
- •13. Зоны нефтегазонакопления и нефтегазообразования. Критерии их выделения. Примеры таких зон.
- •Структурный тип зон нефтегазоскоплений:
- •14. Наиболее распространённые осадочные породы, их происхождение, ёмкостно-фильтрационные свойства.
- •15. Природоохранные мероприятия при геолого-разведочных работах на нефть и газ.
- •1) Мероприятия по охране природной среды на поисково-разведочной стадии:
- •2) Природоохранные мероприятия при строительстве и эксплуатации скважин
- •16. Этапы и стадии поисково-разведочного процесса. Их характеристика.
- •Характеристика стадий Региональный этап
- •Поисковый этап
- •Разведочный этап
- •17. Методы определения пластовых и забойных давлений. Карты приведённых давлений.
- •18. Битумы и битумоиды. Их состав, генезис и принципиальные различия.
- •19. Элементный и компонентный состав нефти. Элементный состав нефти
- •Компонентный состав нефти
- •20. Методы испытания скважин.
- •21. Геологическая документация при разведке нефтяных и газовых месторождений c использованием буровых работ.
- •22. Шкала катагенеза органического вещества осадочных пород.
- •23. Виды режимов пластов. Условия проявления различных режимов. Особенности режимов газовых пластов.
- •24. Гравиразведка. Методика исследований при поисках нефти и газа.
- •25. Углеводородный состав нефти.
- •26. Структурно-тектонические месторождения платформ. Принципы систематики. Характерные типы залежи.
- •2. Месторождения, связанные с эрозионными и рифовыми массивами
- •3. Месторождения, связанные с гомоклиналями
- •4. Месторождения, связанные с синклинальными прогибами
- •27. Методика и стадийность геохимических поисков нефтегазовых месторождений.
- •1) Газовый
- •28. Горючие полезные ископаемые. Основные группы, представления об условиях образования.
- •30. Пробная эксплуатация нефтяных и газовых залежей.
- •Методы воздействия на пласт.
- •31. Принципы классификации и типы нгб.
- •Бассеины на стыке складчатых областей и платформ
- •32. Геологическое строение и нефтегазоносность Западно-Сибирской нгп. Её роль в нефтегазовом потенциале России.
- •33. Принципы классификации месторождений нефти и газа.
- •Современная классификация месторождений по Токаревой
- •Альтернативные классификации месторождений
- •34. Виды геофизических исследования в скважинах.
- •Краткий перечень методов каротажа. Электрический каротаж:
- •Радиоактивные методы:
- •1) Газовый
- •36. Основные нефтегазоносные комплексы и горизонты Восточной Сибири.
- •37. Характеристика зон внк, гвк, гнк. Методы нахождения их поверхностей.Теоретическое обоснование геохимических методов поисков нефти и газа.
- •Теоретическое обоснование геохимических методов поисков нефти и газа.
- •38. Обзор основных нефтегазоносных бассейнов Северной Америки.
- •39. Гидрогеологический цикл и его этапы. Роль этапов в формировании залежей нефти и газа.
- •40. Подготовка скважин к опробованию и его производство.
- •41. Обзор ведущих нефтегазоносных бассейнов Европы.
- •1) Среднеевропейской и Восточно-Европейской древних платформ
- •2) Западно-Европейской молодой платформы:
- •3) Предгорных прогибов альпийских горноскладчатых сооружений Южной Европы;
- •4) Межгорных впадин альпийской складчатости Южной Европы и Средиземноморья
- •42. Электроразведка. Физическая сущность и основные методы. Возможности применения метода.
- •Электрокаротаж (скважинная электроразведка)
- •43. Основные обстановки осадконакопления. Условия накопления и сохранения органического вещества.
- •3. Нивальный (ледниковый. Образуются Морены в результате схода ледников.
- •4. Вулканогенно-осадочный
- •44. Типы нгб, особенности их строения и характеристика условий генерации нефти и газа, аккумуляция и сохранность залежей.
- •Бассеины на стыке складчатых областей и платформ
- •Формирование проходит в несколько стадий:
- •Условия сохранения:
- •45. Радиометрия. Сущность метода и основные модификации. Принцип устройства аппаратуры и круг решаемых задач.
- •Радиоактивные методы и что замеряют:
- •46. Вертикальная зональность нефтегазообразования.
- •47. Принцип районирования и выделения нефтегазоносных территорий.
- •48. Природные горючие газы. Формы их нахождения (свободные, попутные, водорастворённые, рассеяные, газогидраты) и разнообразие их состава.
- •49. Схема дифференциального улавливания ув при латеральной миграции.
- •50. Оценка прогнозных ресурсов нефти и газа. Ресурсы
- •Дополнение
- •51. Обзор ведущих нефтегазоносных бассейнов Азии.
- •-Нгб Центральной и Восточной Азии
- •- Нгб Индостанской платформы
- •52. Причины и признаки разрушения залежей нефти и газа.
- •Факторы разрушения залежей нефти и газа.
- •53.Литолого-стратиграфические залежи нефти и газа. Условия их возникновения и морфологическое разнообразие.
- •Дополнительная классификация
- •55. Виды и формы миграции углеводородов (стадийность, фазовое состояние ув и характер миграции).
- •Факторы миграции
- •56. Поглощения промывочной жидкости. Причины их возникновения и способы борьбы с ними.
- •Причины возникновения поглощений:
- •Методы борьбы с поглощениями (по б.Б. Кудряшову и а.М. Яковлеву)
- •57. Нефтегазоносные бассейны рифтовых систем.
- •58. Буровые установки и сооружения. Классификация буровых установок.
- •Классификация буровых установок
- •Формирование проходит в несколько стадий:
- •Условия сохранения:
- •Разрушение залежи:
- •61. Каустобиолиты. Принципы классификации.
- •Дополнение
- •62. Оценка экологического риска и степени техногенного воздействия на окружающую природную среду при разработке нефтегазовых месторождений.
- •1.Мероприятия при эксплуатации скважины
- •64. Структурные залежи. Их классификация (по а. Н. Бакирову).
- •Структурный класс
- •1. Антиклинальная группа
- •2. Моноклинальная группа
- •65. Общие сведения о скважине. Конструкция скважины.
- •Основные элементы скважины:
- •Категории скважин на нефть и газ:
- •66. Роль нефтегазоносности стран Персидского залива в мировой экономики.
- •67. Пробная эксплуатация нефтяных и газовых залежей. Методы воздействия на пласт.
- •68. Современное состояние и развитие нефтегазового комплекса
- •69. Инновационная деятельность предприятия в нефтегазовом производстве. Оценка эффективности инновационной деятельности.
- •70. Цены на нефть, состав, виды и функции цен. Опек и его влияние на цену нефти.
- •Опек и его влияние цену на нефть.
Формула подсчета запасов растворенного газа(водонапорнвй режим)
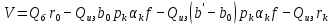
режим водонапорный — поэтому изменение объема воды
Qб - баллансовые
Qиз — извлекаемые
r0 - начальное газосодержание
Для растворенного газа p=10атм
(bэ - b0) ; b0 — добытая нефть с газом, b — когда газ вышел из нефти.
Формула для неводонапорного режима (Жданов)

pk - 10 атм конечное
q — количество растовренного газа на 1 тонну нефти при давлении pk
4. Формы изображения химического состава вод, правила их химического наименования. Химическая классификация вод.
На практике используют следующие формы отображения:
- весовая ионная
- эквивалентная
- процент-эквивалентная формы.
- весовая ионная форма – это выражение состава воды в виде весового количества отдельных ионов. При этом, содержание ионов пишется (в миллиграммах, либо граммах) в единице объема, либо единице массы (обычно в 100 см3, 1000 см3, 100 г, 1 кг).
Если для пресных вод не имеет решающего значения, в каких единицах приведено это выражение, то для рассолов есть различие. Для выражения содержания растворенных газов в ряде веществ, находящихся в коллоидном состоянии, весовая ионная форма не используется.
- эквивалентная форма То есть химический анализ при этом - это веса отдельных ионов в воде, которая образуется вследствие диссоциации (то есть при растворениии, распаде на составляющие) растворенных в воде солей. Соединения, не диссоциирующие (не растворяющиеся) в воде (кремний, железо, алюминий), присутствуют в ней в виде коллоидов и выражаются окислами. Ионная форма выражения анализа широко распространена и является исходной для получения других форм.
более точно учитывает химические свойства воды. Эквивалентный вес (эквивалент) иона - это частное от деления ионного веса на его валентность. Например, эквивалент иона Са2+ равен 20 (40 : 2), а эквивалент иона SO42–, - 48 (96 :2), или 20 весовых единиц иона Са2+ соответствует 48 весовым единицам иона SO42–.
Эквивалентная форма позволяет контролировать точность результатов анализа и вычислять содержание ионов натрия и калия без прямого их аналитического определения, потому что эта форма изображения состава вод основана на том, что ионы реагируют между собой в определенных соотношениях, зависящих от их атомного (или молекулярного) веса и валентности. То есть разные ионы соединяются один с другим в строго определенных весовых соотношениях.
Например, для иона Na+ эквивалентный вес составит 23/1 = 23, для Са++ - 40/2 = 20,
для SO4-- - 96/2 = 48, для Сl- - 35.5/1 = 35,5 и т. д. Тогда на каждые 23 весовых единицы иона Na+ требуется 35,5 весовых единицы иона С1-, 48 весовых единиц иона SO4--..
Для перехода от весовой ионной формы анализа к эквивалентной форме необходимо содержание иона, выраженное в мв (или в г) на 1 л воды, разделить на величину эквивалента иона или, вычислив предварительно величину, обратную эквивалентному весу и называемую переводным коэффициентом, умножить весовое значение иона на этот коэффициент.
В результате такого перехода от ионной формы к эквивалентной получают содержание ионов в мг-экв (миллиграмм-эквивалентах) или в г-экв на то же количество воды. Например, содержание иона Na+, равное 46 мг/л воды, в эквивалентной форме будет равно 46/23 = 2 мг-экв; для SO4-- — при содержании в воде 144 мг/л будет 144/48 = 3 мг-экв и т. д.
Если содержание какого-либо иона выражают в эквивалентной форме, то перед символом иона ставят знак r (английская — русская буква р - реагирующая величина), например гС1-, гСа++ и т. д.
- процент-эквивалентная форма это форма изображения состава вод показывает относительную долю (в процентах), занимаемую каждым ионом во общей ионно-солевой массе, содержащейся в воде. Здесь сумма катионов и сумма анионов составляют по 50 %. Иногда принимают за 100 % сумму катионов (равной сумме анионов), при этом общее содержание ионов будет 200 %.
Содержание каждого иона в процентах вычисляют от общей суммы мг-экв (∑г) следующим образом. Например:
Σ(а +к) – 100%, (сумма ионов и катионов в эквивалентной форме) i – x %, (i – содержание искомого иона в эквивалентной форме; x – содержание искомого иона в процент-эквивалентной форме) Процент-эквивалентная форма не учитывает минерализацию воды. Это дает возможность сравнивать химический состав вод независимо от их степени минерализации.
В гидрогеологии используют три рассмотренные формы. Кроме того, чтобы кратко изобразить химический состав воды используют формулу М.ГЭ. Курлова.
Формула Курлова — это псевдодробь. В числителе — содержание процент-эквивалентной формы главнейших анионов, а в знаменателе содержание катионов. Величины содержания записывают в виде индексов. Ионы располагают в убывающем порядке. Ионы, содержание которых <1% эквивалент, обычно не указывают. Перед дробью отмечаю важнейшие газообразные компоненты воды и величину минерализации. После дроби пишут температуру.
Например: сероводородная соленая вода гидрокарбонатно-хлоридного магниево-кальциево-натриевого состава имеет температуру 35 ˚С, слабощелочная, содержит йод (7.9 мг/дм3) и бром (25 мг/ дм3).
Для оценки нефтянэх вод используют характеристику Пальмера. Основана на утверждении, что ионы соединяются между собой в порядке уменьшения химической активности.
Пальмер выделил шесть солевых характеристик. Основное значение имеют: первая соленость (S1), вторая соленость (S2), первая щелочность (А1) и вторая щелочность (А2).
