
- •1 Круговорот азота в природе
- •1.1 Азотофиксация. Нитрогеназа
- •2 Реакции биосинтеза аминокислот
- •2.2 Трансаминирование кислот
- •2.3 Взаимопревращения аминокислот
- •2.4 Прямое аминирование фумаровой кислоты
- •2.5 Синтез незаменимых аминокислот
- •3 Биосинтез белка
- •3.1 Синтез ДНК – репликация
- •3.2 Синтез РНК – транскрипция
- •3.3 Биологический код
- •3.4 Схема передачи генетической информации от ДНК к белку
- •3.5 Биосинтез белков – трансляция
- •3.6 Понятие о мутациях
- •4 Переваривание белков
- •4.1 Биологическая ценность белков
- •5 Катаболизм аминокислот
- •5.1 Дезаминирование аминокислот
- •5.2 Декарбоксилирование аминокислот
- •5.3 Обезвреживание аммиака и биогенных аминов
- •5.4 Орнитиновый цикл мочевинообразования
- •Список используемой литературы
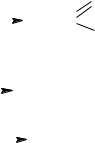
5.3 Обезвреживание аммиака и биогенных аминов
Накопление биогенных аминов может отрицательно сказаться на физиологическом статусе и вызывать ряд существенных нарушений функций в организме.
Однако органы и ткани обладают специальным механизмом обезвреживания биогенных аминов. В данном случае биогенные амины подвергаются окислительному дезаминированию. Катализируют эти реакции ФАД – зависимые моноаминооксидазы и диаминоксидазы:
R |
|
|
|
NH2 |
+ ФАД + Н О |
Моноамин- |
R |
|
C O + NH3+ ФАДН2 |
||
|
|
|
|
|
|
||||||
|
|
CH2 |
2 |
оксидаза |
|
|
|
H |
|||
|
|
Амин |
|
|
|
|
Альдегид |
||||
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
ФАДН2 + О2 |
|
ФАД + Н2О2 |
||||
|
|
|
|
|
|
||||||
2 Н О |
|
2 Н2О + О2 |
|
||
2 2 |
Пероксидаза |
|
Как уже упоминалось выше, у растений амины могут использоваться для биосинтеза алкалоидов.
Аммиак, выделяющийся в реакциях дезаминирования и окисления биогенных аминов, является высокотоксичным соединением.
Один из путей связывания и обезвреживания аммиака в организме животных и растений – это биосинтез глутамина и аспарагина, а также восстановительное аминирование α-кетокислот (см. реакции биосинтеза аминокислот).
У человека, а также всех млекопитающих, амфибий и ряда других животных основным механизмом обезвреживания аммиака является биосинтез мочевины. Мочевина выводится с мочой в качестве главного конечного продукта белкового, азотного обмена.
Обезвреживание образующегося при дезаминировании аминокислот аммиака в виде мочевины свойственно не только животным, но также и различным представителям растительного мира. Исследования показали, что мочевина в растениях играет роль, аналогичную аспарагину и глутамину, т.е. является источником азота для построения белков в случае, если в растении появляется достаточное количество углеводов. Использование мочевины растениями и микроорганизмами для целей синтеза осуществляется благодаря наличию в них чрезвычайно активной уреазы, гидролизующей мочевину с образованием аммиака и угольной кислоты.
Механизм образования мочевины получил название орнитинового цикла мочевинообразования Кребса.
5.4 Орнитиновый цикл мочевинообразования
Мочевина в организме синтезируется из NН3 и СО2. Поступление СО2 и АТФ, необходимых для образования мочевины, обеспечивается работой цикла ди- и трикарбоновых кислот
36
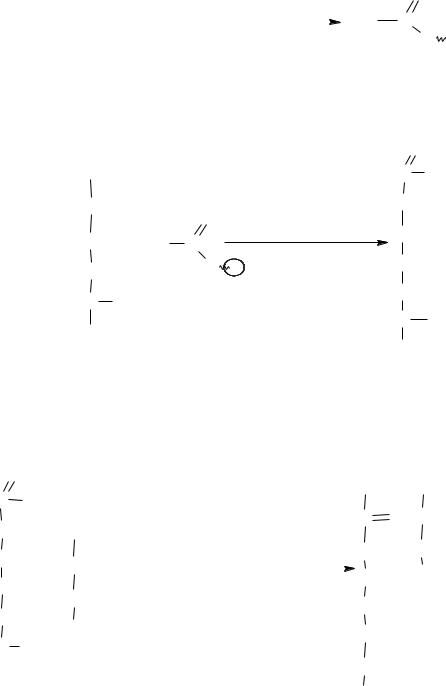
У животных организмов процесс мочевинообразования протекает в печени. На первом этапе синтезируется макроэргическое соединение карбамоилфосфат – метаболически активная форма аммиака:
|
|
|
Карбамоил- |
|
O |
NH3 + CO2 |
+ 2 ATФ + H2O |
|
|
H2N C + 2 AДФ + H3РO4 |
|
|
|
|
|||
фосфатсинтетаза |
|
||||
|
|
|
O Р |
||
|
|
|
|
Карбамоилфосфат |
|
Затем карбамоилфосфат конденсируется с орнитином, образуя цитрул-
лин:
|
|
|
O |
|
|
H2N |
|
|
C NH2 |
||
CH2 |
O |
Орнитин-карбамоил- |
HN |
|
|
H2C |
CH2 |
+ H3РO4 |
|||
+ H2N C |
P трансфераза |
||||
CH2 |
O |
CH2 |
|
||
HC NH2 |
|
CH2 |
|
||
|
HC |
NH2 |
|||
COOH |
|
||||
|
COOH |
||||
Орнитин |
|
||||
|
Цитруллин |
||||
|
|
|
|||
В следующей реакции цитруллин конденсируется с аспарагиновой кислотой – вторым источником азота в цикле мочевины – с образованием аргининсукцината:
|
|
O |
|
|
|
|
|
|
NH2 |
COOH |
|||
C |
NH2 |
|
|
|
|
|
|
||||||
|
|
|
|
|
|
C N |
|
CH |
|||||
NH |
COOH |
|
|
|
|
||||||||
|
|
|
|
||||||||||
|
Аргиноносукцинат- NH |
CH2 |
|||||||||||
H2C |
|
CH |
|
NH2 |
+ АТФ |
||||||||
+ |
|
|
|
CH2 |
COOH + АДФ + Н3РО4 |
||||||||
|
|
|
|||||||||||
|
синтетаза |
|
|||||||||||
H2C |
CH2 |
|
|
||||||||||
CH2 |
|
|
|
CH2 |
|
||||||||
COOH |
|
|
|
|
|||||||||
HC |
|
NH2 |
|
|
|
CH2 |
|
||||||
|
аспарагиновая |
|
HC |
|
NH2 |
|
|||||||
|
|
|
|
||||||||||
|
COOH |
|
кислота |
|
|
|
|||||||
|
|
|
|
|
|||||||||
Цитруллин |
|
|
|
|
|
|
COOH |
|
|||||
|
|
|
|
|
|
|
|
Аргининсукцинат |
|||||
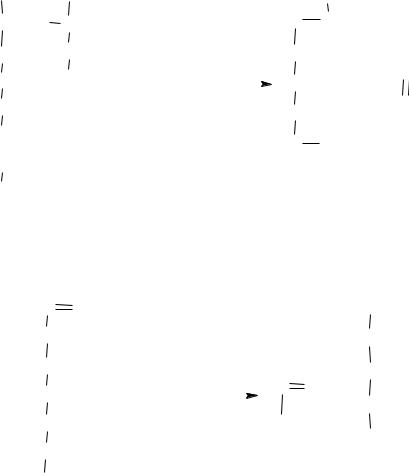
Аргининсукцинат затем расщепляется на аргинин и фумаровую кислоту:
37
NH2 |
COOH |
|
HN |
NH2 |
|
|
|||||||
C |
|
|
N CH |
|
C |
|
NH |
COOH |
|||||
|
|
||||||||||||
|
|
|
|||||||||||
|
|
||||||||||||
|
|
|
|
|
|||||||||
HN |
H2C |
|
CH2 |
|
|
|
|||||||
Аргиноносукцинат- |
|
|
|
|
|
||||||||
|
|
|
CH |
||||||||||
CH2 |
COOH |
CH |
|
|
+ |
||||||||
|
|
|
|
|
|||||||||
CH2 |
|
лиаза |
2 |
|
|
|
CH |
||||||
|
CH2 |
|
|
|
|||||||||
|
|
|
|
|
|||||||||
|
|
|
|
|
|
COOH |
|||||||
CH2 |
|
|
HC |
NH2 |
|
||||||||
|
CH |
|
|
NH2 |
|
Фумаровая |
|||||||
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
COOH |
|
||||||||
COOH |
|
|
|
кислота |
|||||||||
|
Аргинин |
|
|
|
|||||||||
Аргининсукцинат
Завершающей стадией синтеза мочевины является гидролиз аргинина:
NH2 |
|
|
|
|
|
|
|
|
|
|||
|
|
|
NH |
|
|
|
|
|
NH2 |
|||
C |
|
|
|
|
|
|
||||||
HN |
|
|
|
|
|
NH2 |
CH2 |
|||||
CH2 |
|
|
|
CH2 |
||||||||
|
|
|
|
|
||||||||
|
|
C |
O + |
|||||||||
H C |
|
+ Н2О |
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
||||||
2 |
|
|
|
Аргиназа |
|
|
|
|
CH2 |
|||
CH2 |
|
NH2 |
||||||||||
|
|
CH |
|
NH2 |
||||||||
HC |
|
NH2 |
|
Мочевина |
|
|||||||
|
|
|
COOH |
|||||||||
|
|
|
||||||||||
COOH |
|
|
|
|
|
|
||||||
|
|
|
|
|
Орнитин |
|||||||
Аргинин |
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
||||
Реакции орнитинового цикла до стадии образования цитрулина проис-хо- дят в митохондриях, а последующие стадии – в цитозоле.
Суммарное уравнение биосинтеза мочевины:
СО2 + NH3 + Аспартат + 3АТФ + 2Н2О → СО(NH2)2 + фумарат + 2(АДФ +Н3РО4) + АМФ + Н4Р2О7
Таким образом, в молекуле мочевины одна группа NH2 образуется за счет NH3, полученного при распаде аминокислот, вторая – за счет NH2-группы аспарагиновой кислоты. Таким путем NH2-группа любой аминокислоты может включаться в мочевину.
Для пополнения аспарагиновой кислоты фумарат вступает в цикл Кребса и под действием фермента фумаразы присоединяет воду, образуя яблочную кислоту. При участии малатдегидрогеназы яблочная кислота окисляется в оксалоацетат, последний – в реакции трансаминирования с глутаминовой кислотой вновь образует аспарагиновую кислоту.
38
Список используемой литературы
1.Березов Т.Т. Биологическая химия: Учебник для вузов/ Т.Т. Березов, Б.Ф.Коровкин. –3-е изд., перераб. и доп. – М.: Медицина, 1998. – 704 с.
2.Филиппович Ю.Б. Основы биохимии. – М.: Ангар, 1999. – 512 с
3.Жеребцов Н.А., Попова Т.Н., Артюхов В.Г. Биохимия: Учебник. – Воронеж: Из-во ВГУ, 2002. – 696 с.
4.Биохимия растительного сырья. /Под. ред. В.Г. Щербакова.– М.: Колос, 1999. – 376 с.
5.Ленинджер А. Биохимия. – М.: Мир, 1999. Т1.-3.
6.Основы биохимии. /Под ред. Анисимова. – М.: Высшая школа, 1986. – 551 с.
7.Кретович В.Л. Биохимия растений. – М.: Высшая школа, 1986. – 503 с.
8.Комов В.П. Биохимия: Учеб. для вузов (В.П. Комов, В.Н.Шведова). – М.: Дрофа, 2004. – 640 с.
