
Кислородсодержащие_соединения
.docКИСЛОРОДСОДЕРЖАЩИЕ ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ: химические свойства и способы получения
I. Правила номенклатуры описаны в теме 1 (стр. 5–12), общая схема [М.н.] приведена на стр. 10. Названия функциональных групп (основные и заместительные) приведены в табл. 3 (стр. 8–9).
Для низших спиртов широко используются их наименования по названию радикала, с которым связана ОН-группа: этиловый спирт, вторбутиловый и т.д.
Тривиальные названия низших карбоновых кислот, их солей и сложных эфиров приведены в табл. 5 (стр. 51–52). Они же используются при (Р.н.) радикальных производных кислот; например:

II. Приемы получения функциональных групп
1. Получение группы (-ОН) спиртов
-
гидратация алкенов:
![]()
-
восстановление оксосоединений:

Таблица 5
Названия карбоновых кислот, их солей и сложных эфиров
R-COOH – алкановая кислота
HOOC-R-COOH – алкандиовая кислота
R-CO-O-R1 – [алкиловый эфир алкановой кислоты]
|
классифик. |
n |
Формула |
Название кислоты |
Название соли и сложного эфира |
||
|
[М.н.] |
тривиальное |
|||||
|
одноосновные |
предельные |
1 |
H-COOH |
метановая |
муравьиная |
формиат |
|
2 |
CH3COOH |
этановая |
уксусная |
ацетат |
||
|
3 |
CH3CH2COOH |
пропановая |
пропионовая |
пропионат |
||
|
4 |
CH3CH2CH2COOH |
бутановая |
масляная |
бутират |
||
|
4 |
(CH3)2CHCOOH |
2-метилпропановая |
изомасляная |
изобутират |
||
|
5 |
CH3(CH2)3COOH |
пентановая |
валериановая |
валерат |
||
|
6 |
CH3(CH2)4COOH |
гексановая |
капроновая |
капронат |
||
|
непред |
3 |
СH2=CH-COOH |
пропеновая |
акриловая |
акрилат |
|
|
4 |
СH2=C(CH3)COOH |
2-метилпропеновая |
метакриловая |
метакрилат |
||
|
4 |
СH3CH=CH-COOH |
бутен-2-овая |
кротоновая |
кротонат |
||
|
6 |
СH3-(CH=CH)2COOH |
гексадиен-2,4-овая |
сорбиновая |
сорбат |
||
|
ароматические |
7 |
|
карбоксибензол |
бензойная |
бензоат |
|
|
|
8 |
|
1,2-дикарбоксибензол |
фталевая |
фталат |
|
|
диовые |
ароматич. |
8 |
|
1,3-дикарбоксибензол |
изофталевая |
изофталат |
|
8 |
|
1,4-дикарбоксибензол |
терефталевая |
терефталат |
||
|
алифатические |
2 |
НООС-СООН |
этандиовая |
щавелевая |
оксалат |
|
|
3 |
НООС-СН2-СООН |
пропандиовая |
малоновая |
малонат |
||
|
4 |
НООС-(СН2)2-СООН |
бутандиовая |
янтарная |
сукцинат |
||
|
4 |
НООС-СН(СН3)-СООН |
метилпропандиовая |
изоянтарная |
изосукцинат |
||
|
5 |
НООС-СН2-СООН |
пентандиовая |
глутаровая |
глутарат |
||
|
6 |
НООС-СН2-СООН |
гександиовая |
адипиновая |
адипинат |
||
|
4 |
|
бутендиовая (цис-) |
малеиновая |
малеинат |
||
|
4 |
|
бутендиовая (транс-) |
фумаровая |
фумарат |
||
|
|
оксик-та |
6 |
|
3-окси-3-карбокси- пентандиовая |
лимонная |
цитрат |
-
метод Гриньяра (спирты – из альдегидов и кетонов):

-
щелочной гидролиз галогенидов (замена Hal на ОН-группу):
![]()
5) восстановление карбоксила
![]()
6) получение α-гликолей (мягкое окисление алкенов по Вагнеру):

2. Получение фенолов
1) сплавление со щелочами солей ароматических сульфокислот
 2)
кумольный способ
2)
кумольный способ

3) способ Рашига
 4)
метод ИК СО РАН
4)
метод ИК СО РАН

3. Получение оксогрупп

1) окисление спиртов

2) щелочной гидролиз гем-дигалогенидов:
 3) гидратация
ацетиленовых У.В. по Кучерову (см. методич.
указание II-6,
стр. 21);
3) гидратация
ацетиленовых У.В. по Кучерову (см. методич.
указание II-6,
стр. 21);
4) ацилирование аренов по Фриделю-Крафтсу (см. методич. указание II-4, с. 21);
5) плавление солей без щелочи
(а)

(б)
 ;
;
соль гександиовой кислоты циклопентанон
6) восстановление хлорангидридов:
![]()
4. Получение карбоксилов (СООН)
1) окисление первичных спиртов и альдегидов

2) гидролиз нитрилов

3) щелочной гидролиз гем- тригалогенидов

4) по В.Гриньяру из СО2

5) окисление гомологов бензола (получение ароматических кислот)

6) окисление циклокетонов (получение диовых кислот)

7) окисление симметричных алкенов или алкинов:
![]()
![]()
8) гидролиз функциональных производных карбоновых кислот

Карбоновая кислота получается всегда. Вид (состав) второго продукта (HY) определяется классом гидролизуемого функционального производного кислоты: (МеОН) от соли, (R-OH) от сложного эфира, (HCl) от хлорангидрида, (NH3) от амида, (R′-COOH) от ангидрида.
5. Именные реакции кислородсодержащих соединений
-
правило Эльтекова – кето-енольная таутомерия (неустойчивость и изомеризация енолов)

-
правило Эрленмейера (неустойчивость геминальных полиолов)
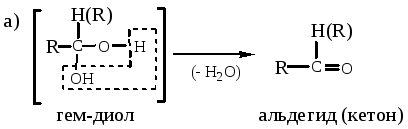

-
Бородина реакция (образование ацеталей)

-
Бутлерова реакция – альдольно-кротоновая конденсация альдегидов (за счет -Н):
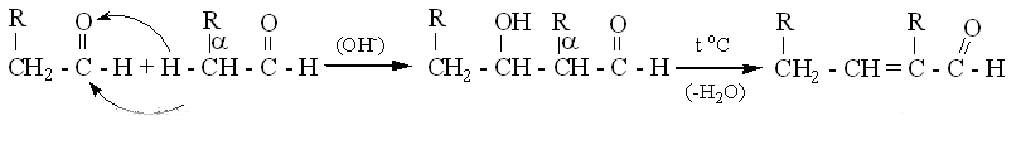
альдегид альдоль 2,4-диалкил- кротоновый альдегид
-
Кневенагеля синтез – конденсация малоновой кислоты с альдегидами с образованием -непредельных кислот

-
Реакции диспропорционирования альдегидов (окисление до кислоты и восстановление до спирта)
(а) реакция Канницаро (ароматические альдегиды)

(б) реакция Тищенко (алифатические альдегиды)

-
реакция Кижнера (восстановление гидразином карбонильных соединений до углеводородов):

-
Байера-Виллигера реакция окисления перекисью водорода оксосоединений (образование сложных эфиров из альдегидов и кетонов):



-
Сложно-эфирная конденсация по Кляйзену с образованием эфира β-оксокислоты

-
Реформатского реакция получения эфиров β-оксикарбоновых кислот взаимодействием альдегидов или кетонов с эфирами α-Br-замещенных кислот в присутствии Zn:


6. Качественные реакции на О-содержащие функциональные группы
1) на ОН-группу спиртов

2) на фенолы
а) кислая среда водного раствора;
б) растворение в щелочи;
в) фиолетовое окрашивание с раствором FeCl3.
Спирты (в том числе и ароматические) со щелочами не реагируют.
3) Обнаружение карбонильного кислорода (в альдегидах и в кетонах):
(а) осадки с Н2N-Х (оксимы с H2N – OH, гидразоны с Н2N-NН2 и фенилгидразоны с Н2N – NH – C6H5);
(б) осадки с NаНSO3 (бисульфитные производные).
4) на альдегидную группу (в отличие от кетогруппы):
альдегид
кислота
![]() ;
;
(б) реакция «медного зеркала»:

5) на многоатомные спирты:





