
- •«Российский государственный университет правосудия»
- •Цели и задачи курса
- •Глава 12. Химические реакции
- •Химические реакции
- •Как проходят реакции
- •Закон сохранения массы
- •Химические уравнения
- •Классификация химических реакций
- •2.По изменению степеней окисления реагентов
- •3.По тепловому эффекту реакции
- •4.По типу превращений реагирующих частиц
- •Скорость химической реакции
- •Вычисление скорости реакции вследствие изменения концентрации реагирующих веществ
- •Вычисление скорости реакции с газовыми компонентами вследствие изменения давления
- •Вычисление скорости реакции вследствие изменения температуры
- •Химическое равновесие
- •1. Вычисление константы химического равновесия
- •2. Вычисление равновесных концентраций по исходным концентрациям реагирующих веществ и наоборот
- •3. Смещение химического равновесия
- •Основная литература
- •Дополнительная литература
- •Интернет – источники
- •Приложение 1 Скорость химической реакции. Химическое равновесие
- •I вариант
- •II вариант
- •Приложение 2 Упражнения и задачи
- •Приложение 3 Задачи для самостоятельного решения
3. Смещение химического равновесия
Химическое равновесие сохраняется до тех пор, пока остаются неизменными условия, в которых система находится. Изменение условий (концентрация веществ, температура, давление) вызывает нарушение равновесия. Через некоторое время химическое равновесие восстанавливается, но уже в новых, отличных от предыдущих условиях. Такой переход системы из одного равновесного состояния в другое называется смещением (сдвигом) равновесия. Направление смещения подчиняется принципу Ле Шателье.
При увеличении концентрации одного из исходных веществ равновесие смещается в сторону большего расхода этого вещества, усиливается прямая реакция. Уменьшение концентрации исходных веществ смещает равновесие в сторону образования этих веществ, так как усиливается обратная реакция. Повышение температуры смещает равновесие в сторону эндотермической реакции, при понижении температуры – в сторону экзотермической реакции. Увеличение давления смещает равновесие в сторону уменьшения количеств газообразных веществ, то есть в сторону меньших объемов, занимаемых этими газами. Напротив, при понижении давления равновесие смещается в сторону возрастания количеств газообразных веществ, то есть в сторону больших объемов, образуемых газами.
П р и м е р 1.
Как повлияет увеличение давления на равновесное состояние следующих обратимых газовых реакций:
а) SO2 + C12=SO2CI2;
б) Н2 + Вr2=2НВr.
Решение:
Используем принцип Ле Шателье, согласно которому повышение давления в первом случае (а) смещает равновесие вправо, в сторону меньшего количества газообразных веществ, занимающих меньший объем, что ослабляет внешнее воздействие возросшего давления. Во второй реакции (б) количество газообразных веществ, как исходных, так и продуктов реакции, равны, как равны и занимаемые ими объемы, поэтому давление не оказывает влияния и равновесие не нарушается.
П р и м е р 2.
В реакции синтеза аммиака (–Q) 3Н2 + N2 = 2NН3 + Q прямая реакция экзотермическая, обратная – эндотермическая. Как следует изменить концентрацию реагирующих веществ, температуру и давление для увеличения выхода аммиака?
Решение:
Для смещения равновесия вправо необходимо:
а) увеличить концентрации Н2 и N2;
б) понизить концентрацию (удаление из сферы реакции) NH3;
в) понизить температуру;
г) увеличить давление.
П р и м е р 3.
Гомогенная реакция взаимодействия хлороводорода и кислорода обратима:
4НС1 + O2 = 2С12 + 2Н2O + 116 кДж.
1. Какое влияние на равновесие системы окажут:
а) увеличение давления;
б) повышение температуры;
в) введение катализатора?
Решение:
а) В соответствии с принципом Ле Шателье повышение давления приводит к смещению равновесия в сторону прямой реакции.
б) Повышение t° приводит к смещению равновесия в сторону обратной реакции.
в) Введение катализатора не смещает равновесия.
2. В каком направлении сместится химическое равновесие, если концентрацию реагирующих веществ увеличить в 2 раза?
Решение:
Начальные скорости прямой и обратной реакций следующие:
υ→ = k→[HCl]02[O2]02; υ0← = k←[H2O]02[Cl2]02
После увеличения концентраций скорость прямой реакции стала:
υ→ = k→[2HCl]4[2O2] = 32 k→[HCl]04[O2]0
то есть возросла по сравнению с начальной скоростью в 32 раза. Аналогичным образом скорость обратной реакции возрастает в 16 раз:
υ← = k←[2H2O]2[2Cl2]2 = 16k←[Н2O]02[С12]02.
Увеличение скорости прямой реакции в 2 раза превышает увеличение скорости обратной реакции: равновесие смещается вправо.
П р и м е р 4.
В какую сторону сместится равновесие гомогенной реакции:
PCl5 = РС13 + Сl2 + 92 КДж,
если повысить температуру на 30 °С, зная, что температурный коэффициент прямой реакции равен 2,5, а обратной – 3,2?
Решение:
Поскольку температурные коэффициенты прямой и обратной реакций не равны, повышение температуры по-разному скажется на изменении скоростей этих реакций. Пользуясь правилом Вант-Гоффа (1.3), находим скорости прямой и обратной реакций при повышении температуры на 30 °С:
υ→(t2)
= υ→(t1)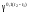 =υ→(t1)2,50,1·30
= 15,6υ→(t1);
=υ→(t1)2,50,1·30
= 15,6υ→(t1);
υ←(t2)
= υ←
(t1)
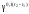 =υ→(t1)3,20,1·30
= 32,8υ←
(t1)
=υ→(t1)3,20,1·30
= 32,8υ←
(t1)
Повышение температуры увеличило скорость прямой реакции в 15,6 раза, обратной – в 32,8 раза. Следовательно, равновесие сместится влево, в сторону образования РСl5.
П р и м е р 5.
Как изменятся скорости прямой и обратной реакций в изолированной системе С2Н4 + H2 ⇄ С2Н6 и куда сместится равновесие при увеличении объема системы в 3 раза?
Решение:
Начальные скорости прямой и обратной реакций следующие:
υ0 = k[C2H4]0 [H2]0; υ 0 = k[C2H6]0.
Увеличение объема системы вызывает уменьшение концентраций реагирующих веществ в 3 раза, отсюда изменение скорости прямой и обратной реакций будет следующим:
υ 0 = k[1/3 С2Н4] [1/3Н2] = 1/9υ0
υ = k[1/3C2H5] = 1/3υ0
Понижение скоростей прямой и обратной реакций неодинаково: скорость обратной реакции в 3 раза (1/3 : 1/9 = 3) превышает скорость обратной реакции, поэтому равновесие сместится влево, в сторону, где система занимает больший объем, то есть в сторону образования С2Н4 и Н2.
