- •Укладачі: Вязовик Віталій Миколайович, к.Т.Н., доцент Атамась Галина Миколаївна, асистент, Клименко Тетяна Всеволодівна, старший викладач Рецензент:Осипенкова і.І., к.Т.Н., доцент
- •18006, М. Черкаси, бульвар Шевченка, 460, 4к.
- •1.Теоретичні основи.
- •2. Хімічні реактиви, посуд та прилади.
- •3.Опис приладів.
- •4. Послідовність виконання роботи.
- •5.Опрацювання результатів.
- •6.Вимоги до звіту.
- •7. Контрольні запитання.
- •1. Основні положення
- •2. Опис експериментального стенду.
- •2. Порядок виконання роботи
- •3. Обробка дослідних даних
- •4. Контрольні питання
- •1. Теоретичні основи процесу.
- •2.Опис установки.
- •3. Методика проведення лабораторних робіт та обробка результатів.
- •1.Теоретичні основи
- •4.Послідовність виконання роботи
- •5.Опрацювання результатів роботи.
- •6.Контрольні запитання
- •1. Теоретичні основи .
- •2. Опис установки.
- •3. Виконання роботи.
- •4. Обробка експериментальних даних.
- •5. Контрольні запитання.
- •1. Основні положення
- •2. Методика проведення випробування
- •3. Обробка експериментальних даних
- •4. Контрольні питання
- •1. Загальні положення
- •2. Методика проведення роботи
- •3. Обробка експериментальних даних
- •1. Теоретичні основи
- •2. Опис установки
- •3. Проведения роботи
- •4. Обробка експериментальних даних
- •1.Теоретичні основи
- •2. Опис установки
- •3. Виконання роботи
- •4. Обробка результатів дослідів
- •Контрольні запитання
- •1. Теоретичні основи
- •2. Опис установки
- •3. Проведення роботи
- •4. Обробка результатів дослідів
- •Контрольні запитання
- •1. Теоретичні основи
- •2. Опис установки
- •3. Проведення роботи
- •4. Обробка результатів дослідів
- •Контрольні запитання
- •1. Теоретичні основи
- •2. Опис установки
- •3. Виконання роботи
- •4. Обробка результатів дослідів
- •Контрольні запитання
- •Опис установки.
- •2. Методика проведення роботи і обробка дослідних даних.
- •1. Теоретичні основи
- •2. Опис експериментальної установки
- •3. Методика проведення випробування
- •4. Обробка результатів випробування
- •Контрольні питання
- •1. Теоретичні основи
- •2. Опис установки
- •3. Методика проведення роботи
- •4. Методика розрахунку
- •Контрольні питання
- •1. Основні положення
- •2. Опис установки
- •3. Методика проведення роботи і обробка дослідних даних
- •Контрольні питання
- •1. Теоретичні основи
- •2. Методика проведення випробувань
- •3. Обробка дослідних даних
- •Контрольні питання
- •1. Загальні положення
- •2. Методика проведення випробування
- •3. Обробка результатів випробування
- •Контрольні питання
- •Література, що рекомендується
1. Теоретичні основи
Багато харчових продуктів є сумішами двох або більш рідин, які в технологічному процесі необхідно розділити. Одним з найпоширеніших способів розділення суміші рідин є перегонка.
Розділення шляхом перегонки застосовується для суміші рідин, які мають різну летючість, тобто при одній і тій же температурі характеризуються різною пружністю пари; іншими словами, суміш складається з рідин з різною температурою кипіння (при тому ж барометричному тиску). Рідина з більш низькою температурою кипіння називається легколетким, або низькокиплячим, компонентом. Рідина з більш високою температурою кипіння називається важколетким, або висококиплячим, компонентом.
Суть процесу перегонки полягає в тому, що суміш, яка розділяється, нагрівається до кипіння, при цьому внаслідок різної летючості компоненти суміші переходять в пару в різний час і в не рівних кількостях. Склад пари і рідини, що залишилася і що утворюється, відрізняється від складу початкової суміші. Пара міститиме більше низькокиплячого компоненту (збагатившись їм в порівнянні з початковою сумішшю), а в рідині, що залишилася і яка називається кубовим залишком, буде більше висококиплячого компоненту.
Отримана пара після конденсації в конденсаторі перетворюється на рідину, що збагачена низькокиплячим компонентом, називається дистилятом.
Кожному складу рідкої суміші відповідає певний склад пари, що знаходиться з нею в рівновазі. Співвідношення цих рівноважних складів звичайно визначають експериментально і за ними складають відповідні таблиці.
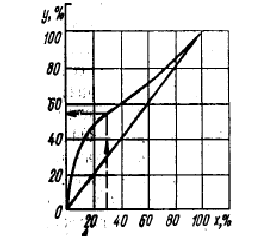
Графічна залежність між складом рідини і складом пари за низькокиплячим компонентом дається на діаграмі у вигляді кривої рівноваги (рис. 1).
За кривою рівноваги можна для заданого складу рідини визначити склад пари. Наприклад, якщо в рідині міститься 30% спирту, то в рівноважній парі - 57%. Діагональ діаграми відповідає однаковому складу низкокиплячого компоненту в рідині і в парі (х=у) Крива рівноваги розташована вище за діагональ, отже, пара збагачена низькокиплячим компонентом. Чим ближче крива рівноваги до діагоналі, тим менше відрізняються температури кипіння компонентів суміші, менше різниця в складах рідини і пари і тим, отже, важче розділяється суміш при перегонці.
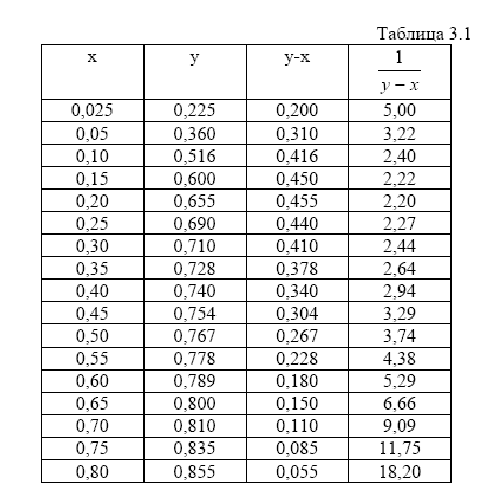
Таблиця 1 - Залежність між складом рідини х і рівноважним їй паром для суміші етиловий спирт – вода
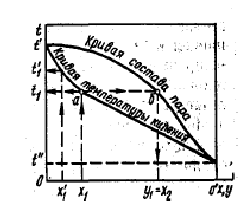
Дослідження процесу перегонки проводиться також за допомогою діаграми температур (рис.2). По осі абсцис відкладені склади рідини х і пари у за низькокиплячим компонентом; по осі ординат - температура кипіння t.
Точка 0' відповідає складу чистого низькокиплячого компоненту (х=100%) з мінімальною температурою кипіння t'; точка 0 - складу чистого висококиплячого компоненту (х = 0) з максимальною температурою кипіння t'.
За діаграмою температур при відомому складі суміші х можна визначити температуру її кипіння і склад пари над нею у. Якщо заданий склад рідини х1, то, підіймаючись вгору до кривої температур кипіння (точка а) і переходячи по горизонталі на вісь ординат, знаходять температуру кипіння суміші t1.
Склад пари можна визначити, продовживши горизонталь з точки а до кривої складу пари (точка б) і спускаючись вниз на вісь абцисс у. З діаграми видно, що при зменшенні вмісту низькокиплячого компоненту в рідині (х1'<х1) температура кипіння підвищується (t1'<t1).
|
Рисунок1 - Крива рівноваги для суміші етиловий спирт -вода |
Рисунок 2 - Діаграма температур
|
Діаграма температур пояснює основний принцип перегонки. Рідині складу х1 з температурою кипіння t1 відповідає пара складу у1. Якщо цю пару сконденсувати, вийде рідина - дистилят складу (х2 = у1) > х1.
Перегонка може бути здійснений різними способами і розділяється на просту, з дефлегмацією і складну (ректифікація).
Проста перегонка здійснюється в установці з перегінним кубом. В процесі простої перегонки при випаровуванні рідини в пару переходить більше низькокиплячого компоненту, а його вміст в рідині, що залишилася, зменшується. Таким чином, під час протікання процесу температура кипіння рідини підвищується, а пара, що утворюється, міститиме все менше і менше низькокиплячого компоненту і, отже, склад дистиляту з цієї пари за вмістом низькокиплячого компоненту з часом погіршуватиметься.
Тому для збору дистиляту різного складу, що стікає з конденсатора, встановлюють декілька приймачів, які сполучають з конденсатором по черзі в ході процесу. Практично проста перегонка зводиться до безперервного повторення процесів однократного випаровування і конденсації пари, причому кожного разу склад рідини за низькокиплячим компонентом зменшується, температура кипіння підвищується і вміст низькокиплячого компоненту в дистиляті зменшується, наближаючись до вмісту його в початковій суміші.
Проста перегонка застосовується у тому випадку, коли не потрібно дуже повне розділення суміші і коли температури кипіння компонентів сильно відрізняються.