
Министерства здравоохранения и социального развития РФ
«Волгоградский государственный медицинский университет»
Кафедра теоретической биохимии с курсом клинической биохимии
Реферат на тему: «Биохимические основы развития атеросклероза»
Выполнил студент 7 гр.
1 курса лечебного факультета
Кондратьева Екатерина Андреевна
Преподаватель
ассистент кафедры
Агеева Елизавета Михайловна
Волгоград
2013 Год.
Оглавление:
Введение 3
Роль ЛПНП и ЛПВП в организме 4
Развитие атеросклероза 7
Лечение 8
Литература 11
Введение
Атеросклероз — хроническое заболевание артерий эластического и мышечно-эластического типа, возникающее вследствие нарушения липидного обмена и сопровождающееся отложением холестерина и некоторых фракций липопротеидов в интиме сосудов.
На данный момент единой теории возникновения данного заболевания нет. Выдвигаются следующие варианты, а также их сочетания:
теория липопротеидной инфильтрации — первично накопление липопротеидов в сосудистой стенке,
теория дисфункции эндотелия — первично нарушение защитных свойств эндотелия и его медиаторов,
аутоиммунная — первично нарушение функции макрофагов и лейкоцитов, инфильтрация ими сосудистой стенки,
моноклональная — первично возникновение патологического клона гладкомышечных клеток,
вирусная — первично вирусное повреждение эндотелия (герпес, цитомегаловирус и др.),
перекисная — первично нарушение антиоксидантной системы,
генетическая — первичен наследственный дефект сосудистой стенки,
хламидиозная — первичное поражение сосудистой стенки хламидиями, в основном, Chlamydia pneumoniae.
гормональная — возрастное повышение уровня гонадотропных и адренокортикотропных гормонов приводит к повышеному синтезу строительного материала для гормонов-холестерина.
Причины развития атеросклероза
Учитывая опыт доказательной медицины, можно выделить факторы, от которых зависит атерогенез: предрасполагающие, провоцирующие и способствующие факторы.
Предрасполагающим фактором является наследственность. При исследованиях выявлено, что у лиц страдающих атеросклеротическим поражением сосудов, имеются близкие родственники, имеющие аналогичное поражение сосудов в сходном или другом сегменте сердечно-сосудистой системы. Пол и возраст также являются факторами: считается, что наиболее часто атеросклероз развивается у мужчин в возрасте 35-50 лет — причины связаны с физиологическими особенностями. Также в группу риска входят лица подверженные хроническим стрессовым ситуациям. Провоцирующим фактором является стресс и курение, которые вызывают сужение сосудов. Доказано, что одна выкуренная сигарета – вызывает генерализованный спазм всех сосудов на 40 минут. Также, никотин способен повышать уровень атерогенного холестерина в крови и усиливает склеивание (агрегацию) тромбоцитов, вызывая спазм сосудов и ухудшая в них ток крови. Что обуславливает, повреждение сосудистой стенки и повышение слипания тромбоцитов, запуская, таким образом, процессы проникновения в стенку сосудов холестерина, накопления его в виде бляшек.
Способствующим фактором является артериальная гипертензия, гипертоническая болезнь. Нездоровый образ жизни: курение, употребление алкоголя, жирная и жаренная пища в значительной мере способствуют развитию болезни. И являются основой для формирования атеросклеротических бляшек.
Ожирение способствует повышенной нагрузке на сердце, нарушается нормальный обмен жиров и углеводов, растет атерогенность крови, снижается переносимость гипоксии.
Роль ЛПВП и ЛПНП в организме.
Прежде чем сказать о развитии атеросклероза, следует указать роль ЛПВП в организме.
ЛПВП выполняют 2 основные функции: они поставляют апопротеины другим ЛП в крови и участвуют в так называемом "обратном транспорте холестерола". ЛПВП синтезируются в печени и в небольшом количестве в тонком кишечнике в виде "незрелых липопротеинов" - предшественников ЛПВП. Они имеют дисковидную форму, небольшой размер и содержат высокий процент белков и фосфолипидов. В печени в ЛПВП включаются апопротеины А, Е, С-II, фермент ЛХАТ. В крови апоС-II и апоЕ переносятся с ЛПВП на ХМ и ЛПОНП. Предшественники ЛПВП пракгически не содержат холестерола и ТАГ и в крови обогащаются холестеролом, получая его из других ЛП и мембран клеток. Для переноса холестерола в ЛПВП существует сложный механизм. На поверхности ЛПВП находится фермент ЛХАТ - лецитишхолестерол-ацилтрансфераза. Этот фермент превращает холестерол, имеющий гидроксильную группу, выступающую на поверхность липопротеинов или мембран клеток, в эфиры холестерола. Радикал жирной кислоты переносится от фосфатидилхолита
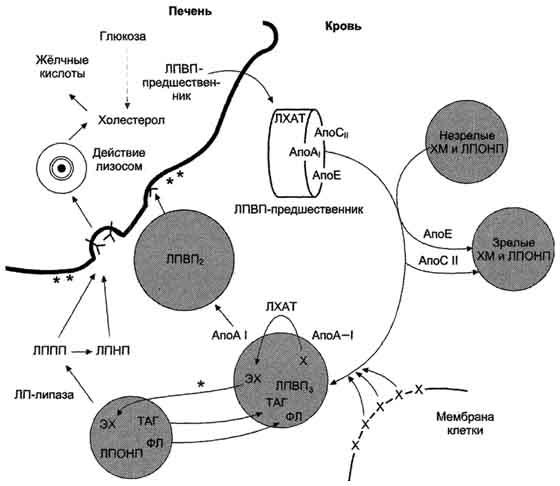
Рис. 8-70. Роль ЛПВП и ЛПНП в обратном транспорте холестерола в печень. Незрелые ЛПВП-предшественники обогащаются холестеролом, который поступает в ЛПВП при участии фермента ЛХАТ с поверхности клеток и других липопротеинов, содержащих холестерол. Незрелые ЛПВП, обогащаясь холестеролом, превращаются в ЛПВП3 - частицы сферической формы и большего размера. ЛПВП3 обменивают эфиры холестерола на триацилглицеролы, содержащиеся в ЛПОНП, ЛППП при участии "белка, переносящего эфиры холестерола"*. ЛПВП3 превращается в ЛПВП2, размер которых увеличивается за счёт накопления триацилглицеролов. ЛПОНП и ЛППП под действием ЛП-липазы превращаются в ЛПНП, которые доставляют холестерол в печень. Часть ЛПВП захватывается клетками печени, взаимодействуя со специфическими для ЛПВП рецепторами к апоА-I. На поверхности клеток печени фосфолипиды и триацилглицеролы ЛППП, ЛПВП2 гидролизуются печёночной ЛП-липазой**, что дестабилизирует структуру поверхности ЛП и способствует диффузии холестерола в гепатоциты. ЛПВП2 в результате этого опять превращаются в ЛПВП3 и возвращаются в кровоток. X - холестерол, ЭХ - эфиры холестерола, ФЛ - фосфолипиды, ЛХАТ - лецитин-холестеролацилтрансфераза, А-I - апопротеин, активатор ЛХАТ.
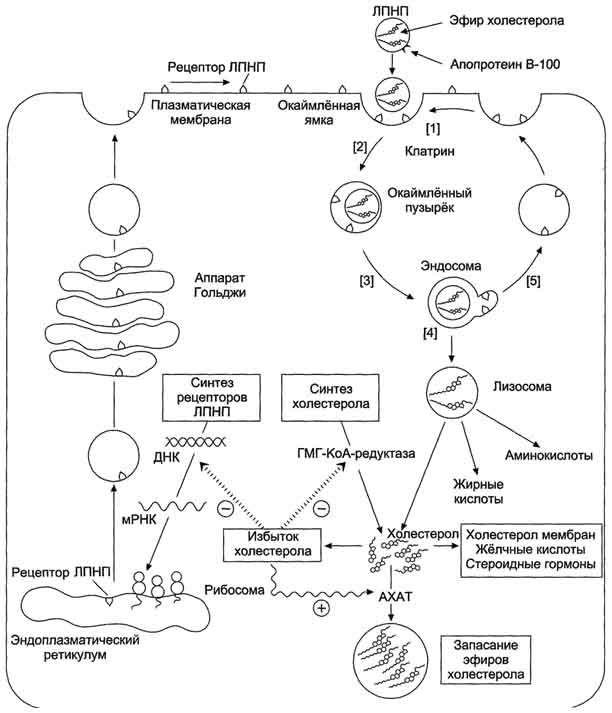
Рис. 8-69. Синтез рецепторов ЛПНП и их последующие превращения. После взаимодействия ЛПНП с рецептором (1) окаймлённые ямки вместе с рецептором и ЛПНП поглощаются по механизму эндоцитоза (2). В образовавшейся эндосоме снижается значение рН за счёт работы протонного насоса, использующего энергию АТФ. При снижении рН рецепторы ЛПНП отделяются от ЛПНП (3), и большая часть рецепторов возвращается в плазматическую мембрану (5). Таким образом, рецепторы ЛПНП могут многократно использоваться клеткой. После удаления рецептора ЛПНП эндосомы сливаются с лизосомами, и гидролитические ферменты лизосом расщепляют компоненты эндосом (4). В результате освобождается холестероп, который может, быть использован для формирования структуры мембран, в клетках печени для синтеза жёлчных кислот, в клетках эндокринной системы для синтеза стероидных гормонов
Таким образом, холестерол из всех тканей возвращается в печень в основном в составе ЛПНП, но в этом участвуют также ЛППП и ЛПВП2. Практически весь холестерол, который должен быть выведен из организма, поступает в печень и уже из этого органа выделяется в виде производных с фекалиями. Путь возвращения холестерола в печень называют "обратным транспортом" холестерола.
Развитие атеросклероза
Процесс начинается с повреждения эндотелия сосудов, причём повреждение может иметь различные механизмы. Важнейший механизм - повреждение эндотелия за счёт изменённой структуры ЛПНП, например в результате активации свободно-радикального ПОЛ в составе ЛПНП; повреждение провоцируется свободными радикалами, образующимися в процессе метаболизма или поступающими извне. В ходе ПОЛ в ЛПНП изменяется не только структура самих липидов, но и нарушается структура апопротеинов. Окисленные ЛПНП захватываются макрофагами через скевенджер-рецепторы. Этот процесс не регулируется количеством поглощённого холестерола, как в случае его поступления в клетки через специфические рецепторы, поэтому макрофаги перегружаются холестеролом и превращаются в "пенистые клетки", которые проникают в субэндотелиальное пространство. Это приводит к образованию жировых полосок в стенке кровеносных сосудов. На этой стадии эндотелий сосудов может сохранять свою структуру. При увеличении количества "пенистых клеток" происходит повреждение эндотелия сосудов. В норме клетки эндотелия секретируют простагландин I2 (простациклин I2), который ингибирует агрегацию тромбоцитов. При повреждении клеток эндотелия тромбоциты активируются. Во-первых, они секретируют тромбоксан А2 (ТХ А2, который стимулирует агрегацию тромбоцитов, что может привести к образованию тромба в области атеросклеротической бляшки; во-вторых, тромбоциты начинают продуцировать пептид - тромбоцитарный фактор роста, стимулирующий пролиферацию ГМК. ГМК мигрируют из медиального слоя во внутренний слой артериальной стенки и способствуют таким образом росту бляшки. Далее происходит прорастание бляшки фиброзной тканью (коллагеном, эластином); клетки под фиброзной оболочкой некротизируются, а холестерол откладывается в межклеточном пространстве. На этой стадии в центре бляшки образуются даже холестериновые кристаллы. На последних стадиях развития бляшка пропитывается солями кальция и становится очень плотной. В области бляшки часто образуются тромбы, перекрывающие просвет сосуда, что приводит к острому нарушению кровообращения в соответствующем участке ткани и развитию инфаркта. Чаще всего атеросклеротические бляшки развиваются в артериях миокарда, поэтому наиболее распространённое заболевание, развивающееся в результате атеросклероза, - инфаркт миокарда.
