
- •Билет №1
- •Билет №2
- •Билет №3
- •Билет №4
- •3. Rp:Sol.Collargoli 1 % – 200 ml
- •Билет №5
- •3. Rp: Sol. Protargoli 0,5 % – 200 ml
- •Билет №6
- •Билет №7
- •1. Летучие растворители
- •Билет №8(ф)
- •Билет №9(ф)
- •Билет №10(ф)
- •Билет №11(ф)
- •Билет №12(ф)
- •Билет №13(ф)
- •Билет №14
- •Билет №15
- •Билет №17(ф)
- •Билет №18(ф)
Билет №6
1. Растворимость - это способность веществ растворяться в воде или других растворителях. Для обозначения растворимости веществ ГФ XI приняты условные термины. Если в рецепте прописаны вещества с различной растворимостью, первыми растворяют труднорастворимые вещества. Большинство ТЛВ являются кристаллическими веществами. Процесс растворения кристаллического вещества состоит из двух одновременно протекающих процессов: сольватации (гидратации) частиц и разрушения кристаллической решетки. Для эффективности растворения важно, чтобы силы сцепления между молекулами растворителя и частицами растворяемого вещества были больше сил взаимного притяжения этих частиц между собой. Вода по сравнению с другими растворителями обладает огромной полярностью (самое высокое значение диэлектрической постоянной). Именно этим свойствам обуславливаются высокая ионизирующая способность воды и ее разрушительное действие на кристаллические решетки многих полярных соединений. При растворении веществ наблюдается поглощение или выделение теплоты. Поглощение теплоты указывает на затрату энергии. Объясняется это тем, что на перевод вещества из твердого состояния в жидкое, т.е на разрушение кристаллической решетки, обязательно расходуется энергия. После же растворения ионы получают возможность относительно свободно двигаться внутри раствора, для чего необходимо увеличение их кинетической энергии. Увеличение ее происходит за счет отнятия энергии у растворителя в форме тепла, в результате чего происходит охлаждение раствора. Чем прочнее кристаллическая решетка, тем значительнее охлаждение раствора. Выделение тепла при растворении веществ всегда указывает на активно протекающую сольватацию, т.е. образование соединений между растворимым веществом и растворителем. Конечный тепловой эффект растворения (Q) нужно рассматривать как сумму двух слагаемых - положительного теплового эффекта сольватации (g) и отрицательного теплового эффекта разрушения кристаллической решетки (-с): Q=g + (-c)
Знак теплового эффекта растворения будет зависеть от того, какое слагаемое преобладает. Если кристаллическая решетка прочна, то слагаемое (-с) численно больше g; в этом случае растворение вещества будет проходить с поглощением тепла. Наоборот, у веществ с непрочной кристаллической решеткой и сильно сольватируемых (гидратируемых) превалирует слагаемое g; при этом растворение будет проходить с выделением тепла. Часто положительный и отрицательный тепловые эффекты растворения оказываются одинаковыми или очень близкими друг к другу; в таких случаях при растворении мы не замечаем охлаждения или разогревания раствора.
2. С учетом КУО: 1000/10=100г; 1000-(100*0,26)=974мл. В подставку отмериваю 974 мл воды, добавляют 100,0 в-ва, фильтруют. Указывают номер серии и анализа, наименование и концентрацию, подпись, дату.
3. Для приготовления ЛФ необходимо взять 84 мл формалина с концентрацией формальдегида 37%. Поправочный коэффициент показывает: отношение фармакопейной концентрации к истинной:
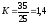 60
۰1,4
= 84 мл V Н2О=
150 - 84 = 66 мл
60
۰1,4
= 84 мл V Н2О=
150 - 84 = 66 мл
Если концентрация в прописи рецепта не указана, то отпускают 35% раствор формальдегида (формалин).
5. Истинный р-р легкорастворимого в-ва. Подставка: 200мл воды мятной+8,0магния сульфата+4,0натрия бромида, процеживаем в контейнер из оранжевого стекла, +20,0мл настоек.
