
10 тем лекций по физе
.pdfIX - Кристмас-фактор, антигемофильный ф. В. Гликопротеид. Образуется в печени под влиянием витамина К. Активируется XIа, VIIа, и IIа. Приводит фактор X в Xа. При его отсутствии – гемофилия В.
X - Стюарт-Прауэр-фактор. Гликопротеид. Образуется в печени под влиянием витамина К. Являясь протромбиназой, активируется VIIа и IХа. Переводит II в IIа.
XI - плазменный предшественник тромбопластина. Гликопротеид. Образуется в печени. Активируется XIIа, калликреином совместно с высокомолекулярным кининогеном (ВМК).
XII - фактор Хагемана. Белок. Предп., образуется эндотелиальными клетками, лейкоцитами, макрофагами. Активируется отрицательно заряженными поверхностями, адреналином, калликреином. Запускает внешний и внутренний механизм образования протромбиназы и фибринолиза, активирует фактор XI и прекалликреин.
XIII - фибринстабилизирующий фактор (ФСФ) фибринолиза. ФСФ – глобулин. Синтезируется фибробластами и мегакариоцитами.
Фактор Флетчера, или прекалликреин. Белок. Участвует в активации XII, плзминогена и ВМК.
Фактор Фитцджеральда, высокомолекулярный кининоген (ВМК). Образуется в тканях. Активируется калликреином. Принимает участие в активации XII, XI и фибринолиза.
Активация плазменных факторов происходит главным образом за счет протеолиза и сопровождается отщеплением пептидных ингибиторов. Активные состояния обозначаются присоединением к номеру «а».
Плазменные фаторы делят на:
1.витамин К- зависимые (образуется преимущественно в печени под влиянием К).
2.витамин К- независимые.
В эритроцитах много соединений, аналогичных тромбоцитарным факторам. Важнейший – частичный тромбопластин (напоминает Р3), входящий в состав мембраны. Также большое количество АДФ, фибриназы и т.д. При травме около 1 % эритроцитов вытекающей крови разрушается, способствуя образованию тромбоцитарной пробки и фибринового сгустка.
Лейкоциты – содержат лейкоцитарные факторы. Моноциты и макрофаги при стимуляции антигеном синтезируют белковую часть тромбопластина (III) – апопротеин III. Является продуцентами витамин К-зависимых факторов свертывания: II, VII, IX и X.
Процесс свертывания крови – преимущественно проферментно-ферментный каскад, в котором проферменты, переходя в активное состояние, приобретают способность активировать другие факторы свертывания крови. Подобная активация может носить последовательный и ретроградный характер.
Три фазы процесса свертывания крови:
1)комплекс последовательных реакций, приводящий к образованию протромбиназы;
2)под влиянием протромбиназы переход протромбина (II) в тромбин (IIа).
3)под влиянием тромбина из фибриногена образуется фибрин.
Первая фаза - образование протромбиназы – может происходить по внешним и внутренним механизмам (Рис. 21).
Внешний механизм предполагает обязательное присутствие тромбопластина (III). Формирование протромбиназы начинается с активации фактора VII при его взамодействии с тромбопластином и фактором XIIа.
VII может переходить в деятельное состояние под влиянием XIа, IXа, Xа, IIа и калликреина.
VIIа переводит X в Xа (появление протромбиназы), а также активирует IX, и этим участвует в образовании протромбиназы по внутреннему механизму.
151
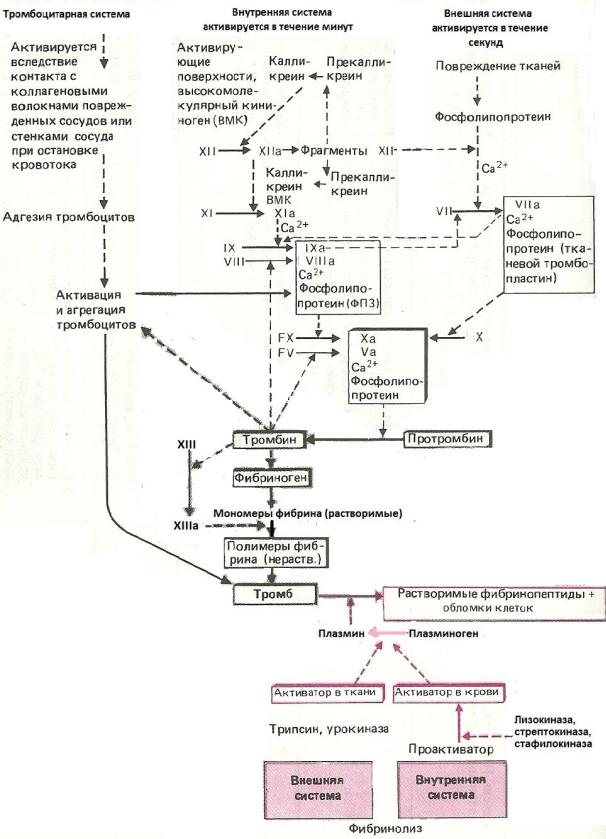
Рис. 21. Схема свёртывания крови и фибринолиза.
Образование протромбиназы по внешнему пути происходит быстро (20 – 30 с), ведет к появлению небольшой порции тромбина (IIа), который способствуют необратимой агрегации тромбоцитов, активации факторов XIII и V и значительно ускоряет формирование протромбиназы по внутреннему механизму.
152
Внутренний механизм связан с участием тромбоцитов (фактор Р3) или разрушенных эритроцитов. Инициатором внутреннего механизма образования протромбиназы является фактор XII, который активируется травмированной поверхностью стенки сосуда, кожей, коллагеном, адреналином (в лабораторных условиях
– при контакте со стеклом).
XIIа переводит XI в XIа. В этой реакции может принимать участие калликреин (активируется XIIа) и ВМК (активируется калликреином).
XIа оказывает влияние на IX, переводя его в IХа. IХа – направляется на протеолиз Х при обязательном участии VIII (VIIIа). Активация Х под влиянием VIII и IXа называется теназной реакцией.
Вторая фаза: переход II в IIа осуществляется под влиянием протромбиназы (Ха) в присутствии Vа и сводится к протеолитическому расщеплению протромбина; появляется фермент тромбин, обладающий свертывающей активностью.
Третья фаза: переход фибриногена в фибрин носит поэтапный характер.
Под влиянием IIа от фибриногена отщепляются фибринопептиды и образуют фибрин–мономер Iм. Из него, за счет полимеризации формируются олигомеры и димеры фибрина (Iо и Id). Из них за счет продольного и поперечного связывания образуются протофибриллы – легкорастворимый фибрин Is (быстро лизирующийся под влиянием плазмина, трипсина).
Вдальнейшем под влиянием XIII (ФСФ), который после активации тромбином в присутствии Са2+ прошивает фибринполимеры дополнительными перекрестными связями, появляется труднорастворимый фибрин, i (insolulle).
Сгусток становится резистентным к фибринолитическим (протеолитическим) агентам.
Образовавщийся фибриновый сгусток благодаря тромбоцитам, входящим в его структуру, сокращается и уплотняется (наступает ретракция) и прочно закупоривает сосуд.
Свертывание крови, контактирующей с травмированными тканями, осуществляется за 5 – 10 минут. Основное время уходит на образование протромбиназы. Переход протромбина в тромбин и фибриногена в фибрин осуществляется довольно быстро.
Вестественных условиях время свертывания крови может уменьшаться (гиперкоагуляция) или удлиняться (гипокоагуляция).
Фибринолиз.
Фибринолиз является неотъемлемой частью системы гемостаза, всегда сопровождает процесс свертывания крови и активируется факторами, принимающими участие в этом процессе.
Предотвращает закупорку кровеносных сосудов фибриновыми сгустками. Ведет к реканализации сосудов после остановки кровотечения.
Ферментом, разрущающим фибрин, является «плазмин» («фибринолизин»). В циркуляции находятся в неактивном состоянии в виде профермента плазминогена.
Может протекать по внешнему и внутреннему механизму.
Внешний фибринолиз осуществляется при участии тканевых активаторов, которые синтезируются в эндотелии сосудов – тканевой активатор плазминогена (ТАП), урокиназа. Последняя также образуется в юкстагломерулярном аппарате почки.
Внутренний фибринолиз осуществляется плазменными активаторами, а также активаторами форменных элементов. Разделен на Хагеман-зависимый и Хагеман – независимый.
Хагеман-зависимый протекает под влиянием XIIа, калликреина и ВМК, которые переводят плазминоген в плазмин.
Хагеман-независимый (под влиянием активаторов плазминогена форменных элементов и активированных протеинов) определяется наиболее быстро и носит срочный
153
характер. Его основное назначение сводится к очищению сосудистого русла от нестабилизированного фибрина, образующегося в процессе внутрисосудистого свертывания крови.
Образовавшийся в результате активации плазмин вызывает расщепление фибрина. При этом появляются ранние (крупномолекулярные) и поздние (низкомолекулярные) продукты фибринолиза.
В плазме находятся и ингибиторы фибринолиза: α2 – антиплазмин (связ. плазмин, трипсин, калликреин, урокиназу, ТАП). α2 – протеазный ингибитор α2-макроглобулин, С1
– протеазный ингибитор. Ряд ингибиторов активатора плазминогена, синтезируется эндотелием, макрофагами, моноцитами, фибробластами.
Фибринолитическая активность крови определяется соотношением активаторов и ингибиторов фибринолиза.
Наряду с ферментативным фибринолизом, Б.А. Кудряшов, выделил неферментативный фибринолиз, обусловленный соединениями естественного антикоагулянта гепарина с ферментами и гормонами. Он приводит к расщеплению в сосудистом русле нестабилизированного фибрина (фибрин-мономеры и фибрин S).
Естественные антикоагулянты.
В естественных условиях кровь остается жидкой благодаря наличию в кровотоке естественных антикоагулянтов (фибринолитическое звено системы гемостаза). Их делят на первичные и вторичные.
Первичные антикоагулянты всегда присутствуют в циркулирующей крови. Вторичные – образуются в результате протеолитического расщепления факторов
свертывания крови в процессе образования и растворения фибринового сгустка. «Отработанные факторы свертывания крови» и продукты деградации фибриногена и фибрина стимулируют фибринолиз. Роль вторичных антикоагулянтов сводится к ограничению внутрисосудистого свертывания крови и распространения тромба по сосудам.
При ускорении свертывания крови и одновременно торможению фибринолиза создаются условия для развития тромбозов, эмболий и ДВС–синдрома (диссиминированное внутрисосудистое свертывание).
ДВС-синдром возникает при переливании несоответствующих групп крови, обширных травмах, длительной операции и т.д. Возникает гиперкоагуляция, которая из-за интенсивного потребления тромбоцитов, фибриногена, факторов V, VIII, XIII и др. сменяется вторичной гипокоагуляцией вплоть до полной неспособности к образованию фибриновых сгустков, что приводит к кровотечениям.
154
7. ФИЗИОЛОГИЯ КРОВООБРАЩЕНИЯ
7.1. Роль сердца в кровообращении, сердечный цикл; 7.2. Основные законы гемодинамики; 7.3. Функциональные особенности сосудов; 7.4. Методы исследования сердечной деятельности; 7.5. Методы исследования сердечнососудистой системы; 7.6. Механизмы регуляции деятельности сердца; 7.7. Регуляция тонуса сосудов; 7.8. Регионарное кровообращение; 7.9. Лимфообращение.
7.1. РОЛЬ СЕРДЦА В КРОВООБРАЩЕНИИ, СЕРДЕЧНЫЙ ЦИКЛ
Основные функции системы кровообращения: транспорт газов и веществ; удаление метаболитов и повреждённых клеток; обмен тепла в организме.
Воснове непрерывного движения крови по сосудам лежит деятельность сердца как насоса и возникающий при этом градиент давления, т.е. разница давлений по ходу сосудистого русла (каскадный уровень снижения давления). Сопротивление, которое испытывает кровь, проходя по различным сосудам, в определённой степени препятствует кровотоку.
Главные функции сердца – резервуарная и нагнетательная. В период диастолы в отделах сердца накапливается очередная порция крови. Во время систолы желудочков часть этой крови выбрасывается из левого в аорту (большой круг), а из правого в лёгочную артерию (малый круг).
За 1 минуту у взрослого человека из каждого желудочка выбрасывается около 4,5 - 5 л крови – минутный объём крови (МОК).
Максимальный объём крови перед началом систолы желудочков 140 – 180 мл – «конечно-диастолический объём». Характеризует максимальные возможности сердца как насоса.
Впериод систолы из желудочков выбрасывается «систолический объём» (СО) - 60
–80 мл. Чем он больше и чем чаще сокращается сердце, тем выше его производительность как насоса. Если СО – 70 мл, ЧСС 70 уд./мин, то МОК – 4900 мл. СО
–важнейшая характеристика производительности работы сердца. Синонимы СО – ударный объём и сердечный выброс.
После изгнания крови в желудочках остаётся около 70 мл крови. Это «конечносистолический объём». Состоит из резервного и остаточного объёмов; остаточный объём
–остаётся даже после самого мощного сокращения, а резервный объём – может выбрасываться при усиленной работе.
Сердечный индекс: МОК/площадь поверхности тела. Ударный индекс: СО/площадь поверхности тела. Сердечный цикл.
Систола предсердий. При распространении возбуждения от синоатриального узла по миокардиоцитам предсердий начинается их сокращение. В процесс вовлекаются все миокардиоциты правого, чуть позже, и левого предсердий. В результате сжимаются устья вен, впадающих в предсердия, повышается внутрипредсердное давление – в левом до 5-8 мм рт.ст., в правом до 4-6 мм рт.ст.. Кровь, которая накопилась в предсердиях во время диастолы, изгоняется в желудочки. Длительность систолы предсердий около 0,1 с. За это время в желудочки входит около 40 мл крови (30 % конечно-диастолического объёма ).
После окончания систолы предсердий начинаются 2 процесса: 1) в предсердиях – диастола (0,7 с); 2) в желудочках начинается систола (0,33 с), а затем диастола (0,47 с). Все временные интервалы приводятся для ЧСС – 75 ударов/минуту.
1-й период систолы желудочков – период напряжения (0,08 с) – состоит из 2-х фаз: асинхронного сокращения (0,05 с) и изометрического сокращения (0,03 с).
Фаза асинхронного сокращения начинается с началом возбуждения желудочков. В течение этой фазы процессы возбуждения (и следующие за ними процессы сокращения) распространяются по миокарду желудочков. Давление в желудочках сначала близко к 0, а
155
к концу фазы – сокращение охватывает все волокна миокарда и давление в желудочках начинает быстро нарастать.
Фаза изометрического сокращения начинается с захлопывания створок предсердножелудочковых (атриовентрикулярных) клапанов, когда давление в желудочках станет выше, чем в предсердиях. При этом возникает I-й (систолический) тон сердца. После захлопывания клапанов и створчатые и полулунные клапаны (и вход и выход) закрыты, объём крови постоянен, т.к. жидкость практически не сжимаема, длина волокон не изменяется, увеличивается их напряжение. Давление в желудочках быстро растёт: до 7080 мм рт.ст. в левом и до 15-20 мм рт.ст. в правом. Левый желудочек приобретает круглую форму и с силой ударяется о внутреннюю поверхность грудной стенки. В 5-м межреберье слева от среднеключичной линии в этот момент определяется верхушечный толчок.
К концу фазы изометрического сокращения давление крови в левом желудочке становится выше, чем в аорте, а в правом желудочке выше, чем в лёгочной артерии. Происходит открытие полулунных клапанов и начинается период изгнания (0,25 с).
Вначале процесс изгнания совершается быстро – фаза быстрого изгнания (0,12 с). Давление в желудочках нарастает: в левом до 120 – 130 мм рт. ст. , в правом до 25 – 30 мм рт. ст.. Такие же давления создаются соответственно в аорте и лёгочной артерии. По мере заполнения аорты и лёгочной артерии кровью, сопротивление выходящему потоку крови увеличивается, фаза быстрого изгнания сменяется фазой медленного изгнания (0,13 с).
Вконце фазы медленного изгнания миокард желудочков начинает расслабляться. Давление в желудочках падает, кровь из аорты и лёгочной артерии устремляется обратно
вполости желудочков и захлопывает полулунные клапаны. При этом возникает II-й (диастолический) тон сердца. Время от начала расслабления желудочков до захлопывания полулунных клапанов называется протодиастолическим периодом (0,04 с).
После захлопывания полулунных клапанов давление в желудочках падает. Створчатые клапаны в это время ещё закрыты, объём крови, а, следовательно, и длина волокон миокарда не изменяется – период изометрического расслабления (0,08 с).
Кконцу изометрического расслабления давление в желудочках становится ниже, чем в предсердиях, открываются предсердно-желудочковые клапаны и кровь из предсердий начинает поступать в желудочки. Начинается период наполнения желудочков кровью (0,25 с), делящийся на фазы быстрого (0,08 с) и медленного (0,17 с) наполнения.
С момента открытия предсердно-желудочковых клапанов вся кровь из предсердий (около 33 мл) быстро устремляется в желудочки. Колебания стенок желудочков вследствие быстрого притока крови вызывает появление III-го тона сердца.
Во время фазы медленного наполнения вся кровь, поступающая из вен в предсердия, протекает сразу в желудочки.
Кконцу фазы медленного наполнения возникает систола предсердий. Предсердия нагнетают в желудочки дополнительное количество крови. Во время систолы предсердий
вжелудочках – пресистолический период (0,1 с).
Колебания стенок сердца, вызванные сокращением предсердий и дополнительным поступлением крови в желудочки, ведёт к появлению IV-го тона сердца.
Если I-й и II-й тоны выявляются уже при аускультации, то III-й и IV-й тоны сердца выявляются при регистрации фонокардиограммы.
7.2. ОСНОВНЫЕ ЗАКОНЫ ГЕМОДИНАМИКИ
Движение крови по сосудам определяется разницей давлений по ходу сосудистого русла (каскадным уровнем снижения давления).
Для оценки артериального давления используются следующие показатели:
Пик кривой давления, регистрируемый во время систолы – систолическое артериальное давление (САД);
Минимальное значение давления в диастоле – диастолическое артериальное давление (ДАД);
156
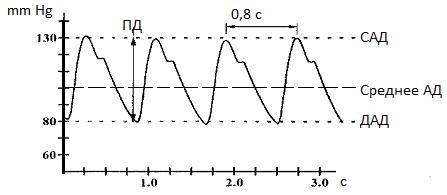
Пульсовое давление ПД=САД-ДАД.
Среднее артериальное давление (Среднее АД) – это результирующая (равнодействующая) всех переменных значений давления в течение сердечного цикла. Это та постоянная величина давления, при которой в отсутствии пульсовых колебаний наблюдался бы такой же гемодинамический эффект.
Для точного вычисления Ср.АД необходимо вычислить площадь под кривой изменения давления и разделить её на длину этой кривой. Для приближённого вычисления Ср.АД используют следующие формулы:
Для аорты Среднее АД = ДАД + 1/2ПД Для периферических артерий Среднее АД = ДАД + 1/3ПД (формула Сеченова).
Рис. 22. Кривая изменения давления в аорте.
Один из основных законов гидродинамики (и, соответственно, гемодинамики): Количество жидкости Q, протекающее через любую трубку, прямо
пропорционально разности давлений вначале (P1) и в конце (P2) трубы и обратно пропорционально сопротивлению (R) току жидкости: Q = (P1-P2)/R.
Т.к. давление в месте впадения полых вен в сердце близко к нулю Q = P/R, где Q – количество крови, изгнанное сердцем за 1 минуту; P – среднее давление в аорте; R – величина сосудистого сопротивления.
Сопротивление трубки определяется по формуле Пуазейля: R = 8lη/πr4, где l – длина трубки, η – вязкость жидкости, r – радиус.
Но геометрия сосудов изменяется вследствие сокращения сосудистых мышц. Вязкость крови также может уменьшаться с уменьшением диаметра сосуда < 1 мм. Форменные элементы располагаются в центре потока, а плазма в пристеночном слое (вязкость плазмы меньше вязкости крови).
При последовательном соединении трубок разного диаметра общее сопротивление вычисляется по формуле R=R1+R2+…+Rn; при параллельном соединении трубок
R=1/(1/R1+1/R2+…+1/Rn).
Наибольшей величиной сопротивления по уравнению Пуазейля должен обладать капилляр, диаметр которого 5-7 мкм. Однако, огромное количество капилляров включено
всосудистую сеть параллельно, и их суммарное сопротивление меньше, чем суммарное сопротивление артериол. В артериолах (ø 15-70 мкм) возникает основное сопротивление току крови. Изменение сопротивления артериол меняет уровень давления крови в артериях. В случае уменьшения сопротивления отток крови из артерий увеличивается, а давление в них уменьшается; наоборот, увеличение сопротивления артериол приводит к уменьшению оттока крови из артерий и повышению в них давления. Изменение просвета артериол – один из главных регуляторов общего артериального давления – «краны сердечно-сосудистой системы» (И.М.Сеченов). Другая важная роль артериол – перераспределение кровотока, регуляция местного кровотока через тот или иной орган: в работающем органе тонус артериол уменьшен, обеспечивая повышенный приток крови, а
внеработающих органах тонус артериол повышен.
157
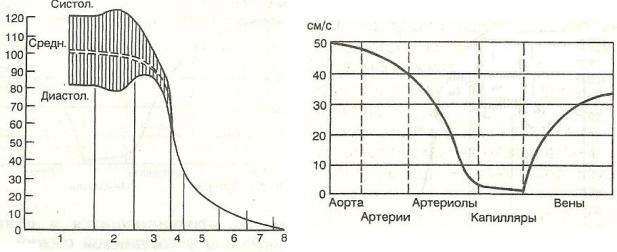
О сопротивлении в различных сосудах можно судить по разности давлений в начале и конце сосуда. Прямые измерения показывают, что давление на протяжении крупных и средних артерий падает на 10 %, а в артериолах и капиллярах на 85 %. Т.е. 10 % энергии, затрачиваемой желудочками сердца на изгнание крови, расходуется на продвижение её в крупных и средних артериях, а 85 % - на продвижение в артериях и капиллярах.
|
|
Рис. 23. Изменения давления в различных |
Рис. 24. Средняя линейная скорость тока |
частях сосудистой системы. |
крови в разных частях сосудистой системы. |
1 – в аорте; 2 – в крупных артериях; 3 – в |
|
мелких артериях; 4 – в артериолах; 5 – в |
|
капиллярах; 6 – в венулах; 7 – в венах; 8 – |
|
в полой вене. |
|
Линейная скорость кровотока – это отношение объёмной скорости кровотока к площади поперечного сечения сосуда (параллельных сосудов): V = Q / πr2.
Объём крови, протекающей за 1 минуту через аорту, равняется объёму, протекающему через полые вены; объём, протекающий через лёгочную артерию, равняется объёму, протекающему через лёгочные вены.
При постоянном объёме крови, протекающем через любое общее сечение сосудистой системы, линейная скорость кровотока не может быть постоянной. Она зависит от ширины данного отдела сосудистого русла. Чем больше общая площадь сечения, тем меньше линейная скорость кровотока. Аорта – самый крупный сосуд – самое узкое место кровеносной системы. При разветвлении артерий происходит увеличение суммарного сосудистого русла. Сумма просветов всех капилляров в 500-600 раз больше просвета аорты, соответственно кровь в капиллярах движется в 500-600 раз медленнее, чем в аорте. В венах линейная скорость снова возрастает – при слиянии вен происходит сужение суммарного просвета. В полых венах линейная скорость достигает половины скорости в аорте.
Т.к. кровь выбрасывается из сердца порциями, кровоток в артериях имеет пульсирующий характер; V и Q максимальны в период систолы и уменьшаются в диастолу.
Ток жидкости может быть ламинарным и турбулентным. При возрастании линейной скорости до некоторой величины в струе образуются завихрения, сопровождающиеся шумом – течение из ламинарного (скользящих слоёв) превращается в турбулентное. Эта величина определяется числом Рейнольдса: Re = VDρ/η, где V – линейная скорость, D – диаметр сосуда, ρ – плотность, η – вязкость. В местах разветвления сосудов завихрения образуются легче, поэтому вероятность сосудистых поражений (атеросклероза) в этих участках выше.
158
7.3.ФУНКЦИОНАЛЬНЫЕ ОСОБЕННОСТИ СОСУДОВ
Сморфологической точки зрения кровеносные сосуды – трубки различного диаметра, состоящие из 3-х основных слоёв: внутреннего (эндотелиального), среднего (ГМК, коллагеновые и эластические волокна), наружного.
Помимо размеров, сосуды отличаются строением среднего слоя:
- в аорте и крупных артериях преобладают эластические и коллагеновые волокна, что обеспечивает их упругость и растяжимость (сосуды эластического типа);
- в артериях среднего и мелкого калибра, артериолах, прекапиллярах и венулах преобладают ГМК (сосуды мышечного типа, обладающие высокой сократимостью);
- в средних и крупных венах есть ГМК, но их сократительная активность невысока; - капилляры вообще лишены ГМК.
Это имеет определённое значение для функциональной классификации:
1)Упруго-растяжимые (магистральные) сосуды – аорта с крупными артериями в большом круге кровообращения и лёгочная артерия с её ветвями в малом круге кровообращения. Это сосуды эластического типа, образующие эластическую, или компрессионную, камеру. Обеспечивают преобразование пульсирующего кровотока в более равномерный и плавный. Часть кинетической энергии, развиваемой сердцем во время систолы, затрачивается на растяжение этой компрессионной камеры, в которую поступает значительный объём крови, растягивающий её. При этом кинетическая энергия, развитая сердцем, переходит в энергию эластического напряжения артериальных стенок. Когда систола заканчивается, растянутые стенки артерий компрессионной камеры спадаются и проталкивают кровь в капилляры, поддерживая кровоток во время диастолы.
2)Сосуды сопротивления (резистивные сосуды) – артериолы и прекапиллярные сфинктеры, т.е. сосуды мышечного типа. От прекапиллярных сфинктеров зависит число функционирующих капилляров.
3)Обменные сосуды – капилляры. Обеспечивают обмен газами и другими веществами между кровью и тканевой жидкостью. Количество функционирующих капилляров может изменяться в каждом участке ткани в значительных пределах, в зависимости от функциональной и метаболической активности.
4)Шунтирующие сосуды (артериовенозные анастомозы) – обеспечивают «сброс» крови из артериальной системы в венозную, минуя капилляры; значительно повышают скорость кровотока; участвуют в теплообмене.
5)Собирательные сосуды (кумулятивные) – вены.
6)Ёмкостные сосуды – крупные вены, обладающие высокой растяжимостью. Содержат ~ 75 % объёма циркулирующей крови (ОЦК). Артериальный отдел ~ 20 % ОЦК, капиллярный ~ 5-7,5 %.
ОЦК распределяется по частям тела не равномерно. Почки, печень, сердце, мозг, составляющие 5 % массы тела, получают более половины всей крови.
ОЦК – это не вся кровь организма. В состоянии покоя до 45 - 50 % всего объёма крови, имеющейся в организме, находится в кровяных депо: селезёнке, печени, подкожном сосудистом сплетении и лёгких. В селезёнке содержится ~ 500 мл крови, которая может быть почти выключена из кровотока. Кровь в сосудах печени и сосудистом сплетении кожи (до 1 л) циркулирует в 10 – 20 раз медленнее, чем в других сосудах.
Микроциркуляторное русло – совокупность конечных артерий, артериол, капилляров, венул, мелких венул. Движение крови по микроциркуляторному руслу обеспечивает транскапиллярный обмен.
Капилляры имеют диаметр ~ 5 – 7 мкм, длину ~ 0,5 – 1 мм. Скорость кровотока ~ 0,5 – 1 мм/с, т.е. каждая частица крови находится в капилляре ~ 1 с. Общая длина капилляров составляет ~ 100000 км.
Есть 2 вида функционирующих капилляров – магистральные, образующие кратчайший путь между артериолами и венулами, и истинные, которые отходят от
159
артериального конца магистрального капилляра и впадают в его венозный конец. Истинные образуют капиллярные сети. В магистральных скорость кровотока выше.
Втканях с более интенсивным обменом число капилляров больше. Капилляры различаются по строению эндотелиального каркаса:
1)С непрерывной стенкой – «закрытые». Это большинство капилляров большого круга кровообращения. Обеспечивают гистогематический барьер.
2)Окончатые (с фанестрами – окошечками). Способны пропускать вещества, диаметр которых достаточно велик. Располагаются в почечных клубочках, в слизистой кишечника.
3)С прерывистой стенкой – между соседними эндотелиальными клетками есть щели, через которые проходят форменные элементы крови. Располагаются в костном мозге, печени, селезёнке.
Взакрытых капиллярах переход веществ из капилляра в ткань и наоборот совершается за счёт диффузии и фильтрации (с реабсорбцией). Пока кровь проходит через капилляр, может произойти 40-кратный обмен между кровью и тканями. Лимитирующий фактор – способность вещества проходить через фосфолипидные участки мембраны и размеры вещества. В среднем из капилляров каждую минуту выходит ~ 14 мл жидкости (~20 л/сутки). Вышедшая на артериальном конце капилляра жидкость дренирует межклеточное пространство, очищает его от метаболитов и ненужных частиц. На венозном конце капилляра большая часть жидкости с метаболитами вновь поступает в капилляр.
Закономерности, обуславливающие обмен жидкости между капиллярами и тканевыми пространствами, были описаны Старлингом.
Силы, способствующие фильтрации, - это гидростатическое давление крови (Ргк) и онкотическое тканевой жидкости (Рот), составляющие в сумме фильтрационное давление. Силы, препятствующие фильтрации, но способствующие реабсорбции, - это онкотическое давление крови (Рок) и гидростатическое давление тканевой жидкости (Ргт), составляющие в сумме реабсорбционное давление.
На артериальном конце капилляра:
Ргк ~ 32,5 мм рт. ст., |
Рот ~ 4,5 мм рт.ст., |
(Ргк + Рот) ~ 37 мм рт. ст. |
Рок ~ 25 мм рт.ст., |
Ргт ~ 3 мм рт.ст., |
(Рок + Ргт) ~ 28 мм рт. ст. |
Результирующее давление, обеспечивающее фильтрацию: 37 – 28 = 9 мм рт.ст.
На венозном конце капилляра: |
|
||
Ргк ~ 17 мм рт. ст., |
Рот ~ 4,5 |
мм рт.ст., |
(Ргк + Рот) ~ 21,5 мм рт. ст. |
Рок ~ 25 мм рт.ст., |
Ргт ~ 3 |
мм рт.ст., |
(Рок + Ргт) ~ 28 мм рт. ст. |
Результирующее давление, обеспечивающее реабсорбцию: 21,5 – 28 = - 6,5 мм рт. ст.
Т.к. фильтрационная результирующая на артериальном конце капилляра выше, чем реабсорбционная результирующая на венозном, объём фильтрации на артериальном конце капилляра выше, чем объём реабсорбции на венозном (20 л/18 л в сутки). Остальные 2 л идут на образование лимфы. Это своеобразный дренаж тканей, благодаря которому крупные частицы, не способные пройти через стенку капилляра, проходят по лимфатической системе, в том числе через лимфатические узлы, где подвергаются разрушению. В конечном итоге, лимфа через грудной и шейный протоки возвращается в венозное русло.
Венозное русло предназначено для сбора крови, т.е. выполняет коллекторную функцию. В венозном русле кровь испытывает меньшее сопротивление, чем в мелких артериях и артериолах, однако большая протяжённость венозного русла приводит к тому, что давление крови по мере приближения к сердцу снижается почти до 0. Давление в венулах 12 – 18 мм рт.ст., в венах среднего калибра 5 – 8 мм рт.ст., в полых венах 1 – 3 мм рт.ст.. В то же время, линейная скорость кровотока, по мере приближения к сердцу, последовательно возрастает. В венулах она составляет 0,07 см/с, в средних венах 1,5 см/с, в полых венах 25 – 33 см/с.
160
