
- •Томский государственный университет систем
- •1.1. Международная программа охраны вод
- •1.2. Гидрология и ее связь с другими науками
- •1.3. Методы изучения водных объектов
- •1.4. Из истории гидрологии
- •1.5. Исследование вод в России
- •2.1 Водный фонд рф и право пользования водными объектами
- •2.2. Государственный мониторинг водных объектов
- •2.3. Водопользование
- •2.4. Права водопользователя
- •2.5. Обязанности водопользователя
- •3.1 Молекула воды.
- •3.2. Химические свойства воды
- •3.3. Формирование химического состава природных вод
- •3.4 Классификация вод по химическому составу
- •4.1 Минерализация воды
- •4.2 Важнейшие показатели воды
- •4.3 Растворенные газы
- •4.4 Главные ионы
- •4.5 Биогенные компоненты
- •4.6 Органическое вещество
- •Контрольные вопросы:
- •5.2 Плотность воды
- •5.3 Тепловые свойства воды.
- •5.4 Вязкость воды (внутреннее трение).
- •5.5 Поверхностное натяжение и смачивание.
- •5.6 Оптические свойства воды.
- •5.7 Акустические свойства воды.
- •5.8 Электропроводность воды.
- •Контрольные вопросы:
- •6.1 Органолептические наблюдения
- •6.2 Запах, мутность, цветность и прозрачность
- •6.3 Нормирование и качество воды
- •6.4 Пдк некоторых веществ в питьевой воде
- •6.5 Основные методы очистки воды
- •6.5.1 Удаление кислорода из воды.
- •6.5.3. Ионный обмен.
- •6.5.4. Катионирование воды.
- •6.5.5. Анионироваиие воды.
- •6.5.6. Химическое обессоливание воды.
- •7.1. Общие понятия круговорота воды
- •7.2. Интенсивность влагооборота
- •7. 3 Типы влагооборота
- •7.3.1. Геокосмический влагооборот
- •7.3.2.Атмосферно-океанический влагооборот
- •7.3.4. Атмосферио-литосферно-биологический
- •7.4. Водные ресурсы
- •7.5 Движение воды в водных объектах
- •7.6 Понятие о водном балансе
- •7.7 Водный баланс земного шара
- •7.8. Пресные воды
- •7.9. Мировой водный баланс
- •7.10. Активность водообмена
- •7.11 Тепловой баланс водных объектов
- •8.1 Виды ледников
- •8.3 Ледниковые трещины
- •8.7 Характеристики современных ледников
- •8.8 Современное оледенение на территории России
- •8.9 Ледниковое влияние на жизнь.
- •9.1 Классификация морских льдов
- •9.2 Условия образования и существования морских льдов
- •9.3 Ледниковый период и морские льды
- •9.4 Структура и свойства морского льда
- •10.1 Водно-физические свойства горных пород и почв
- •10.3 Поле сил в порах
- •10.4 Виды воды в порах
- •10.5 Возникновение и распространение подземных вод
- •10.6 Грунтовые и межпластовые напорные воды
- •10.7 Движение подземных вод
- •10.8 Передвижение воды в водоносных горизонтах
- •10.9 Формула Дарси
- •10.10 Режим подземных и поверхностных вод
- •10.11 Режим грунтовых и межпластовых вод
- •11.1 Основные понятия
- •11.2 Классификация Хортона
- •11.3 Морфологические характеристики бассейна
- •Лекция 12 Речной сток и его составляющие
- •12.1 Водный баланс бассейна реки
- •12.2 Питание рек
- •12.3 Русловые процессы
- •13.1 Классификация озер
- •13.2 Элементы озерного ложа:
- •13.3 Морфометрические характеристики озера.
- •Лекция 14. Водный баланс озер
- •14.1 Термический режим озер
- •14.2 Химический состав озерной воды
- •14.3 Биологические процессы озер
- •14.4 Озерные отложения
- •Контрольные вопросы:
- •15.1 История создания водохранилищ
- •15.2 Размещение водохранилищ на земном шаре
- •15.3 Классификация по морфологии ложа
- •15.4 Классификация по способу заполнения водой
- •15.5 Классификация по географическому положению
- •15.6 Классификация по характеру регулирования стока
- •15.7 Водный баланс
- •15.8 Колебания уровня воды
- •15.9 Течения
- •15.10 Волны
- •15.11 Ледовый режим водохранилищ
- •15.12 Гидрохимические особенности
- •15.13 Гидробиологические особенности
- •15.14 Заиление водохранилищ
- •15.15 Формирование берегов
- •15.16 Роль водохранилищ для человека
- •15.17 Особенности водного баланса водохранилищ
- •Контрольные вопросы:
- •16.1 Происхождение болот
- •16.2 Строение болот
- •16.3 Классификация болот
- •16.4 Функции болот
- •16.5 Болотная гидрографическая сеть
- •16.6 Гидрологический режим и водный баланс болот
- •16.7 Влияние осушительных мероприятий
- •16.8 Движение воды в торфяном грунте
- •16.9 Водный баланс болот
- •17.1 Геологические аспекты
- •17.2 Геоморфология
- •17.3 Гидрогеологические и гидрологические условия
- •17.4 Режим промерзания болота.
- •17.5 Рациональное использование Васюганского болота
- •Контрольные вопросы:
- •18.1 Основные элементы рельефа:
- •18.2 Водный баланс морей и океанов
- •18.4 Полезные ископаемые
- •18.7 Уязвимые звенья экологической системы Мирового Океана.
- •18.8 Антропогенное воздействие на океан
- •18.9 Нефть и нефтепродукты.
- •18.10Тепловое загрязнение водных ресурсов.
- •18.11 Радиоактивное загрязнение и ядовитые вещества
- •18.12 Минеральное, органическое, бактериальное и биологическое загрязнения Мирового океана.
- •18.13 Синтетические поверхностно-активные вещества.
- •18.14 Пестициды.
- •18.15 Водоросли.
- •18.16 Тяжелые металлы.
- •18.17 Самоочищение океана.
- •18.18 Меры борьбы с загрязнением.
4.6 Органическое вещество
Органическое вещество присутствует в коллоидном, растворенном и взвешенном состояниях с концентрацией 2-5 г на литр в морской воде и до 50 мг на литр в речной с болотным питанием воде. .
Источники поступления органических веществ в воду – внутри водоемные процессы их продуцирования и трансформации, атмосферные осадки, поверхностные и подземные стоки, другие водоемы, промышленные и хозяйственно-бытовые стоки.
Контрольные вопросы:
Уровень концентрации органического вещества в воде?
Какие биогенные компоненты входят в состав воды?
Какие ионы возникают в воде?
Газовый состав воды?
Уровень минерализации соленых и пресных вод?
Что означает электропроводность воды воды?
ЛЕКЦИЯ 5 Агрегатные состояния воды и фазовые переходы.
Состояния воды.
Вода может находиться в трех агрегатных состояниях, или фазах,— твердом (лед), жидком (собственно вода), газообразном (водяной пар). Очень важно, что при реально существующих на Земле диапазонах атмосферного давления и температуры вода может находиться одновременно в разных агрегатных состояниях. В этом отношении вода существенно отличается от других физических веществ, находящихся в естественных условиях преимущественно либо в твердом (минералы, металлы), либо в газообразном (О2, N2, СО2 и т.д.) состоянии.
Изменения агрегатного состояния вещества называют фазовыми переходами. В этих случаях свойства вещества (например, плотность) скачкообразно изменяются. Фазовые переходы сопровождаются выделением или поглощением энергии, называемой теплотой фазового перехода («скрытой теплотой»).
Зависимость агрегатного состояния воды от давления и температуры выражается диаграммой состояния воды, или фазовой диаграммой (рис. 5.1.1.).
Кривая ВВ'О на рис 5.1.1. носит название кривой плавления. При переходе через эту кривую слева направо происходит плавление
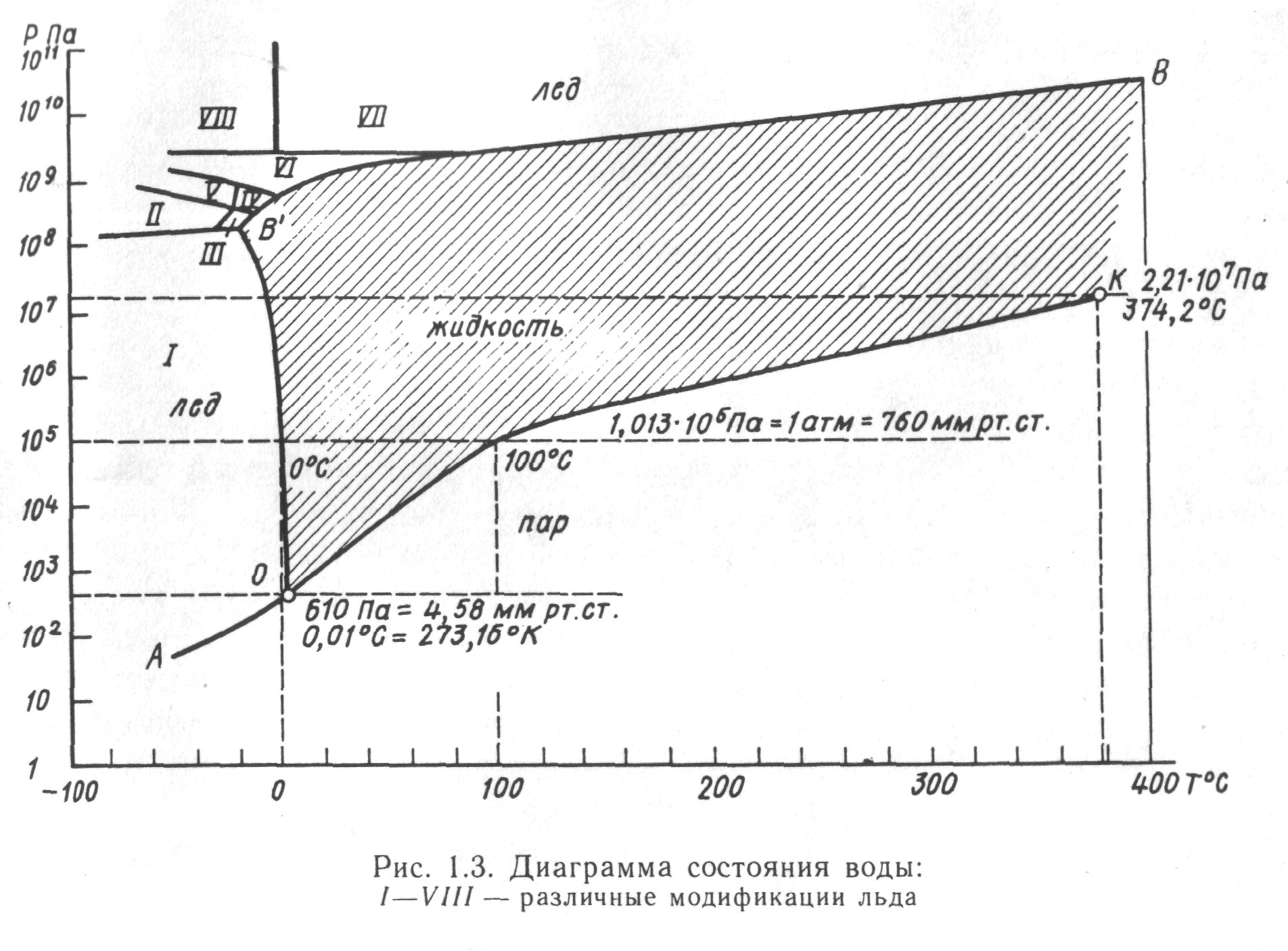
Рис. 5.1.1. Диаграмма состояния воды
I – VIII - различные модификации льда
льда, а справа налево — ледообразование (кристаллизация воды). Кривая ОК называется кривой парообразования. При переходе через эту кривую слева направо наблюдается кипение воды, а справа налево — конденсация водяного пара. Кривая АО носит название кривой сублимации, или кривой возгонки. При пересечении ее слева направо происходит испарение льда (возгонка), а справа налево — конденсация в твердую фазу (или сублимация).
В точке О (так называемой тройной точке, при давлении 610 Па и температуре 0,01° С или 273,16 К) вода одновременно находится во всех трех агрегатных состояниях.
Температура, при которой происходит плавление льда (или кристаллизация воды), называется температурой или точкой плавления Тпл. Эту температуру можно называть также температурой или точкой замерзания Тзам.
С поверхности воды, а также льда и снега постоянно отрывается и уносится в воздух некоторое количество молекул, образующих молекулы водяного пара. Одновременно с этим часть молекул водяного пара возвращается обратно на поверхность воды, снега и льда. Если преобладает первый процесс, то идет испарение воды, если второй — конденсация водяного пара. Регулятором направленности и интенсивности этих процессов служит дефицит влажности — разность упругости водяного пара, насыщающего пространство при данных давлении воздуха и температуре поверхности воды (снега, льда), и упругости фактически содержащегося в воздухе водяного пара, т.е. абсолютной влажности воздуха. Содержание в воздухе насыщенного водяного пара и его упругость увеличиваются с ростом температуры (при нормальном давлении) следующим образом. При температуре О°С содержание и упругость насыщенного водяного пара равны соответственно 4,856 г/м3 и 6,1078 гПа, при температуре 20°С — 30,380 г/м3 и 23,373 гПа, при 40°С — 51,127 г/м3 и 73,777 гПа.
Испарение с поверхности воды (льда, снега), а также влажной почвы идет при любой температуре и тем интенсивнее, чем больше дефицит влажности. С ростом температуры упругость водяного пара, насыщающего пространство, растет, и испарение ускоряется. К увеличению испарения приводит и возрастание скорости движения воздуха над испаряющей поверхностью (т.е. скорости ветра в природных условиях), усиливающее интенсивность вертикального массо- и теплообмена.
Когда интенсивное испарение охватывает не только свободную поверхность воды, но и ее толщу, где испарение идет с внутренней поверхности образующихся при этом пузырьков, начинается процесс кипения. Температура, при которой давление насыщенного водяного пара равно внешнему давлению, называется температурой или точкой кипения Tкип.
При нормальном атмосферном давлении (1,013•105 Па = 1,013 бар = 1 атм = 760 мм рт. ст.) точки замерзания воды (плавления льда) и кипения (конденсации) соответствуют по шкале Цельсия 0 и 100°.
Температура замерзания Тзам и температура кипения воды Ткип зависят от давления (см. рис. 3.9.2.). В диапазоне изменения давления от 610 до 1,013•105 Па (или 1 атм) температура замерзания немного понижается (от 0,01 до 0° С), затем при росте давления приблизительно до 6•107 Па (600 атм) Тзам падает до —5° С, при увеличении давления до 2,2•108 Па (2 200 атм) Тзам уменьшается до —22° С. При дальнейшем увеличении давления Тзам начинает быстро возрастать. При очень большом давлении образуются особые «модификации» льда (II—VIII), отличающиеся по своим свойствам от обычного льда (льда I).
При реальном атмосферном давлении на Земле пресная вода замерзает при температуре около 0° С. На максимальных глубинах в океане (около 11 км) давление превышает 108 Па, или 1 000 атм (увеличение глубины на каждые 10 м увеличивает давление приблизительно на 105 Па, или 1 атм). При таком давлении температура замерзания пресной воды была бы около —12° С.
На снижение температуры замерзания воды
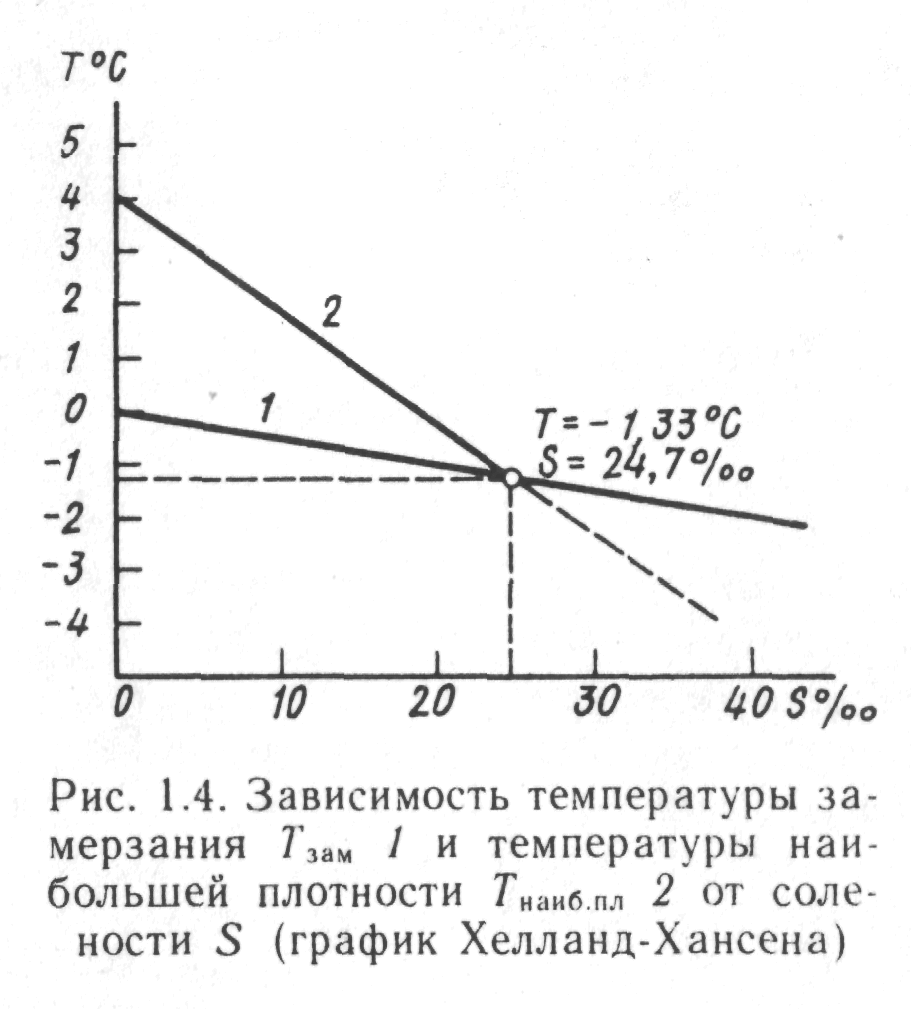
Рис. 5.1.2.
оказывает влияние ее соленость.
1.4). Увеличение солености на каждые 10‰ снижает Тзам приблизительно на 0,54° С:
Тзам = -0,054 S.
Температура кипения с уменьшением давления снижается (см. рис. 3.9.2.). Поэтому на больших высотах в горах вода кипит при температуре ниже, чем 100° С. При росте давления Ткип возрастает до так называемой «критической точки», когда при р = 2,2 • 107 Па и Ткип = 374° С вода одновременно имеет свойства и жидкости и газа.
Диаграмма состояния воды иллюстрирует две «аномалии» воды, оказывающие решающее влияние не только на «поведение» воды на Земле, но и на природные условия планеты в целом. По сравнению с веществами, представляющими собой соединения водорода с элементами, находящимися в Периодической таблице Менделеева в одном ряду с кислородом,— теллуром Те, селеном Se и серой S, температура замерзания и кипения воды необычно высока. Учитывая закономерную связь температуры замерзания и кипения с массовым числом упомянутых веществ, следовало бы ожидать у воды значения температуры замерзания около —90° С, а температуры кипения около —70° С. Аномально высокие значения температуры замерзания и кипения предопределяют возможность существования воды на планете как в твердом, так и в жидком состоянии и служат определяющими условиями основных гидрологических и других природных процессов на Земле.
