
- •Міністерство охорони здоров’я України
- •Контрольні завдання
- •Сучасна номенклатура неорганічних сполук і їх взаємні перетворення. Стехіометричні розрахунки
- •Приклади розв'язування задач
- •Контрольні питання
- •Будова атомів та періодичний закон д.І. Менделєєва
- •Приклади розв'язування задач
- •Контрольні питання
- •Хімічний зв'язок і будова молекул. Конденсований стан речовини
- •Приклади розв'язування задач
- •Контрольні питання
- •Основні закономірності протікання хімічних реакцій. Елементи хімічної термодинаміки і термохімії
- •Приклади розв'язування задач
- •Стандартні ентальпії утворення δн0298, ентропії s0298 і енергії Гіббса δg0298 деяких речовин при 298 к (25°с).
- •Контрольні питання
- •Хімічна кінетика і рівновага
- •Приклади розв’язування задач
- •Контрольні питання
- •Розчини. Коцентрація розчинів
- •Приклади розв’язування задач
- •Контрольні питання
- •Властивості розчинів
- •Контрольні питання
- •Окислювально-відновні реакції. Електрохімічні процеси
- •Слід пам’ятати, що:
- •Правила підбору коефіцієнтів у окислювально-відновних реакціях.
- •Приклади розв’язування задач
- •Контрольні питання
- •Гідроліз солей. Відновний показник (рН)
- •Приклади розв'язування задач
- •Контрольні питання
- •Додаток № 1
- •Константи дисоціації деяких слабких електролітів у водних розчинах при 25°с.
- •Додаток № 2
- •Стандарті електродні потенціали деяких металів у водних розчинах.
- •Література
- •69035, Г. Запорожье, пр. Маяковского, 26
Приклади розв'язування задач
Приклад 1. Визначити еквіваленти (Е) та еквівалентні маси хлору, кисню і азоту у сполуках НСІ, H2О і NH3.
Розв'язування. Маса і кількість речовини — це не ідентичні поняття, оскільки маса речовини виражається у кілограмах (грамах), а кількість речовини — у молях.
Хімічним еквівалентом елементу називається така його кількість у молях, яка сполучається з одним молем атомів водню або заміщує таку саму кількість атомів водню у хімічних реакціях.
Еквівалентною масою називається маса одного еквівалента елементу (речовини). Таким чином, еквіваленти виражають у молях, а еквівалентні маси — у г/моль.
У наведених сполуках з одним молем атомів водню сполучається один моль атомів хлору, 1/2 моль атомів кисню і 1/3 моль атомів азоту. Таким чином, згідно з визначенням, еквівалент хлору, кисню та азоту дорівнюють відповідно 1 моль, 1/2 моль та 1/3 моль, тоді як їх еквівалентні маси: т(Сl)=35,45 г/моль, т(0)=16/2=8 г/моль, ГП(М)= 14/3=4,67 г/моль.
Приклад 2. Із 3,85 г нітрату металу одержано 1,60 г його гідроксиду. Обчислити еквівалентну масу металу mе.
Розв'язування. При розв'язуванні задачі потрібно мати на увазі, що:
а) еквівалентна маса гідроксиду дорівнює сумі еквівалентних мас металу та гідроксильної групи;
б) еквівалентна маса солі дорівнює сумі еквівалентних мас металу та кислотного залишку.
Еквівалентну масу будь-якої зарядженої частинки можна визначити, поділивши молекулярну масу на заряд. Наприклад:
me(NO3-) =62/1=62 г/моль, me(SO42-) =96/2=48 г/моль.
Тобто, за законом еквівалентів:
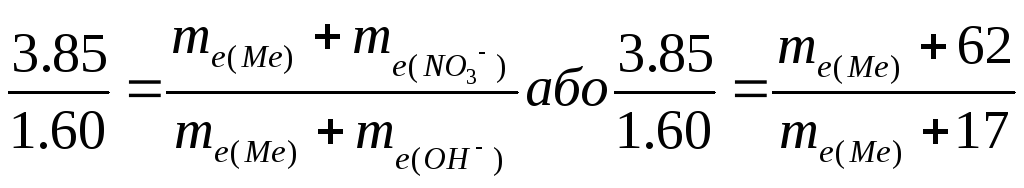
звідки me(Me) = 15 г/моль.
Приклад 3. Скільки грамів металу, еквівалентна маса якого 12,16 г/моль, взаємодіє з 310 мл кисню (н.у.)?
Розв'язування: Об'єм еквівалентної маси кисню (8 г/моль) дорівнюватиме:
![]() або
5600 мл.
або
5600 мл.
Приклад 4. На нейтралізацію 0,943 r фосфітної кислоти витрачено 1,288 г КОН. Обчислити еквівалент, еквівалентну масу і основність кислоти. На підставі розрахунку написати рівняння реакції.
Розв'язування: Еквівалентна маса КОН дорівнює його молярній масі – 56 г/моль. За законом еквівалентів:
![]() звідки
звідки
![]()
Молярна маса Н3РО3 дорівнює 82 г/моль. Тобто, еквівалент H3PO3 дорівнюватиме 41/82=0,5 моль; а її основність n дорівнює 2, таким чином, n=M/me. Отже, при взаємодії з КОН заміщується два атоми водню:
Н3РО3 + 2КОН = К2НРО3 + 2Н2О.
Приклад 5. При прожарюванні суміші ZnCO3 і ZnO масою 1,6 г добуто 1,248 г цинк оксиду. Який склад мала вихідна суміш (у масових частках)?
Розв'язування: а) Рівняння реакції розкладу:
ZnCO3 = ZnO + СО2
125 81 44
Як видно із рівняння реакції, 1 моль ZnCO3 (125 г/моль) втрачає 1 моль СO2 (44 г/моль). Різниця в масі за умовою задачі складає: 1,6 – 1,248=0,352 г.
Звідси:
125г ZnCО3 — 44г СО2
х — 0,352г СО2,
![]() г
ZnCO3
г
ZnCO3
![]()
![]() .
.
б) Виразимо масу ZnСО3 у суміші через х (г), тоді маси ZnO складе (1,6-х) г. Знайдемо масу ZnO, що утворюється при прожарюванні ZnCO3 масою х г:
із 125г ZnCO3 добувають 81г ZnO
х — У,
![]() (г)
(г)
За умовою задачі: 0,648х +(1,6 – х)= 1,248 г.
Звідси 1,6 – 1,248 = х – 0,648х, тоді 0,352 = 0,352х, х = 1 г, тобто маса ZnCO3 у суміші дорівнює 1 г, або:
![]()
![]()
