
Докумвчпчент Microsoft Word
.docx
|
Вариант |
Уравнение реакции |
Т1 |
Т2 |
Т3 |
Ра |
|
42 |
2CS = C(s) + CS2 |
1600 |
2600 |
2500 |
0,5 |
-
Расчет
 ,
,
 ,
СР
(a,
b,
c)
химической реакции по таблицам
стандартных термодинамических величин:
,
СР
(a,
b,
c)
химической реакции по таблицам
стандартных термодинамических величин:
|
|
H°(298) |
S°(298) |
a |
b |
c |
|
CS |
|
210,45 |
49,76 |
0,00204 |
|
|
CS2 |
116700 |
237,77 |
52,09 |
0,00669 |
|
|
C(s) |
|
5,74 |
16,86 |
0,00477 |
|
|
Δa |
Δb |
Δc |
ΔH°(298) |
ΔS°(298) |
|||
|
1,55 |
0,00738 |
-693000 |
-442860 |
-177,39 |
|||
|
Cp = Δa + Δb * T + Δc * T^(-2) |
||
|
Cp(298) |
-4,05 |
|
-
Результаты приближенного расчета термодинамических функций
 ,
,
 ,
,
 и ln(KP)
в интервале температур Т1
Т2
при следующих приближениях:
и ln(KP)
в интервале температур Т1
Т2
при следующих приближениях:
|
T |
Значение |
|
T1 |
1600 |
|
T2 |
1700 |
|
T3 |
1800 |
|
T4 |
1900 |
|
T5 |
2000 |
|
T6 |
2100 |
|
T7 |
2200 |
|
T8 |
2300 |
|
T9 |
2400 |
|
T10 |
2500 |
|
T11 |
2600 |
а) При Ср=0
|
При Ср=0 |
|||
|
H(T) |
S(T) |
G(T)=H(T)-TS(T) |
Ln(Kp)=G(T)/(R*T) |
|
-442850 |
-117,39 |
-159036 |
11,96 |
|
-141297 |
10,00 |
||
|
-123558 |
8,26 |
||
|
-105819 |
6,70 |
||
|
-88080 |
5,30 |
||
|
-70341 |
4,03 |
||
|
-52602 |
2,88 |
||
|
-34863 |
1,82 |
||
|
-17124 |
0,86 |
||
|
615 |
-0,03 |
||
|
18354 |
-0,85 |
||
б) При Ср=Ср(298)=const
|
При Ср=Ср(298)=const |
|||
|
H(T)=dH(298)+Cp*(T-298) |
S(T)=dS(298)+Cp*ln(T/298) |
G(T)=H(T)-TS(T) |
Ln(Kp)=G(T)/(R*T) |
|
-448139 |
-184,20 |
-153412 |
11,54 |
|
-448544 |
-184,45 |
-134979 |
9,55 |
|
-448950 |
-184,68 |
-116523 |
7,79 |
|
-449355 |
-184,90 |
-98043 |
6,21 |
|
-449761 |
-185,11 |
-79543 |
4,79 |
|
-450166 |
-185,31 |
-61022 |
3,50 |
|
-450572 |
-185,50 |
-42482 |
2,32 |
|
-450977 |
-185,68 |
-23923 |
1,25 |
|
-451382 |
-185,85 |
-5347 |
0,27 |
|
-451788 |
-186,01 |
13246 |
-0,64 |
|
-452193 |
-186,17 |
31856 |
-1,47 |
-
Результаты точных расчетов в интервале температур Т1 Т2:
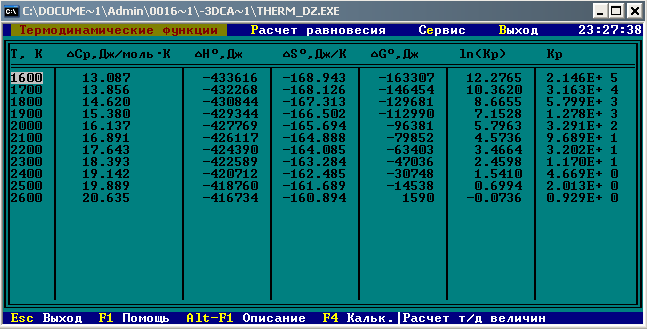
-
Графики температурной зависимости термодинамических функций СР,
 ,
,
 ,
,
 и ln
KP
для всех вариантов расчета:
и ln
KP
для всех вариантов расчета:





-
Результаты расчета равновесных составов: числа молей, мольные доли, мольные и массовые проценты, при заданных Т3 и Р для случаев, когда реагируют стехиометрические смеси:
а) исходных веществ
|
Реакция |
2CS |
=C(s) |
+ CS2 |
|
Кол-во молей до: |
2 |
- |
0 |
|
Кол-во молей после: |
2-2z |
- |
z |
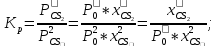




Z=0,5554

 =12+32*2=76
=12+32*2=76


Равновесный состав:
|
|
SO2 |
O2 |
|
Количество молей |
0,8892 |
0,5554 |
|
Мольная доля |
0,615 |
0,384 |
|
Мольный процент |
61,5% |
38,4% |
|
Массовый процент |
48,1% |
51,89% |
б) всех веществ
|
Реакция |
2CS |
=C(s) |
+ CS2 |
|
Кол-во молей до: |
2 |
- |
1 |
|
Кол-во молей после: |
2-2z |
- |
1+z |





Z=0,1109

 =12+32*2=76
=12+32*2=76


Равновесный состав:
|
|
CS |
|
|
Количество молей |
1,7782 |
1,1109 |
|
Мольная доля |
0,615 |
0,384 |
|
Мольный процент |
61,5% |
38,4% |
|
Массовый процент |
48,09% |
51,9% |

-
Исследование вопроса о направление реакции при температуре Т3 и Р, если в исходный момент времени взято по одному молю каждого исходного вещества и по два моля продукта реакции:
|
Реакция |
2CS |
=C(s) |
+ CS2 |
|
Кол-во молей до: |
1 |
- |
2 |
|
Nобщ=3 |
|||
|
xi |
1/3 |
- |
2/3 |
|
Pi |
P*1/3 |
- |
P*2/3 |


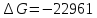
Так как
 то реакция идет слева направо, в сторону
получения продуктов реакции.
то реакция идет слева направо, в сторону
получения продуктов реакции.
Зависимость от Температуры:

ΔH°=-442860
При увеличении Т равновесие двигается влево, выход реакции падает
Зависимость от давления:
Так как
 , Δn=-1,
то при увеличении давления реакция
сдвигается в сторону исходных веществ
(влево).
, Δn=-1,
то при увеличении давления реакция
сдвигается в сторону исходных веществ
(влево).
8)
2CS = C(s) + CS2
-
1 -418760
Z X
Z=0,5554
X=0,5554*(-418760)=-232579
⧋H=-23257
b) 1 -418760
1-Z X
Z=0,1109
X=(1-0,1109)(-418760)=-372319
⧋H=-372319
9)

|
Реакция |
2CS |
=C(s) |
+ CS2 |
|
Кол-во молей до: |
2 |
- |
0 |
|
Кол-во молей после: |
2-2z |
- |
z |













Домашняя работа по
Химической термодинамике
Выполнил: студент группы
МПП-11-1 / П4-11-2
Яловенко Дмитрий

