
- •Содержание
- •Введение
- •1 Основные понятия и законы химии
- •1.1 Основные понятия химии
- •1.2 Основные законы химии
- •2 Основные классы неорганических соединений
- •2.1 Простые вещества
- •2.2 Сложные вещества
- •3 Растворы
- •3.1 Общие свойства растворов
- •3.1.2 Способы выражения состава растворов
- •3.1.3 Физико-химические процессы образования растворов
- •3.1.4 Экстракция
- •3.2 Растворы неэлектролитов
- •3.2.1 Законы Рауля
- •3.2.2 Осмос
- •3.3 Растворы электролитов
- •3.3.1 Электролитическая диссоциация
- •3.3.2 Сильные и слабые электролиты
- •3.4 PH водных растворов
- •4 Ионно-обменные реакции
- •4.1 Необратимые ионно-обменные реакции
- •4.2 Обратимые ионно-обменные реакции
- •5 Гидролиз солей
- •5.1 Различные случаи гидролиза
- •2) Гидролиз соли образованной сильным основанием и слабой кислотой
- •3) Гидролиз соли образованной слабым основанием и слабой кислотой
- •5.2 Константа гидролиза
- •5.3 Смещение равновесия при гидролизе
- •6. Окислительно-восстановительные реакции
- •6.1 Составление уравнений окислительно-восстановительных реакций
- •6.2 Прогнозирование окислительно-восстановительных свойств веществ по степеням окисления элементов
- •6.3 Основные типы окислительно-восстановительных реакций
- •6.4 Взаимодействие металлов с водой, кислотами и щелочами
- •7 Гальванические элементы
- •7.1 Принцип работы гальванического элемента
- •7.2 Водородный электрод сравнения. Электрохимический ряд
- •8 Электролиз
- •8.1 Электролиз расплавов
- •8.2 Электролиз водных растворов
- •8.3 Количественные расчёты в электролизе
- •8.4 Химические источники электрической энергии
- •9 Коррозия металлов
- •9.1 Виды и типы коррозии
- •9.2 Способы защиты металлов от коррозии
- •9.2.1 Изолирование металлов от внешней среды
- •9.2.2 Изменение состава коррозионной среды
- •9.2.3 Рациональное конструирование
- •9.2.4 Электрохимические способы защиты от коррозии
- •10 Термодинамика
- •10.1 Внутренняя энергия и энтальпия. Закон Гесса
- •Или через промежуточный продукт (со) в две реакции:
- •10.2 Энтропия
- •10.3 Энергия Гиббса
- •11 Химическая кинетика Химическая кинетика – учение о скоростях и механизмах протекания химических реакций.
- •11.1 Скорость реакции
- •Основные факторы, влияющие на скорость реакции:
- •Число частиц с энергией большей, чем Еа равно заштрихованной площади.
- •12.1.2 Модель атома по Бору
- •12.2 Современные представления о строении атома
- •13 Периодический закон и периодическая таблица д.И. Менделеева
- •14 Химическая связь и строение молекул
- •14.1 Химическая связь
- •14.1.1 Квантово-механическое описание модели молекулы водорода
- •14.1.2 Основные характеристики химической связи
- •Валентный угол–это угол между двумя химическими связями.Он отражает геометрию молекулы.
- •14.1.3 Типы химических связей Ковалентная связь –это связь между двумя атомами за счет образования общей электронной пары.
- •14.2 Состав и строение молекул
- •15 Типы кристаллических решеток
- •16.1 Общая характеристика s-элементов первой и второй групп
- •16.2 Свойства воды
- •16.2.1 Строение молекулы воды
- •16.2.2 Физические свойства воды
- •16.2.3 Химические свойства воды
- •16.3 Жесткость воды
- •18 Комплексные соединения
- •18.1 Состав комплексных соединений
- •18.2 Реакции с участием комплексных соединений
- •19.8.1 Элементы триады железа
- •19.8.2 Платиновые металлы
- •20 Органические соединения
- •20.1 Углеводороды
- •20.2 Кислородсодержащие соединения
- •20.3 Амины и аминокислоты
- •21 Полимеры
- •21.1 Классификации полимеров
- •21.2 Полимеризационные полимеры
- •21.3 Поликонденсационные полимеры
- •21.4 Структура и состояние полимеров
- •22 Рабочие вещества низкотемпературной техники
- •22.2 Хладагенты органического происхождения
- •Список использованных источников
14 Химическая связь и строение молекул
После изучения строения атома следующим этапом в изучении строения вещества стало исследование природы химической связи. Так как основным принципом самопроизвольного протекания процессов в природе является «принцип энергетического минимума», поэтому необходимым условием образования химической связи является уменьшение энергии системы при переходе от отдельных атомов к молекуле.
14.1 Химическая связь
14.1.1 Квантово-механическое описание модели молекулы водорода
В 1927 г. Гайтлер и Лондон выполнили квантово-механический расчет изменения энергии при сближении двух атомов водорода, в зависимости от расстояния между атомами. Результаты приведены на рисунках 14.1и 14.2.
|
|
Рисунок 14.1 – Энергетическая диаграмма образования молекулы водорода из атомов водорода: 1 – экспериментальные данные, 2, 3 – расчетные данные; 1, 2 – противоположные спины, 3 – параллельные спины. |
Из рисунка 14.1 видно, что по мере сближения атомов с параллельными спинами (кривая 3) энергия системы резко возрастает, то есть химическая связь не образуется. Если спины атомов антипараллельны (противоположны по знаку), то с уменьшением расстояния между атомами энергия системы вначале уменьшается (участок a – b), проходя через некий минимум (точка b), а затем увеличивается (участок b – c). Следовательно, образование химической связи возможно, если спины атомов антипараллельны.

Рисунок 14.2 – Геометрическая модель молекулы водорода
Из рисунка 14.2 видно, что расстояние между центрами атомов в молекуле меньше суммы радиусов двух атомов, т.е. происходит взаимное перекрывание электронных облаков. Область перекрытия имеет избыточный отрицательный заряд и электростатически взаимодействует с ядрами обоих атомов, что обеспечивает между ними химическую связь.
Расчет энергии системы из трех атомов водорода не приводит к уменьшению энергии, т.е. химическая связь является двухэлектронной и имеет электрическую природу.
На основании полученных данных был предложен механизм образования химической связи, называемый «метод валентных связей».
1 Химическая связь является двухэлектронной. Электроны, участвующие в образовании химической связи, имеют противоположные спины и образуют общую электронную пару.
2 Различают обменный и донорно-акцепторный механизмы образования химической связи:
а) обменный – химическая связь образуется в результате перекрывания пары орбиталей, на каждой из которых было по одному электрону с противоположными спинами. Например, образование молекул водорода и хлороводорода:

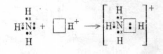
б) донорно-акцепторный – химическая связь образуется в результате перекрывания пары орбиталей, на одной из которых имелась электронная пара, а на второй – свободная орбиталь без электронов. Атом, предоставивший орбиталь с электронной парой, называют донором, а атом, предоставивший свободную орбиталь, – акцептором. Например, взаимодействие аммиака с ионом водорода с образованием катиона аммония:
По способу перекрывания электронных облаков различают σ- и π- связи:
1) σ-связь образуется за счёт перекрывания электронных облаков по прямой линии, соединяющей центры взаимодействующих атомов;
2) π -связь образуется за счёт перекрывания электронных облаков выше и ниже линии, соединяющей центры взаимодействующих атомов. Она образуется в основном при перекрывании р-орбиталей. π-связь является значительно менее прочной, чем σ-связь.
Количество химических связей определяется валентностями элементов. Валентность элемента равна числу орбиталей, принимающих участие в образовании химических связей.

