Лекция 3. Галогены. Оксиды и кислоты
.docЛекция 3. Кислородные соединения галогенов
-
Оксиды галогенов.
-
Кислородсодержащие кислоты галогенов.
-
Применение галогенов и их соединений.
1. Оксиды галогенов
Галогены образуют ряд соединений с кислородом. Но эти соединения неустойчивы, ∆Go >0, они легко взрываются при нагревании и в присутствии органических соединений. Их получают только косвенным путем.
Относительно устойчивы следующие кислородные соединения галогенов:
|
Свойства |
OF2 |
Cl2O |
ClO2 |
Cl2O6 |
Cl2O7 |
I2O5 |
|
Внешний вид при н.у. |
Желтый газ |
Желто-коричн. газ. Ядовит |
Желто-зелен. газ. Ядовит |
Темно-красная жидкость |
Бесцветная жидкость. Взрывоопасна |
Бесцв. крист. вещество |
|
Темп. пл., оС |
-223,8 |
-116 |
-59 |
3,5 |
-90 (устойчивее остальных оксидов) |
Разл. при t>350 oC |
|
∆Go, кДж/моль |
+42,5 |
93,40 |
122,3 |
|
|
- |
|
Строение молекул |
|
|
|
|
|
|
|
|
→ Усиление окислительной активности → |
|||||
Также известны Cl2O3, Br2O3, BrO2, Br2O5, I2O4, I2O6.
Получение.
OF2 (оксид фтора, или правильнее – фторид кислорода) – сильнейший окислитель. Его получают действием F2 на охлажденный разбавленный раствор щелочи:

Оксиды хлора и йода можно получить по реакциям:
![]()
![]()
![]()

Химические свойства:
-
Термически неустойчивы:

-
Все соединения галогенов с кислородом (кроме OF2) – кислотные оксиды.
Cl2O, Cl2O7, I2O5 при взаимодействии с водой образуют кислоты:
![]()
![]()
ClO2, Cl2O6 (С.О.=+4, +6 – неустойчивы) при взаимодействии с водой диспропорционируют:
![]() ,
,

-
Оксиды галогенов – окислители:

OF2 содержит O+2 – очень сильный окислитель:
![]()
-
Оксиды с промежуточной степени окисления галогена диспропорционируют:
![]()
![]() .
.
-
Кислородсодержащие кислоты галогенов
Все кислородсодержащие кислоты галогенов хорошо растворимы в воде. HClO4, HIO3 и H5IO6 известны в свободном виде, остальные нестойки, существуют только в разбавленный водных растворах. Наиболее стабильны соединения в С.О. -1 и +5.
|
С.О. |
Формула |
Внешний вид |
Кисл.-осн. свойства |
К |
Названия кислот |
Названия солей |
|
+1 |
HOF HOCl HOBr HOI |
Существуют только в растворе |
Слабые кислоты Амфотерное соед. |
5∙10-8 2∙10-9 2∙10-10 |
Фторноватистая Хлорноватистая Бромноватистая Иодноватистая |
Гипофториты Гипохлориты Гипобромиты Гипоиодиты |
|
+3 |
HClO2 |
-ʺ- |
Кислота средн. силы |
1,1∙10-2 |
Хлористая |
Хлориты |
|
+5 |
HClO3 HBrO3 HIO3 |
-ʺ- -ʺ- Бесцв. кристаллы |
Сильные кислоты |
10 0,2 0,15 |
Хлорноватая Бромноватая Иодноватая |
Хлораты Броматы Иодаты |
|
+7 |
HClO4 (HBrO4) H5IO6 |
Бесцв. жидкость
Бесцв. кристаллы |
Самая сильная кислота
Слабая кислота |
1010
5∙10-4 |
Хлорная Бромная Ортоодная |
Перхлораты Перброматы Периодаты |
Сравнение силы кислот
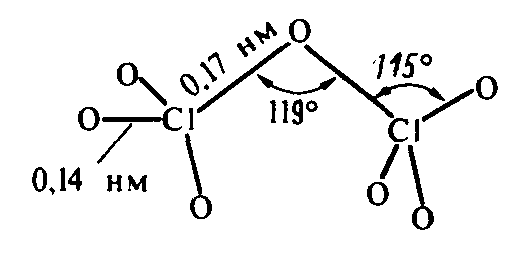
Строение кислородных кислот хлора:

Изменение свойств в ряду кислородных кислот хлора можно показать схемой:

Эта закономерность характерна не только для хлора, но и для брома и иода.
При возрастании степени окисления галогена увеличивается заряд иона, это усиливает притяжение его к O2-, и затрудняет диссоциацию по типу основания. Вместе с этим увеличивается отталкивание положительный ионов H+ и Эn+, это облегчает диссоциацию по типу кислоты.

Рис. 1. Схема фрагмента молекулы Э(ОН)n
HOCl – амфотерное соединение: может диссоциировать и по типу кислоты, и по типу основания:
![]()


![]()
В ряду ClO- - ClO2- - ClO3- - ClO4- увеличивается устойчивость кислот и анионов. Это объясняется увеличением числа электронов, принимающих участие в образовании связей:

Кратность связи =1 Кратность связи=1,5
d(Cl-O)=0,170 нм d(Cl-O)=0,145 нм
С увеличением количества атомов кислорода в кислотах, увеличивается экранирование Cl, поэтому окислительная способность палает.
Таким образом, в ряду НClO → НClO2 → НClO3 → HClO4
-
усиливается сила кислот;
-
увеличивается устойчивость кислот;
-
уменьшается окислительная способность.
Сила кислородсодержащих кислот в ряду HOCl-HOBr-HOI уменьшается из-за увеличения ковалентного радиуса и ослабления связи O-Hal:

Кд 5∙10-8 2∙10-9 2∙10-10
О кислительные
свойства уменьшаются
кислительные
свойства уменьшаются
В ряду HCO-HBrO-HIO увеличивается устойчивость кислот. Например, при нагревании или действии света они разлагаются:
![]() ,
∆Gо (кДж) HClO,
HBrO, HIO
,
∆Gо (кДж) HClO,
HBrO, HIO
-51,4 -5,2 54,5
Получение.
-
Фторноватистую кислоту получают при помощи реакций:
![]() .
(при н.у.)!!!
.
(при н.у.)!!!

Хлорноватистую кислоту получают гидролизом хлора (НСl удаляют действием СaCO3):
![]()
Равновесие устанавливается, когда прореагирует 30% хлора.
HClO и HBrO получают разложением гипохлоритов и гипобромитов:
![]() .
.
2. HClO2 получают из солей:
![]() .
.
3. HHalO3 получают:
- из солей:
![]()
- окислением галогенов сильными окислителями:
![]()
4. HClO4, H5IO6 из солей:
![]()
![]()
Химические свойства
-
Разлагаются при нагревании и на свету:

-
Сильные окислители (все кислоты - более сильные окислители, чем их соли):

Хлорная кислоты – слабый окислитель только в концентрированных растворах:
![]()
Соли оксокислот более устойчивы, чем кислоты. Их устойчивость растет с увеличением степени окисления.
Химические свойства солей:
1. Хлораты и перхлораты распадаются только при нагревании:

![]()
2. Они, как и кислоты, являются окислителями (но более слабыми, чем их кислоты):
![]()

Получение солей:
МеHalO получают пропусканием галогегенов через холодный раствор щелочи, соды, поташа:

МеHalO3 получают пропусканием галогенов через горячие (60-70 оС) растворы щелочей:
![]()
МеClO4 и Ме5IO6 окислением хлоратов и иодатов при электролизе или слабым нагреванием:

![]()
7. Применение
Фтор
Плавиковая кислота используется для травления стекла, удаления остатков песка с металлического литья, в химическом синтезе.
В ядерной промышленности применяют UF6.
В качестве хладагентов используют CF2Cl2.
В металлургии применяют CaF2.
Фторопроизводное этилена тетрафторэтилен в результате полимеризации дает ценный полимер – тефлон, устойчив к химическим реагентам и незаменим в производстве веществ особой чистоты, для изготовления аппаратуры.
Фторопроизводные материалы – в медицине, заменители кровеносных сосудов и сердечных клапанов. Изделия из фторопластов широко применяются в авиационной, электротехнической, атомной и др. отраслях.
Хлор
Хлор необходим для синтеза в органическом и полимерном синтезе. Методом хлорной металлургии получают кремний и тугоплавкие цветные металлы (титан, ниобий, тантал и др.).
Применяется как окислитель и для стерилизации питьевой воды.
Соляная кислота и галогениды используется в металлургической, текстильной и пищевой промышленности.
HClO применяется как бактерицидное и отбеливающее средство. Выделяющийся при растворении кислоты атомарный кислород обесцвечивает красители и убивает микробы:
![]() .
.
Жавелевая вода – это смесь хлорида и гипохлорита калия, ее получают действием щелочи на «хлорную воду», она обладает отбеливающими свойствами:
![]() .
.
Белильная или хлорная известь – белый порошок с резким запахом, применяется как отбеливающее и дезинфицирующее средство:
![]() .
.
Бром
Используется в органическом синтезе.
В фотографическом деле используется AgBr.
Соединения брома применяются для производства лекарств.
Иод
I2 необходим для металлургии, его применяют как антисептическое и дезинфицирующее средство. Йод замещает атомы водорода в молекулах белков микроорганизмов, что приводит к их гибели:
![]() .
.
Для деревообработки применяют KI.
Cоединения иода применяются для производства лекарств, в пищевых добавках (NaI), для синтеза и в химическом анализа (иодометрия).