
- •Глава 1. Галоидпроизводные углеводородов
- •Номенклатура алкилгалогенидов, алкенилгалогенидов, алкинилгалогенидов и арилгалогенидов
- •1. Получение алкилгалогенидов
- •1.1. Галогенирование алканов
- •1.2. Присоединение галогеноводородов к алкенам
- •1.3. Замещение гидроксильной группы на галоген.
- •1.4. Свойства Галоидпроизводных углеводородов
- •1.4.1. Реакции нуклеофильного замещения
- •1.4.2. Механизм sn1
- •Дифенилметилгалогенид Трифенилметилгалогенид
- •1.4.3. Механизм sn2
- •1.4.4. Реакции отщепления
- •1.4.5. Реакции алкилгалогенидов с металлами
- •Глава 2. Спирты
- •Номенклатура одноатомных спиртов
- •2.4. Синтез спиртов из карбонильных соединений с помощью магнийорганических соединений
- •2.5. Гидролиз алкилгалогенидов
- •2.6. Свойства одноатомных спиртов
- •Температуры кипения некоторых спиртов и изомерных им простых эфиров
- •Кислотно-основные свойства спиртов
- •Кислотность спиртов
- •Из этих данных следует, что равновесие в системе спирт – щелочь всегда смещено в сторону спирта, а не алкоголята:
- •Замещение гидроксильной группы на галоген. Получение алкилгалогенидов
- •Получение алкилгалогенидов из спирта и галогеноводородных кислот
- •Получение алкилгалогенидов из спиртов и галогенидов фосфора
- •Дегидратация спиртов
- •2.10. Образование простых эфиров из спиртов
- •2.11. Получение простых эфиров по Вильямсону
- •2.12. Окисление спиртов
- •Восстановление спиртов
- •Взаимодействие с щелочными и щелчноземельными металлами.
- •2.15. Двухатомные спирты
- •2.16. Получение диолов
- •2.17. Свойства диолов
- •2.21. Расщепление простых эфиров кислотами
- •Глава 3. Тиолы и сульфиды
- •3.1 Получение тиолов
- •3.2 Свойства тиолов
- •Решения некоторых тестовых задач по теме спирты и тиолы
- •Только в реакциях 3) и 4) используются третичные спирты. Поскольку стабильность третичного карбениевого иона бензильного типа выше, чем стабильность третичного карбениевого иона алкильного типа:
- •5. Какого алкена образуется меньше при дегидратации 3-метилгексанола-3?
- •Глава 4. Альдегиды и кетоны
- •Альдегиды классификация
- •Строение карбонильной группы
- •4.1. Реакционные центры в молекулах альдегидов и кетонов
- •4.2. Химические свойства альдегидов и кетонов
- •4.3. Реакции альдегидов и кетонов по механизму нуклеофильного присоединения (an)
- •4.4. Реакции нуклеофильного присоединения по карбонильной группе с последующим отщеплением воды.
- •4.5. Окисление альдегидов и кетонов.
- •4.6. Реакция Канниццаро -Тищенко
- •4.7. Реакции полимеризации.
- •Получение альдегидов и кетонов
- •4.9. Медико-биологическое значение соединений с карбонильной группой
- •Отдельные представители альдегидов и кетонов
- •Эталонное решение задач
Только в реакциях 3) и 4) используются третичные спирты. Поскольку стабильность третичного карбениевого иона бензильного типа выше, чем стабильность третичного карбениевого иона алкильного типа:
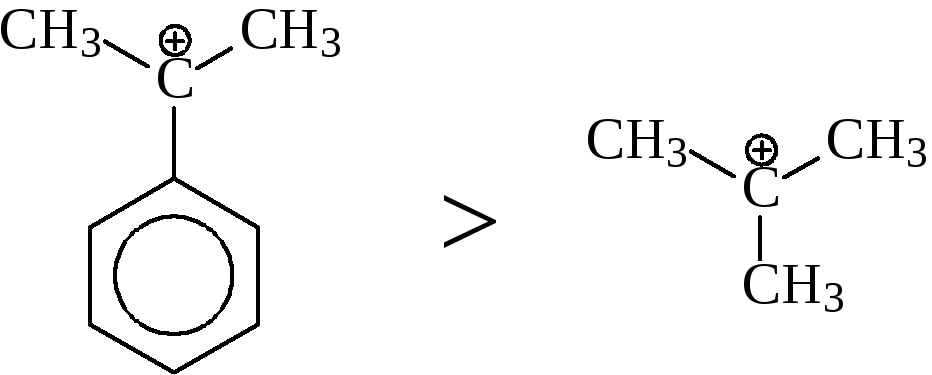
скорость замещения гидроксила на галоген будет максимальной для реакции 4).
3. При взаимодействии алкоголятов щелочных металлов с алкилгалогени- дами выход простого эфира максимален в реакции?
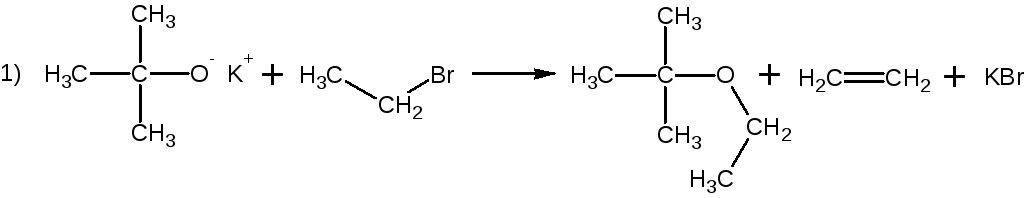
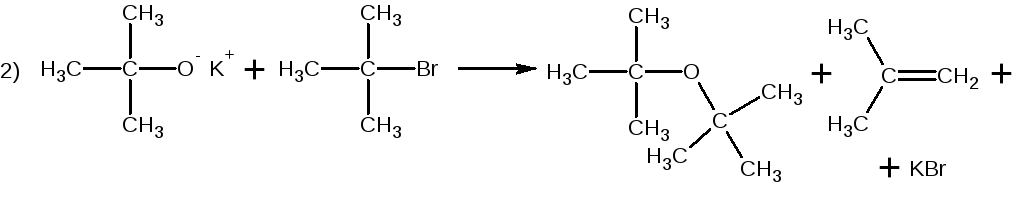


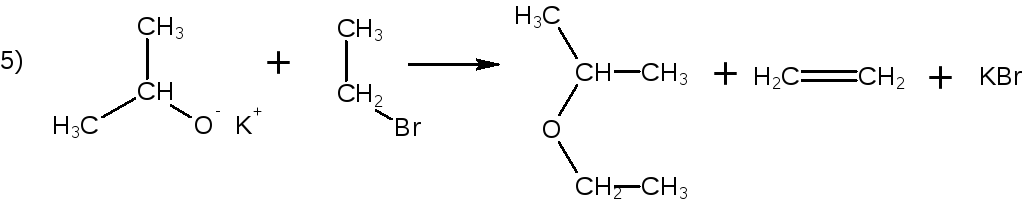
Ответ.
Образование простого эфира происходит в результате бимолекулярного нуклеофильного замещения галогена в алкилгалогениде при действии алкоголят-иона. Пространственные препятствия при атаке алкоголят-иона по атому углерода, связанному с галогеном, возрастают с увеличением степени замещения у этого атома углерода, т.е. при переходе от первичного к третич-ному галогениду. В таком же направлении будут возрастать пространствен-ные препятствия в алкоголяте, т.е. алкоголяты первичных спиртов будут более активны, чем – третичных. Таким образом, выход простого эфира максимален в реакции 3), в которой реагируют первичный галогенид и алкоголят первичного спирта.
Установите соответствие.
Из приведённых соединений первичным спиртом и фенолом (A),
вторичным спиртом и фенолом (B), третичным спиртом и фенолом (C),
фенолом и тиолом (D), тиолом и тиофенолом (E) одновременно
являются:
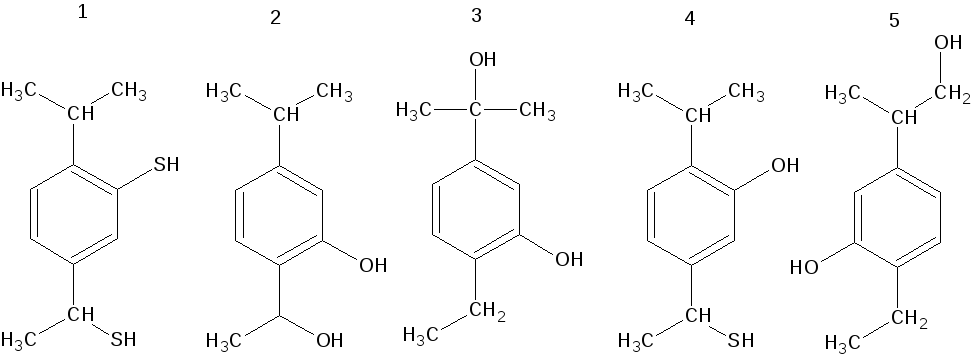
Ответ.
Первичные, вторичные и третичные спирты содержат следующие молекуляр-ные фрагменты, соответственно:
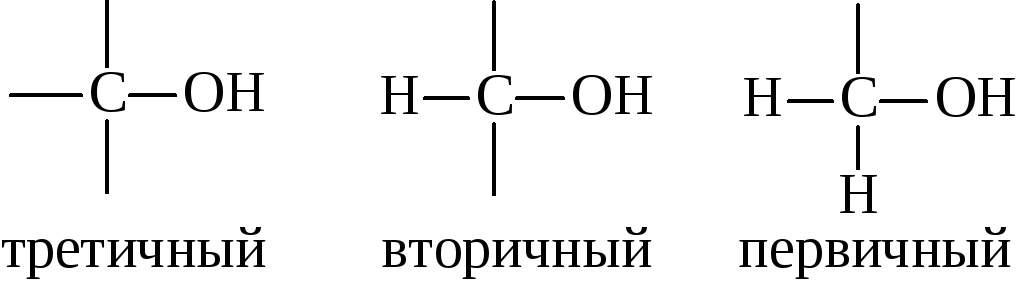
в которых с гидроксильной группой связан алкильный радикал. Тиолы вместо гидроксильной группы содержат SH-группу, а фенолы и тиофенолы содержат OH- и SH-группы, связанные с бензольным кольцом. Отсюда следует что (A) соответствует 5; (B)-3, (C)-2, (D)-4, (E)-1.
5. Какого алкена образуется меньше при дегидратации 3-метилгексанола-3?

Ответ.
При дегидратации спиртов, как правило, преимущественно образуется наиболее стабильный алкен. Стабильность алкена возрастает с увеличением количества алкильных групп у двойной связи. Следовательно, с максималь-ным выходом образуются алкены (3) и (5), содержащие по три алкильные группы у двойной связи, а с минимальным выходом – (4). Алкены (1) и (2) не могут образоваться из 3-метилгексанола-3.
6. Для замещения гидроксильной группы в спиртах на галоген используются
следующие реагенты:
Хлорид натрия;
Бромид фосфора (III);
Фторид серы (VI);
Хлорид галлия;
Фторид ксенона (II)
Ответ.
Для замещения гидроксильной группы в спиртах на галоген (помимо гало-геноводородных кислот, которые не рассматриваются в данных примерах) используются галогенангидриды кислот. К их числу принадлежит только бромид фосфора (III).
7. Одним из методов получения спиртов является гидратация алкенов. Для
каких замещённых алкенов гидратация будет протекать в соответствии
с правилом Марковникова?
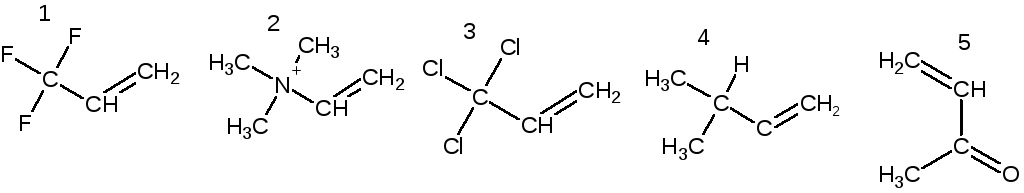
Ответ.
Гидратация в соответствии с обобщённым правилом Марковникова протекает для алкенов, содержащих заместители +I или -I, +M типа. В представленных примерах только для соединения (4).
8. Дегидратации с образованием алкена подвергается легче всего:
Метанол.
Пентанол-2
Пентанол-1
2-метилпропанол-2
Циклопентанол
Ответ.
Дегидратации с образованием алкена легче всего подвергаются третичные спирты. В приведённом ряду к ним относится только (4).
9. Окислению подвергаются следующие спирты:
1-метилциклопентанол-1
пентанол-3
3-метилпентанол-3
2-метилпропанол-2
2-фенилпропанол-2
Ответ.
Окислению легче всего подвергаются первичные и вторичные спирты. В условиях окисления первичных и вторичных спиртов третичные спирты не окисляются. В приведённом ряду только спирт (2) является вторичным и, следовательно, подвергается окислению.
10. Восстановление спиртов до углеводородов происходит при
взаимодействии их с:
Щелочными металлами.
Концентрированной соляной кислотой.
Комлексными гидридами металлов (LiAlH4 , NaBH4 ).
4) Концентрированной йодистоводородной кислотой.
5) Гидридами натрия или калия.
Ответ.
Из приведённого ряда соединений для восстановления спиртов до углеводо-родов используется только концентрированная йодистоводородная кислота в присутствии красного фосфора.
1) ROH + 2HJ = RH + J2 + H2O 2) 2P + 3J2 = 2PJ3
3) 2PJ3 + 3H2O = 6HJ + 2H3PO3
Красный фосфор используется для связывания выделяющегося иода (реакция 2) и регенерации HJ (реакция 3).
11. Для получение дисульфидов используют окисление тиолов различными
окислителями. Какие окислители можно использовать для этой цели
А) HJO3 ; B) HClO4 + H2SO4 ; C) Br2; D) XeF4 ; E) HBrO4 .
Ответ.
Для этой цели обычно используются “мягкие” окислители, чтобы исключить дальнейшее окисление дисульфидов. Из приведённого ряда соединений к ним можно отнести только Br2 , т.е. С).
12. Какие из приведённых ниже диолов при дегидратации будут
образовывать циклические моноэфиры?
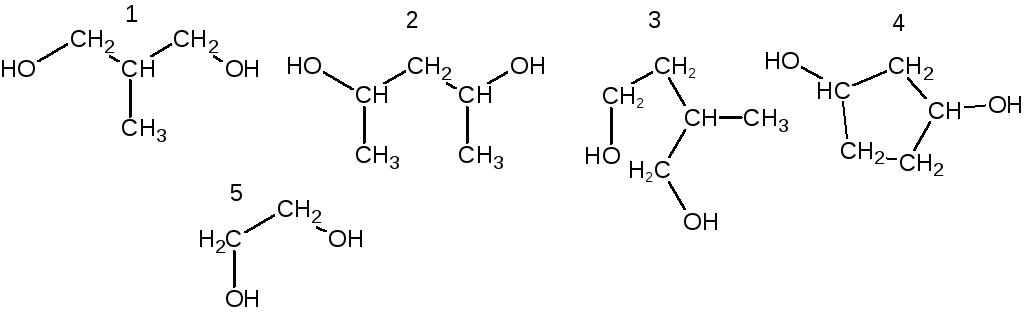
Ответ.
Наиболее легко образуются самые стабильные циклы – пяти- и шестичлен-ные. Из приведённого ряда соединений только диол 3 способен при внутри-молекулярной циклизации образовывать пятичленный цикл.
Расположите приведённые ниже спирты и воду в порядке увеличения
их кислотности.
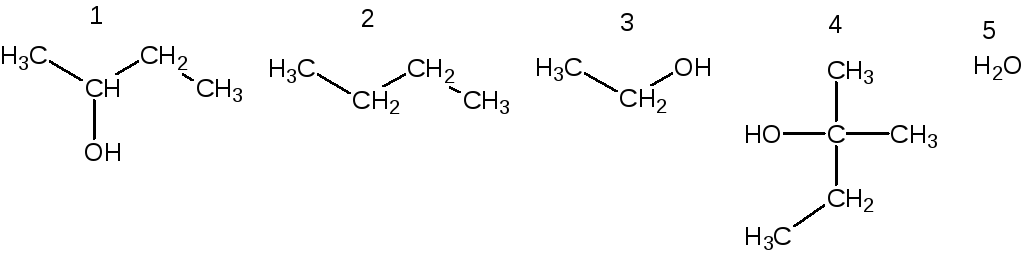
Ответ.
Кислотность спиртов возрастает от третичных к первичным, а вода более сильная кислота чем спирты. Кислотность первичных спиртов с различной величиной радикала приблизительно одинакова. Таким образом, ряд увеличения кислотности спиртов будет выглядеть следующим образом:
4 < 1 < 2 ≈ 3 < 5.
14. Определите верны (В) или неверны (Н) каждое из двух частей
утверждения и само утверждение в целом.
При нагревании метил-втор-бутилового эфира с иодистоводородной кислотой образуется смесь метанола, втор-бутанола, метилиодида и втор-бутилиодида, т.к. реакция расщепления простых эфиров кислотами не региоселективна.
Ответ.
В том случае, если эфир содержит первичные или вторичные алкильные группы, реализуется SN2-механизм, в котором иодид-ион атакует сопряжённую кислоту простого эфира по менее замещенному атому углерода
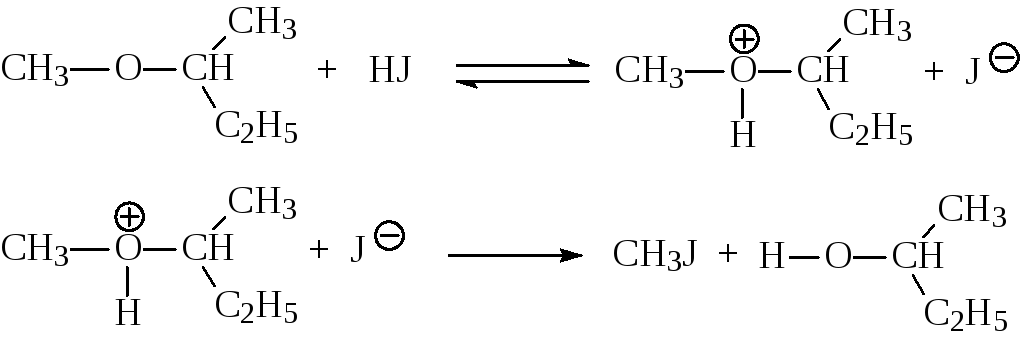
в этом случае образуются только иодистый метил и втор-бутиловый спирт. Таким образом правильный ответ ННН.
Почему для расщепления простых эфиров используют иодистоводород-
ную (HJ) или бромистоводородную (HBr) кислоты, но не соляную (HCl)
или плавиковую (HF)?
Ответ.
На первой стадии в результате кислотно-основной реакции простой эфир превращается в свою сопряжённую кислоту,
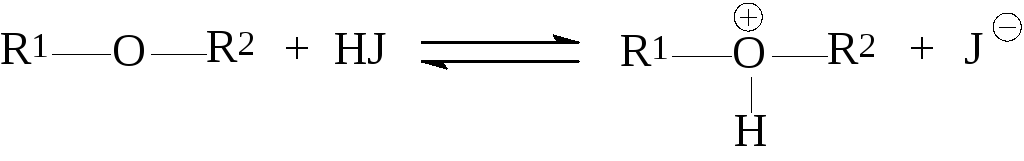
а вторая стадия представляет собой нуклеофильное замещение в сопряжён-ной кислоте простого эфира (или иногда используют термин в протонирован-ной форме простого эфира) под действием галогенид-иона.

Вторая стадия будет осуществляться тем легче, чем более сильным нуклео-филом будет галогенид ион. В водных растворах нуклеофильность галогенид-ионов возрастает от фтора к иоду: F¯<< Cl¯< Br¯ < J¯.
