
- •Военно-медицинская академия
- •Исторические этапы кафедры
- •Руководители (начальники) кафедры
- •Профессоры кафедры
- •Раздел I. Общая патофизиология
- •Глава 1. Дизрегуляция и патологические изменения эффекторов как причины расстройств функциональных систем (нозологический очерк)
- •Глава 2. Болезнь и типовой патологический процесс
- •Глава 3. Нарушения периферического крово- и лимфообращения
- •Глава 4. Диссеминированное внутрисосудистое свертывание
- •Этиология диссеминированного внутрисосудистого свертывания
- •Глава 5. Гипоксия
- •Группировка компонентов горного комплекса по постоянству воздействия на человека
- •Уровни адаптации к гипоксии
- •Глава 6. Воспаление
- •Этапы функционирования нейтрофилов как клеточных эффекторов острого воспаления
- •Медиаторы острого воспаления, высвобождаемые в его очаге тучными клетками
- •Глава 7. Лихорадка и реакция острой фазы
- •Глава 8. Расстройства обмена воды и натрия
- •Наиболее частые причины дефицита объема внеклеточной жидкости
- •Содержания в жидкостях теряемых во внешнюю среду катионов натрия, калия и хлоридного аниона
- •Глава 9. Нарушения обмена калия и кальция
- •Причины гипокалии и гипокалиемии
- •Болезни и патологические состояния, которые вызывают диарею как причину гипокалиемии
- •Патологические состояния и болезни, связанные с высокой действующей концентрацией минералкортикоидов и гипокалиемией (без дефицита внеклеточной жидкости)
- •Изменения электрокардиограммы при расстройствах обмена калия
- •Устранение гиперкалиемии
- •Глава 10. Расстройства кислотно-основного состояния
- •Нормальные величины параметров кислотно-основного состояния
- •Глава 11. Дислипопротеинемии и атеросклероз
- •Глава 12. Реакции повышенной чувствительности
- •Эффекты проаллергических цитокинов
- •Глава 13. Аутоиммунные механизмы развития болезней
- •Глава 14. Артериальная гипертензия
- •Верхние пределы нормальных колебаний ад
- •Классификация тяжести артериальной гипертензии в зависимости от уровня диастолического ад
- •Классификация тяжести артериальной гипертензии
- •Частота видов вторичной артериальной гипертензии среди всех случаев аг у больных
- •Причины обструкции-окклюзии почечной артерии и реноваскулярной аг
- •Глава 15. Патология клетки
- •Звенья антиоксидантной системы и ее некоторые факторы
- •Глава 16. Канцерогенез
- •Иммунные и сывороточные опухолевые маркеры
- •Иммуномаркеры опухолей
- •Раздел II. Частная патофизиология
- •Глава 1. Патогенез дыхательной недостаточности, артериальной гипоксемии и заболеваний органов дыхания
- •Компенсация респираторного ацидоза ори гиперкапнии
- •Элементы системы терапии при одн
- •Эффекты проаллергических цитокинов
- •Связь признаков астматического статуса и обострения бронхиальной астмы со звеньями их патогенеза
- •Стадии обострения бронхиальной астмы и астматического статуса
- •Глава 2. Патофизиология сердечно-сосудистой системы
- •Классификация кардиомиопатий воз
- •Причины дилатационной кардиомиопатии
- •Связи патологических изменений клеток сердца при оим с изменениями электрокардиограммы
- •Дозы фибринолитических средств для тромболизиса при тромбозе венечных артерий
- •Степени восстановления проходимости обтурированной тромбом венечной артерии под действием тромболитичесих средств
- •Патогенетическая классификация симпатикотонической постуральной артериальной гипотензии
- •Симпатиколитическая артериальная гипотензия
- •Глава 3. Патофизиология органов пищеварения
- •Причины острого панкреатита
- •Критерии Ranson (Ranson j.H., Rifkind k.M., Roses d.F. Et al., 1974)
- •Летальность при остром панкреатите в зависимости от числа критериев
- •Наиболее частые причины внутрипеченочного и внепеченочного холестаза
- •Холестатический синдром
- •Связь клинических признаков цирроза печени со звеньями его патогенеза
- •Этиология и патоморфогенез циррозов печени
- •Расстройства высшей нервной деятельности и сознания у больных в печеночной коме
- •Этиопатогенетическая классификация осмотической диареи
- •Глава 4. Патофизиология крови
- •Франко-американо-британская классификация острого лимфоидного лейкоза (острой лимфоцитарной лейкемии)
- •Франко-американо-британская классификация острого миелоидного лейкоза
- •Связь симптомов и звеньев патогенеза хронического миелоидного лейкоза
- •Некоторые механизмы развития коагулопатии, связанной с острыми и хроническими лейкозами
- •Глава 5. Патофизиология почек
- •Отрицательные следствия олигурии
- •Различия между преренальной и ренальной острой почечной недостаточностью
- •Механические препятствия оттоку мочи вне почек как причины обструктивной уропатии
- •Лечебные воздействия, направленные на устранение и предупреждение действия факторов преренальной почечной недостаточности
- •Показания к гемодиализу
- •Патогенетическая терапия гипокалиемии при острой почечной недостаточности
- •Патогенетическая терапия метаболического ацидоза при острой почечной недостаточности
- •Патогенетическая терапия патологического увеличения объема внеклеточной жидкости при острой почечной недостаточности
- •Глава 6. Патофизиология эндокринопатий
- •Признаки и звенья патогенеза гипотиреоза
- •Патогенез и симптомы гипертиреоза
- •Признаки и патогенез болезни Аддисона
- •Патогенез и признаки недостаточности секреции эндогенных кортикостероидов
- •Глава 7. Патофизиология нервной системы
- •Принципы предупреждения и лечения патологической боли у тяжелых раненых
- •Глава 8. Иммунодефициты
- •Врожденные иммунодефициты
- •Глава 9. Патофизиология шока, комы, раневой болезни и синдрома множественной системной органной недостаточности
- •Шкала комы Глазго
- •Причины комы, связанной с локальными повреждениями структур головного мозга
- •Причины комы вследствие энцефалопатий, распространенных в пределах всего головного мозга
- •Элементы терапии больного, находящегося в коме
- •Признаки септического шока
- •Грамотрицательными бактериями
- •Раздел III. Патофизиология расстройств функциональных систем организма, связанных с военно-профессиональной детельностью
- •Глава 1. Изменение функций организма при действии факторов авиационного и космического полета
- •Факторы полета
- •Структурные и функциональные изменения, возникающие при действии ударных перегрузок
- •Резонансные частоты тела человека и его отдельных частей
- •Глава 2. Профессиональная патология специалистов военно-морского флота
- •Влияние гипербарии на функциональное состояние гипербарии
- •Глава 3. Психогенные расстройства в условиях боевых действий и чрезвычайных (экстремальных) ситуаций
Глава 11. Дислипопротеинемии и атеросклероз
Патогенез гиперлипопротеинемии первого типа
Семейный дефицит липопротеинлипазы наследуется по аутосомно-рецессивому типу. Так как при данном нарушении липидного обмена в крови растет содержание не связанных с патогенезом атеросклероза триглицеридов и хиломикронов, то с высоким риском атеросклероза данная дислипопротеинемия не связана. Алолипопротеин С-II - это одна из составляющих липопротеинов очень низкой плотности и липопротеинов высокой плотности. Представляет собой эндогенный активатор липопротеинлипазы. При наследственном дефиците аполипопротеина С-II возникает состояние, аналогичное дислипопротеинемии первого типа (синдром Брекенриджа), которое, как и семейный дефицит липопротеинлипазы, в частности характеризует панкреатит, связанный с высокими концентрациями в крови триглицеридов и хиломикронов. Панкреатит данной этиологии может привести ко вторичному сахарному диабету.
Патогенез семейной гиперхолестеринемии (дислипопротеинемии второго типа)
Семейная гиперхолестерицемия второго типа наследуется по аутосомно-доминантному типу. Она представляет собой результат закрепления в ряду поколений мутаций аллелей Rbo, Rb-b и Rtio. В результате данных мутаций экспрессия рецепторов к липопротеинам низкой площостд на поверхности клеток, образующих холестерин, недостаточна. Низкая экспрессия рецепторов снижает пиноцитоз атерогенных липопротеинов низкой плотности. В результате в данных клетках дадает содержание свободного холестерина, что растормаживает ключевой фермент синтеза холестерина, гидроксиметилглютарил-коэнзим А-редуктазу. Синтез холестерина растет, и нарастает гилерхолестеринемия. Гиперхолестеринемия повышает образование атерогенных липопротеинов низкой плотности гепатоцитами. Кроме того, их содержание в крови растет из-за недостаточного пиноцотоза данных атерогенных липо- протеинов гепатоцитами. Высокая концентрация атерогенных липопротеинов низкой плотности во внеклеточной жидкости и плазме крови обусловливает высокий риск атеросклероза и приводит к инфаркту миокарда в период онтогенеза от 20 до 50 лет.
Атерогенность липопротеинов низкой плотности
Липопротеины низкой плотности представляют собой субстраты для свободнорадикального окисления с образованием окисленных форм липопротеинов низкой плотности. Окисленные формы липопротеинов низкой плотности - это эндогенные лиганды к “рецёпторам-мусорщикам” наружной поверхности эндотелиальных клеток. Их взаимодействие с “рецепторами-мусорщиками” активирует эндотелиальше клетки, которые в инактивиройанном состоянии высвобождают факторы клеточного pостa, цитокины-флогогены и свободные кислородные радикалы. Таким образом, индуцируется хроническое воспаление сосудистой стенки с патогенным пролиферативным компонентом, составляющее морфопатогенез возникновения и деструкции атеросклеротйческой бляшки.
Вероятность деструкции атеросклеротической бляшки определяет характер воспаления сосудистой стенки. Главным эффектором воспаления являются мононуклеарные фагоциты.
Позитивный эффект таких антибактериальных препаратов, как рокситромицин и азитромицин, на атерогенез и нестабильность атеросклеротической бляшки послужили основой для предположения о том, что Chlamydia pneumoniae играет роль в этиологии атеросклероза. Кроме того, данное действие антибиотиков из группы макролидов связывают с их влиянием на калиевый канал наружной мембраны мононуклеарных фагоцитов, в резудатате чего происходит депрессия макрофагов как клеточных эффекторов воспаления. Острые респираторные инфекции - это фактор риска инфаркта миокарда, внезапной сердечной смерти и нестабильной стенокардии.
Гиперлипидемии третьего, четвертого и пятого типов
В основе гиперлипидемии третьего типа лежит наследуемая по аутосомно-доминантному типу врожденная недостаточность катаболизма атерогенных липопротеинов промежуточной плотности. Гиперлипидемию третьего типа характеризуют ускоренное развитие атеросклероза и высокий риск тромбоза венечных артерий и острого инфаркта миокарда, сахарный диабет, ожирение, гипотиреоз и особо выраженный ксантоматоз. У больных выявляют poст в плазме крови концентраций триглицеридов и холестерина, которые липопротеины промежуточной плотности переносят от печени на периферию. О сахарном диабете у таких больных свидетельствует сниженная толерантность по отношений к глюкозе.
Гиперлипидемия четвертою типа - это наследуемое по аутосомно-доминантному типу нарушение липидного обмена, которое характеризует гипертриглицеридемия, то есть аномально высокое содерние триглицеридов в плазме крови. Это наиболее частое из нарушений: липидного обмена у больных, при котором атеросклероз редко поражает периферические и венечные артерии. При гиперлипидемии четвертого типа в плазме крови повышены концентрации тиглицеридов и липопротеинов очень низкой плотности. Отдельно выделяют приобретенную гиперлипидемию четвертого типа, котоую вызывают сахарный диабет, уремия, препараты из группы глюкокортикоидов, а также бета-адреномиметики.
Гиперлипидемия гиперлипопротпеинемия пятого типа - это полиэтиологичное нарушение липидного обмена, вследствие которого у части больных возникает ксантоматоз и панкреатит как следствия патогенно высоких концентраций в плазме крови липопротеинов очень низкой плотности и хиломикронов.
Ведущие звенья патогенеза атеросклероза
Атеросклеротическое перерождение сосудов во многом определяет пролиферация миоцитов сосудистой стенки, индуцируемая факторами клеточного роста тромбоцитов, активированных мононуклеаров, а также самих гладкомышечных клеток. Термин “атеросклероза” описывает изменения сосудистой стенки при этом системном типовом патологическом процессе. Слово “атере” (греч.) означает “кашица” и указывает на образование в стенках сосудов кашицеобразных липидных отложений с их дальнейшим склерозированием и уплотнением.
По определению Всемирной организации здравоохранения: “Атеросклероз - зто вариабельная комбинация изменений внутренней оболочки (интимы) артерий, включающая накопление липидов, сложных углеводов, фиброзной ткани, компонентов крови, кальцификацию и сопутствующие изменения средней оболочки (медии)”.
При гистологическом исследовании пораженных атеросклерозом участков сосудистой стенки выявляют характерное патологическое образование, атеросклеротическую бляшку. Ее формируют липиды, лейкоциты, гладкомышечные клетки и межклеточное вещество интимы артерий. Образованию бляшки предшествует адгезия (прилипание) циркулирующих моноцитов и лимфоцитов к артериальному эндотелию с последующим локальным накоплением пенистых клеток. Необходимым условием адгезии является экспрессия на поверхности эндотелиальных клеток адгезивных молекул (активация эндотелиальных клеток). Пенистые клетки представляют собой активированные мононуклеары, видоизмененные в результате эндоцитоза лицидов.
Некоторые липопротеины можно считать атерогенными, неатерогенными, а третьи антиатерогенными.
Под атерогенными следует понимать липопротеины, высокая коцентрация которых в плазме крови достоверно связана с развитием атеросклероза. Поверхность макрофагов содержит рецепторы к липопротеинам очень низкой плотности и непостоянные рецепторы к измененным в результате окисления липопротеинам низкой плотности (“рецепторы-мусорщики”). Предположительно активация мононуклеаров через связывание зтих рецепторов с окисленными атерогенными липопротеинами ведет к активации субинтимальных мононуклеарных фагоцитов, в результате которой они приобретают способность к эндоцитозу липопротеинов.
В ранней стадии атеросклеротического поражения сосудистой стенки в ней выявляют липидные прожилки и пенистые клетки. Этот начальный этап формирования атеросклеротической бляшки вызывает возбуждение непостоянно присутствующих на клеточной поверхности макрофагов - рецепторов к окисленным липопротеинам низкой плотности (ацетил-рецепторы ЛПНП, “рецепгорн-мусорщики”). Эти рецепторы обладают высоким сродством к окисленным липопротеинам низкой плотности (“мусору”). Изменения липопротеинов низкой плотности в результате окисления, которое обусловливает их высокое сродство к “рецепторам-мусорщикам”, включают:
трансформацию лецитина в составе липопротеинов в лизолецитин;
окисление холестерина;
рост отрицательного заряда и плотности липопротеинов;
снижение содержания в липопротеинах низкой плотности полиненасыщенных жирных кислот;
распад структурного апопротеина липопротеинов низкой плотности В-100 с высвобождением гистидина, лизина и пролина. Окисленные липопротеины служат хемоаттрактантами для макрофагов сосудистой стенки, одновременно являясь для них и объектом эндоцитоза.
Как результат патогенных межклеточных взаимодействий атеросклероз представляет собой патологические изменения стенок артерий большого и среднего диаметров, которые составляют и вызывают локальная аккумуляция в интиме липидов и мононуклеаров, миграция и пролиферация гладкомышечных клеток, а также отложения вещества внеклеточного матрикса. Патогенные межклеточные взаимодействия, приводящие к атеросклерозу, реализуются не только через действие факторов роста, но и в результате эффектов цитокинов-флогогенов, медиаторов воспаления и экспрессии адгезивных молекул. Начальным этапом патогенеза атеросклероза как последовательности межклеточных взаимодействий является адгезия моноцита циркулирующей крови к эндотелиальным клеткам с их последующей миграцией в интиму. При этом индукторы атеросклероза, окисленные (модифицированные) липопротеины низкой плотности, воздействуя на лейкоциты циркулирующей крови и эндотелиальные клетки, вызывают экспрессию на их поверхности адгезивных молекул. Так, лизофосфатидилхолин - элемент молекулы окисленных атерогенных липопротеинов - индуцирует экспрессию межклеточной адгезивной молекулы-1 на поверхности эндотелиальных клеток. Известно, что атерогенные липопротеины оказывают на эндотелий прямые и непрямые влияния, повышающие экспрессию на их поверхности эндотелиально-лейкоцитарных адгезивных молекул (ЭЛАМ). Непрямой эффект атерогенных липопротеинов на рост экспрессии таких адгезивных молекул состоит в стимуляций паракринной секреции гладкомышечными клетками и мо-нонуклеарными макрофагами сосудистой стенки. Адгезия лейкоцитов к сосудистой стенке служит первым этапом их проникновения в интиму. Там активированные моноциты секретируют ряд активаторов эндотелия и хемоаттрактантов, стимулирующих дальнейшую инфильтрацию очага атеросклеротического повреждения моноцитами и лимфоцитами из циркулирующей крови, Патогенное функционирование иммунокомпетентных клеток в качестве эффекторов атеросклероза указывает на участие в развитии атеросклероза иммнопатологической реакции.
Атеросклероз - это хроническое воспаление сосудистой стенки, протекающающее с преобладанием пролиферативнго компонента. Его основными клеточными эффекторами являются эндотелиоциты, моноциты циркулирующей крови, мойонуклеарные фагоциты субинтимального слоя, гладагомышечные сосудистые клетки, актвированные окисленными атерогенными липопротеинами или цитокинами-флогогенами.
Воспаление в очаге атеросклеротического поражения усиливает взаимосвязанное с ним локальное свертывание крови, которое могут вызвать сами атерогенные липорротеины. Так, атерогенный липопротеин содержит гдикопротеин, связанный р аполипротеином В. Идентичность структуры липопротеина строению плазминогена может обусловливать внутрисосудистый тромбогенез через конкурентное связывание рецепторов к плазминогену на поверхности эндотелиоцитов.
Атеросклеротическое перерождение сосудистой стенки начинается с образования прожилок атерогенных липопротеинов и пенистых макрофагов в сосудистой стенке. В данном начальном этапе формирования атеросклеротической бляшки особую роль играют мононуклеарные фагоциты сосудистой стенки, которые сами могут индуцировать окисление липопротеинов низкой плотности через высвобождение свободных кислородных радикалов и (или) активацию липооксигеназы. Так как мононуклеары представляют собой эффектор единой системы иммунитета организма, то мы вправе предположить роль в развитии атеросклероза нервного эндогенного этиологического фактора, столь сильно меняющего состояние системы иммунитета, и ее макрофагального звена в частности. Кроме того, патогенный стресс как состояние, которое характеризует системная интенсификация свободнорадикального окисления липидов, может повышать уровень окисления липопротеинов низкой плотности и тем самым предрасполагать к атеросклерозу.
Пенистые клетки высвобождают ряд цитокинов, чье действие вызывает пролиферацию клеточных элементов, в особенности миоцитов гладкомышечных элементов сосудистой стенки. Кроме того, цитокины активированных макрофагов активируют эндотелиоциты, что ведет к росту экспрессии их тромбогенного потенциала. Цитокины пенистых клеток активируют и нейтрофилы циркулирующей крови, что вызывает воспаление с полиморфонуклеарами в качестве его клеточных эффекторов. В результате в составе атеросклеротичсеской бляшки находятся пролиферирующие миоциты сосудистой стенки, агрегаты активированных тромбоцитов и других форменных элементов крови, активированные нейтрофилы и нити фибрина. Все это характеризует атеросклеротическую бляшку как очаг воспаления и локус тромбоза.
Макрофаги, окисленные липопротеины, ацетил-ЛПНП-рецепторы играют определяющую роль в индукции атеросклероза. В дальнейшем процесс образования атеросклеротической бляшки теряет связь с этими этиологическими факторами, то есть через патогенные межклеточные взаимодействия происходит его эндогенизация.
В 70-е годы были сформулированы основные положения теории атеросклероза, которую назвали теорией “реакция на травму”, В соответствии с данной теорией, механическое и токсическое повреждение эндотелия обнажает субэндотелиальные структуры. В результате обнажения субэндотелиальных структур происходит адгезия тромбоцитов к макромолекулам субэндотелиального слоя. Адгезия активирует тромбоциты, которые в активированном состоянии высвобождают вещества, стимулирующие тромбообразование: аденозиндифосфат, тромбин, фактор тромбоцитов III. Кроме того, активированные тромбоциты высвобождают фактор клеточного роста тромбоцитов. Высвобождение факторов клеточного роста и тромбогенеза стимулирует пролиферацию гладкомышечных клеток, повышает массу межклеточного матрикса, а также вызывает отложение фибрина и образование тромба в месте повреждения эндотелия, что и формирует атеросклеротйческую бляшку.
Современные представления о патогенезе атеросклероза во многом повторяют теории “реакции на травму”. При этом под травмой следует понимать не морфологический дефект эндотелия, а патогенное изменение функционального состояния эндотелиоцитов.
Функциональное состояние эндотелиальной клетки - это детерминанта образования вазоактивных веществ, строения межклеточного матрикса и секреции факторов клеточного роста на уровне стенки сосудов. Патогенное состояние эндотелиальной клетки как инициирующий момент патогенеза атеросклероза в основном обусловлено ее реакцией на взаимодействие с окисленными атерогенными липопротеинами низкой плотности. Образование окисленных атерогенных липопротеинов связано с образованием и высвобождением свободных кислородных радикалов. Воздействие свободных кислородных радикалов на атерогенные липопротеины приводит к появлению в их составе окисленных жирных кислот и фрагментации аполипопротеина В-100. В результате таких изменений структуры липопротеина он перестает быть лигандом к рецепopaм липопротеинов низкой плотности и связывается с “рецепторами-мусорщиками” на наружной клеточной поверхности эндотелиоццитов. Это активирует эндотелиальную клетку, которая в активированном состоянии начинает активно высвобождать свободные кислородные радикалы. Кроме того, в активированном состоянии эндотелиальная клетка высвобождает ряд биоактивных веществ, цитокинов, прокоагулянтов и факторов клеточного роста. Гиперактивация эндотелиальной клетки через секрецию флогогенов вовлекает в воспаление мононуклеары сосудистой стенки, которые в активированном состоянии становятся клеточными эффекторами воспаления, которое и составляет в основном патогенез атеросклероза (рис.11.1), обусловливая альтерцию сосудистой стенки и образование атероскле-ротической бляшки. В активированном состоянии эндотелиальная клетка репрессирует на своей поверхности адгезивные молекулы. Это стимулирует адгезию мононуклеарных и полиморфонуклеарных фагоцитов к эндотелиоцитам как Начальный этап преимущественно мононуклеарного воспаления, составляющего патогенез атеросклероза.
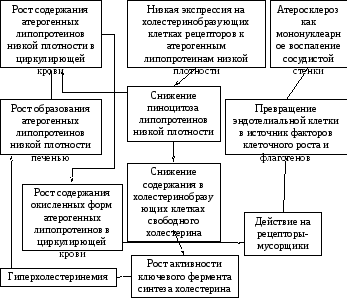
Рис. 11.1. Схема ведущих звеньев патогенеза атеросклероза при пшерли-попротеинемии второго типа
