
6 курс / Эндокринология / ЭХОСЕМИОТИКА_АУТОИММУННЫХ_ЗАБОЛЕВАНИЙ_ЩИТОВИДНОЙ_ЖЕЛЕЗЫ
.pdf
271
Рис.226. Ультрасонограммы, отражающие особенности эхосемиотики аутоиммунного тиреоидита у больных с локализованной (а, б) и диффузной (в) формами заболевания.
Подробное описание — в тексте.
мых при AT, обусловлена измененнием размеров ЩЖ. Анализ данных ультразвукового исследования показал, что в большинстве случаев (81% из 501 исследованного больного) при аутоиммунном тиреоидите наблюдается увеличение объема органа (рис. 229 а, б, в). Во многих случаях увеличение размеров ЩЖ достигает значительной степени выраженности. Поданным ультразвуковой морфометрии у 27% обследованных нами больных имело место диффузное увеличение ЩЖ 1-й степени, у 35% больных — II степени и у 19% — третьей степени. В то же время у 13% больных размер железы оставался нормальным и у 6% наблюдалось уменьшение органа.
УвеличениетолщиныперешейкаЩЖ.
Важную дополнительную информацию для ультразвуковой диагностики аутоиммунного тиреоидита Хашимото можно получить и при выполнении исследования в поперечной плоскости сканирования. На ультразвуковых томограммах, произведенных в этой проекции, отчетливо идентифицируется еще один, характерный для тиреоидита признак
— увеличение толщины перешейка ЩЖ (рис. 230 а, б). Во многих случаях (по нашим наблюдениям у 85% обследованных больных AT) изменения линейных размеров перешейка ЩЖ достигают значительной степени выраженности.
Нарушение эхоструктуры или появле-

272
Рис.227. Эхограммы щитовидной железы, выполненные в поперечных плоскостях сканирования больных аутоиммунным тиреоидитом Хашимото.
Отчетливо видно сглаживание границ между краем передней поверхности щитовидной железы и мышцами шеи. Определяются и другие признаки аутоиммунного тиреоидита: наличие множественных гипоэхогенных участков и общее снижение эхогенности.
ние на фоне AT объемных образований. |
коллоидный узел. Две трети больных имели |
Наиболее сложным видом изменений щи- |
различную степень отклонения от нормаль- |
товидной железы у больных аутоиммунным |
ных размеров органа. Ультразвуковая диаг- |
тиреоидитом являются такие состояния, ког- |
ностика подобных изменений в железе до- |
да железа претерпевает одновременно три |
лжна слагаться из трех этапов. Первоначаль- |
типа изменений, т.е. когда отмечается из- |
но выполняется оценка эхогенности ЩЖ, т.е. |
менение эхогенности, происходит измене- |
мы четко устанавливаем наличие AT, затем |
ние размеров органа и в щитовидной желе- |
необходимо произвести измерение разме- |
зе формируются объемные образования - |
ров органа, т.е. выясняем степень увеличе- |
кисты, аденомы, рак, коллоидные узлы и др. |
ния органа и затем — изучить особенности |
[23, 56] — то есть наблюдается истинное |
эхоструктуры. Для этого: 1) определяли раз- |
нарушениеэхоструктуры.Поднашимна- |
меры и форму объемного образования; 2) |
блюдением находилось 31 больной AT, сре- |
устанавливали степень изменений их эхоп- |
ди которых у 13-ти обнаружены аденомы, у |
лотности и эхоструктуры; 3) производили |
4-х — рак ЩЖ, у 3 больных — злокачествен- |
характеристику их контуров; 4) выясняли |
ная лимфома, у 4 — киста и у 7 больных |
локализацию объемных образований; 5) |

273
Рис.228. Ультрасонограммы щитовидной железы больных аутоиммунным тиреоидитом, отражающие различную степень бугристой деформации края задней поверхности.
определяли их число. Выполнив ультразвуковое исследование в указанной последовательности, часто удается получить дополнительные диагностические критерии для определения характера процессов, вследствие развития которых происходят сочетанные изменения в щитовидной железе при AT.
Диагностика кист не встречала какихлибо трудностей: обнаружение анэхогенных образований с четкими контурами указывало на формирование в ней полостей, запол-
ненных жидкостью (рис. 231а). В то же время при обнаружении гипоэхогенных (рис.2316) или гиперэхогенных образований (рис. 231 в) у больных AT имеются значительные трудности дифференциальной диагностики. В этих наблюдениях высказывалось предположение о наличии рака, аденомы, коллоидного узла и лишь выполнение УЗТПАБ позволяет установить или исключить диагноз злокачественности объемных образований, формирующихся на фоне аутоиммунного тиреоидита [31, 47, 56].

274
Рис.229. Ультрасонограммы ЩЖ в норме (а) и и больных аутоиммунным тиреоидитом Хашимото (б, в), отражающие различную степень выраженности увеличения объема органа.
Темным тоном показано увеличение объема щитовидной железы.
Рис.230. Увеличение толщины перешейка щитовидной железы у больных аутоиммунным тиреоидитом Хашимото.
275
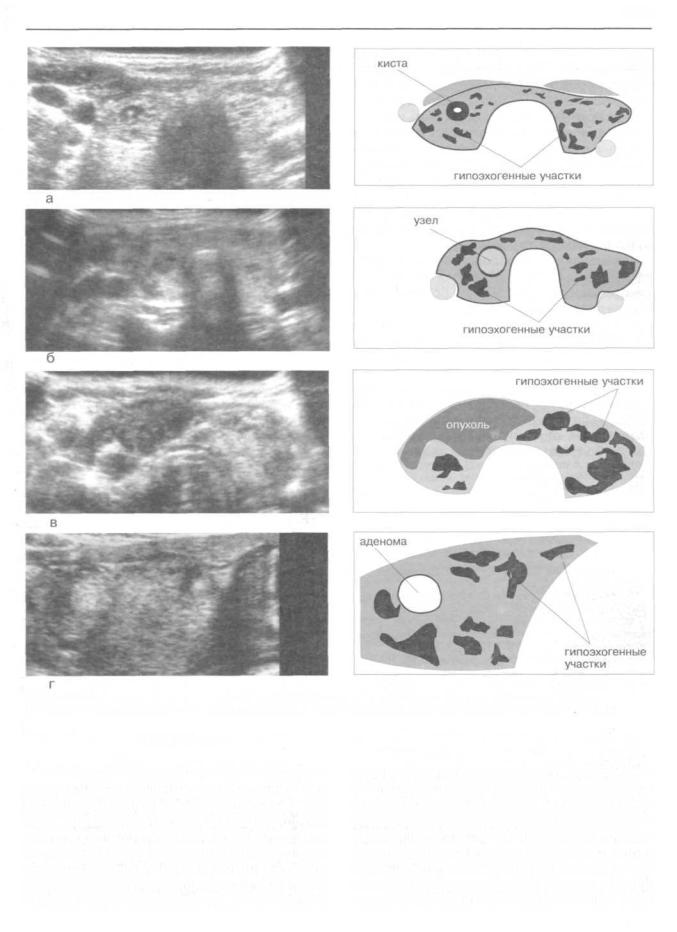
Рис.231. Ультрасонограммы щитовидной железы больных с сочетанной формой аутоиммунного тиреоидита.
а — киста; 6 — коллоидный узел; в — рак щитовидной железы; г — аденома (на фоне аутоиммунного тиреоидита^
Заключение |
|
Таким образом, на ультразвуковых томог- |
поверхности; 2) изменение размеров до- |
раммах ЩЖ у больных аутоиммунным ти- |
лей и перешейка ЩЖ и 3) изменение на |
реоидитом отчетливо выявляются: 1) изме- |
фонеATэхоструктурыввидекист,аде- |
нение эхогенности в виде беспорядочно |
ном, рака и коллоидных узлов и др. Об- |
расположенных гипоэхогенных участков раз- |
наружение описанных выше эхосемиотичес- |
личного размера и формы, мелких гипер- |
ких признаков является основой для при- |
эхогенных включений, сглаживания границ |
менения ультрасонографии в ранней и уточ- |
между железой и передними мышцами шеи, |
ненной диагностике хронического лимфоци- |
бугристой деформации контуров ее задней |
тарного тиреоидита Хашимото. При этом |

276
особую значимость приобретает сочетанная оценка изменений эхогенности, эхоструктуры, размеров ЩЖ. Такой методический подход способствует не только распознаванию ранних признаков AT, но может быть использован для отличительного разграничения больных очаговой и диффузной формами заболевания, изучения степени выраженности деструктивных изменений ЩЖ на разных стадиях патологического процесса и выделения лимфопролиферативной,
фиброзной и фибролимфоидной форм аутоиммунноготиреоидита.
Применение ультрасонографии является эффективным диагностическим методом отличительного разграничения больных аутоиммунным тиреоидитом от пациентов с многоузловым эутиреоидным зобом. Эхосемиотика ЩЖ при AT настолько характерна, что, во многих случаях, выполнение только ультразвукового исследования позволяет получить необходимые критерии для дифференциальной диагностики AT. Для верификации природы патологических изменений, развивающихся в области очаговых изменений ЩЖ у больных хроническим лимфоцитар-
ным тиреоидитом, ультразвуковое исследование целесообразно дополнять результатами УЗ-ТПАБ. Обнаружение в мазках лимфоцитов и плазматических клеток является надежной основой для верификации диагноза AT.
Целесообразность применения УЗ-ТПАБ
убольных AT приобретает важную роль в связи с фактами о частом сочетании этого заболевания со злокачественными эпителиальными опухолями ЩЖ и лимфомами. При обнаружении на ультрасонограммах ЩЖ больных AT «солидных» узлов необходимо произвести цитологическое изучение материала из этих объемных образований. Использование ультразвукового контроля при выполнении тонкоигольной аспирационной биопсии значительно облегчает задачу получения такого материала и позволяет произвести цитологическую идентификацию рака ЩЖ, злокачественных лимфом и аденом. Применение УЗ-ТПАБ во многих случаях исключает необходимость применения неоправданных хирургических вмешательств
убольных аутоиммунным тиреоидитом.
ЛИТЕРАТУРА
1. Абдраханов Е.А. Зоб Риделя. Здравоохр. Ка- |
Тез.респ.конф., 12-14марта 1991,Минск, 1991, стр. |
захстана,1970,N7,стр.73. |
155. |
2. АлешинБ.В., ТкачФ.С. Аутоиммунный тирео- |
9. Горохова В.А., Кеда Ю.М., Крюкова И.В. и |
идит. Пробл. эндокринол., 1968, т.4, N6, стр. 113. |
др.Иммуноферментныйметодопределенияаутоан- |
3. Анохин Б.М. Клинико-радиологические сопос- |
тителкмикросомальнымантигенамтиреоцитовчело- |
тавленияубольныхаутоиммуннымитиреоидитами. |
века. Пробл. эндокринол., 1990, т. 36, N 6, стр. 8. |
Пробл. эндокринол., 1979, т. 25, N 3, стр. 31. |
10. Давыдова Е.В., Грицевич Н.М., Лавничук |
4. Базарова Э.И., Серпуховитин СЮ. Некото- |
О.А.,ЛеоноваЛ.А.Некоторыевопросыдиагностики |
рые вопросы диагностики и лечения аутоиммунного |
аутоиммунноготиреоидитавдетскомвозрасте.Тез. |
тиреоидита.Пробл.эндокринол., 1989, т.35,N2,стр. |
докл. 3-й респ. конф. 15-17 апреля 1992 г., Гомель, |
37. |
1992, стр. 150. |
5. Бомаш Н.Ю. Морфологические признаки зоба |
11.КалининА.П.Диагностикааутоиммунноготи- |
Хашимото.Арх.патол.,1966,т.28,N10,стр.27. |
реоидита. Сов. мед., 1988, N 1, стр. 42. |
6. Бронштейн М.Э. Морфологические варианты |
12. КалининА.П., Потемкина Е.Е., Пешева Н.В. |
аутоиммунных заболеваний щитовидной железы. |
Иммунологическиеаспектыаутоиммун |
Пробл. эндокринол., 1991, т. 37, N 2, стр. 6. |
ноготиреоидита.Пробл.эндокринол.,1994,т.40,N |
7. Виноградова Ю.Е., Виноградов Д.Л., Пове- |
1, стр. 56. |
ренныйA.M.,ЦыбА.Ф.Аутоиммунныетиреоидитыу |
13. Океанова Т.А., Внотченко С.Л., Федосеева |
больныхнекоторымигематологическимизаболевани- |
Г.И. Динамика антитиреоидных антител у больных |
ями. Тер. архив, 1994, т. 66, N 7, стр. 65. |
зобом Хашимото. Тер. архив, 1990, т. 62, N 9, стр. 87. |
8. Воронцова Т.В., Галицкая Н.Н., Поверенный |
14. ПоверенныйA.M. Почему антитела кДНК яв- |
A.M. идр. Новый комплекс лабораторных тестовдля |
ляютсяпоказателемаутоиммунногопроцесса.Имму- |
выявления групп риска с аутоиммунными тиреоиди- |
нология, 1986, N 6, стр. 86. |
тами.Научно-практическиеаспектысохраненияздо- |
15. ПоверенныйA.M., РоттГ.М., Сулаева Н.И. |
ровья людей, подвергшихся радиационному воздей- |
и др. Взаимодействие иммуноглобулинов с заряжен- |
ствию в результате аварии на ЧернобыльскойАЭС: |
нымибиополимерами:значениеврегуляциигумораль- |

279
7.2.ПОДОСТРЫЕ ТИРЕОИДИТЫ
Кчислу этих, довольно редких заболеваходит разрушение фолликулов в участках
ний, относятся: подострый гранулематозный тиреоидит [7, 8, 31] и безболевой «послеродовой» тиреоидит [9, 22, 38]. В последние годы получены данные, что в диагностике подострых тиреоидитов выполнение ультразвукового исследования позволяет получить важную дополнительную информацию [11, 12, 17, 24, 25].
Подострый гранулематозный тирео-
идит описан впервые Де Карвеном в 1905 году. Это заболевание характеризуется развитием воспалительных процессов в ткани ЩЖ и деструктивными изменениями тиреоидной паренхимы [5, 6, 8, 31]. На более поздних стадиях заболевания формируются небольшие по размеру инфильтраты из лимфоцитов, макрофагов и гигантских клеток [21, 31].
Наиболее распространенной концепцией о причинах развития тиреоидита Де Карвена является вирусная теория [7, 8, 14, 37]. Однако природа вируса, вызывающего развитие этого заболевания, точно не установлена. Считают, что подострый тиреоидит Де Карвена может быть индуцирован вирусом Коксаки, аденовирусами, вирусом эндемического паротита и др. [5, 8, 11].
Развитию тиреоидита Де Карвена способствуют наследственные факторы [7, 36]. Генетическая предрасположенность к этому заболеванию связана с функциональными нарушениями системы гистосовместимости [5, 37]. Вирусные антигены комплексируются с антигенами гистосовместимости на поверхности тиреоцитов, вызывая деструкцию этих клеток. Дополнительным предрасполагающим фактором развития тиреоидита Де Карвена являются очаги хронической инфекции в области носоглоточного лимфоидного кольца [6, 8, 14, 35].
Патоморфологи выделяют несколько стадий развития изменений ткани ЩЖ при тиреоидите Де Карвена [6, 7, 21, 36]. В ранние сроки отмечается гиперемия, расширение мелких кровеносных сосудов, экссудация и отек межфолликулярной стромы ЩЖ. Одновременно развиваются дистрофические изменения тиреоцитов. Затем проис-
предсуществующих воспалительных изменений стромы, деструкция тиреоцитов и выход их содержимого (коллоида) в перифолликулярное пространство [31, 36]. Это сопровождается инфильтрацией ткани ЩЖ лимфоцитами, макрофагами и гигантскими клетками. Формируются гранулемы с характерной структурой [21, 31]. Заключительной стадией развития тиреоидита Де Карвена является соединительно-тканное замещение участков деструкции тиреоидной паренхимы с образованием очагов фиброза.
Чаще всего тиреоидит Де Карвена встречается у женщин в возрасте 40-50 лет [5, 8, 12]. Симптоматика этого заболевания не столь характерна, чтобы только на основании клинических данных установить правильный диагноз. Заболевание может начинаться остро, с повышения температуры тела до фибрильной и появления болей в области шеи. Реже тиреоидит Де Карвена развивается постепенно, сопровождаясь недомоганием, неприятными ощущениями при глотании, болезненностью при поворотах или наклонах головы.
Ранними признаками тиреоидита Де Карвена являются: дискомфорт при глотании, общее недомогание, болезненность в области щитовидной железы. Стадия развернутой клинической симптоматики характеризуется интенсивными болями в области шеи с иррадиацией в нижнюю челюсть, затылочную область. Боли усиливаются во время поворотов головы, при жевании и глотании. Отмечаются интенсивная потливость, сердцебиение, бессоница, артралгия.
При пальпации щитовидная железа может быть умеренно увеличена в размерах, плотная, болезненная. Регионарные лимфоузлы обычно не увеличены. У большинства больных в начальном периоде заболевания наблюдаются явления тиреотоксикоза [1,4, 8, 36].
В распознавании тиреоидита Де Карвена определенное значение приобретают данные лабораторных исследований [2, 3, 5, 7]. При общем анализе крови у этих больных обычно отмечаются признаки воспали-

2 80
тельного процесса: увеличение СОЭ и лимфоцитоз. В сыворотке крови появляются неспецифические маркеры острой воспалительной реакции. Для тиреоидита Де Карвена характерно также возрастание уровня содержания тироксина и трийодтиронина крови [11, 13, 17]. Это связывают с массивным выходом гормонов из деструктивно измененныхтиреоцитов [31, 36]. Одновременно у части больных отмечается резкое возрастание в крови тиреоглобулина [2, 3, 36]. В последние годы появились сообщения о появлении в крови больных тиреоидитом Де Карвена аутоантител к тиреоглобулину и микросомальной фракции ЩЖ [1, 4, 8].
Описанные изменения не являются абсолютно патогномоничными для подострого гранулематозного тиреоидита. Данные лабораторных исследований могут быть использованы лишь в качестве дополнительных критериев в диагностике данного заболевания.
Окончательный диагноз тиреоидита Де Карвена формулируется, обычно, при цитологическом изучении аспиратов из тканищитовиднойжелезы[12, 14,21].
Идентификация в мазках гигантских клеток, содержащих большое количество ядер, является основанием для верификации подострого гранулематозного тиреоидита. Следует, однако, отметить, что выполнение тонкоигольной аспирационной биопсии без применения специальных методов контроля за пункционной иглой позволяет не во всех случаях получить адекватный для цитологического анализа материал. Пальпаторно установить расположение гранулем при тиреоидите де Карвена не всегда представляется возможным. Значительные трудности возникают и на этапе получения материала из гранулемы, если биопсия выполняется «вслепую» [21, 36]. В этих случаях диагностически более эффективным является применение тонкоигольной пункционной биопсии, выполненной под эхоскопическим контролем. Показано, что информативность УЗ-ТПАБ в диагностике тиреоидита Де Карвена значительно превышает аналогичный показатель «слепых» биопсий.
По мере накопления опыта применения УЗ-ТПАБ при подостром гранулематозномтиреоидите былиполученыновыеданные об эхосемиотике этого заболевания [12, 14, 17, 35]. На ультрасоно-
граммах идентифицируются изменения ЩЖ в виде диффузного снижения эхогенности тиреоидной паренхимы [11, 12, 35], увеличения размеров ЩЖ у части больных [13, 14, 17] и появлении в тиреоидной паренхиме гипоэхогенных участков различных размеров и формы [12, 17, 35]. Последние представляют собой ультрасонографический эквивалент гранулем, развивающихся при тиреоидите Де Карвена [21]. Такое заключение подтверждается и результатами проведенного нами исследования.
Под нашим наблюдением находилось 3 больных (все — пациентки в возрасте 35-40 лет), у которых в ходе клинико-лаборатор- ных исследований был установлен диагноз подострого гранулематозного тиреоидита Де Карвена. При выполнении ультразвукового исследования у всех больных было установлено увеличение размеров и объема ЩЖ с диффузным снижением эхогенности тиреоидной паренхимы (рис. 232). У двух из них на ультрасонограммах визуализировались локусы отчетливого снижения акустической плотности. В мазках из аспиратов, полученных с помощью УЗ-ТПАБ, во всех трех случаях были идентифицированы гигантские многоядерные клетки (цитологическое исследование выполнено доктором мед.наук Н.Ю.Полонской).
Таким образом, ультразвуковое исследование,дополняемоерезультатами УЗ-ТПАБ,являетсядиагностическиэф- фективным методом для верификации подострогогранулематозноготиреоидита де Карвена. Данные, полученные с по-
Рис.232. Ультрасонограмма больной Ж., 29 лет.
Диагноз: подострый тиреоидит де Карвена. ЩЖ увеличенного размера. Визуализируются множественные гипоэхогенныеучастки, расположенные по всей паренхиме органа. УЗ-ТПАБ — гигантские многоядерные клетки в аспирате,

мощью тонкоигольной аспирационной биопсии, выполненной под эхоскопическим контролем, могут быть использованы для дифференциальной диагностики этого редкого заболевания от аутоиммунного тиреоидита Хашимото [8, 16] и диффузного токсического зоба [10, 27, 36].
Безболевой подострый тиреоидит —
возникает обычно спорадически или после родов [22, 23, 28]. Его особенностью является отсутствие болевого синдрома [7, 30]. Безболевой подострый тиреоидит проявляется симптомами тиреотоксикоза у 30-40% больных [9, 18, 26, 38] и гипотиреоза — у 25-40% [22, 23, 28, 30]. Характерной особенностью безболевого послеродового тиреоидита, сопровождающего симптомами тиреотоксикоза, является относительно низкий уровень накопления 1311 щитовидной железой на радионуклидных сцинтиграммах [9, 18, 26]. Этот признак служит основным критерием в дифференциальной диагностике безболевого тиреоидита от ранних стадий диффузного токсического зоба [22, 23].
В происхождении безболевого послеродового тиреоидита важную роль играют аутоиммунные нарушения [20, 29, 33, 39]. У больных обычно отмечается нерезко выраженное возрастание концентрации тироксина и трийодтиронина в крови [18, 26, 38], повышение титра аутоантител к тиреоглобулину [20, 22] и микросомальной фракции ЩЖ [39]. Аналогичные изменения происходят также у больных подострым гранулематозным тиреоидитом Де Карвена [2, 3, 5] и у пациенток на ранних стадиях ДТЗ [10]. Это диктует необходимость проведения дифференциальной диагностики послеродового тиреоидита. Применение ультразвукового исследования в этих случаях позволяет получить ценную информацию [25, 32].
Нами было выполнено ультразвуковое исследование щитовидной железы у 2-х
281
пациенток с послеродовым безболевым тиреоидитом. На ультрасонограммах отмечалось диффузное увеличение линейных размеров и объема ЩЖ И-й степени. При этом визуализировались незначительное снижение эхогенности тиреоидной паренхимы и гипоэхогенные участки с нечеткими контурами. Выполнение УЗ-ТПАБ этим больным позволило исключить диагноз злокачественной опухоли (цитологическое исследование выполнено в лаборатории патоморфологии МРНЦ РАМН). В отличие от больных с подострым гранулематозным тиреоидитом Де Карвена, в мазках больных послеродовым тиреоидитом отсутствовали лимфоциты и гигантские клетки. Дифференциально-диаг- ностическим критерием для отличительного разграничения безболевого тиреоидита от ранних стадий диффузного токсического зоба являются данные радионуклидного сканирования: у больных ДТЗ отмечается возрастание уровня накопления "тТс-пертех- нетата, а у больных с послеродовым тиреоидитом — уменьшение скорости поглощения радиофармпрепарата тиреоидной паренхимой.
В целом, результаты наших наблюдений согласуются с выводами других авторов о роли ультрасонографии в диагностике безболевого тиреоидита [15, 25, 32, 38]. Этот метод не имеет самостоятельного значения при распознавании данного заболевания. Однако признаки незначительного увеличения размеров и объема ЩЖ и нерезко выраженное диффузное снижение эхогенности тиреоидной паренхимы при относительно низком уровне тироксина крови позволяют исключить диагноз ДТЗ и подострого тиреоидита Де Карвена. Дополнительные свидетельства в пользу послеродового тиреоидита могут быть получены в процессе динамического наблюдения за пациентками.
ЛИТЕРАТУРА
1. Балаболки» М.И., Арион В.Я., Сакаева Н.А. |
ненияприподостромтиреоидите.Врачеб.дело,1986, |
Иммунокорригирующаятерапияаутоиммунногоипо- |
N8, стр.59. |
достроготиреоидита.Сов.мед., 1989,N6,стр.106. |
3. ЕпишинА.В., Свидер И.О. Т, В — лимфоциты |
2. Епишин А.В., Свидер И.О. Иммунные изме- |
приподостромтиреоидите.Сов.мед.,1987,N10,стр. |

283
7.3. ДИФФУЗНЫЙ ТОКСИЧЕСКИЙ ЗОБ
Диффузный токсический зоб (ДТЗ) — широко распространенное заболевание, чаще встречающееся у женщин в возрасте 30-50 лет [5, 6, 11]. В отечественной и немецкой литературе для обозначения ДТЗ часто используют термин «базедова болезнь» — по имени врача из г.Мерзебурга, в 1840 году опубликовавшего сообщение о четырех больных с характерной триадой симптомов
— зобом, «пучеглазием» и тахикардией. В англо-американской литературе ДТЗ предпочитают называть по имени Graves — автора, за пять лет до Basedow'a описавшего больных с тахикардией и экзофтальмом. На патогенетическую связь между увеличением размеров ЩЖ и клиническими проявлениями ДТЗ впервые указал немецкий врач P.J.Mobius в 1886 году. С этого периода были начаты и продолжаются до сих пор целенаправленные исследования по изучению патогенеза диффузного токсического зоба. На этой основе разрабатываются методы диагностики и лечения данного заболевания.
Согласно современным представлениям, при ДТЗ происходит резкое возрастание скорости синтеза и секреции тиреоидных гормонов гиперплазированными клетками щитовидной железы [7, 12, 25]. Ведущая роль гиперпродукции тироксина и трийодтиронина в развитии симптомов тиреотоксикоза при ДТЗ подтверждена как в опытах на экспериментальных моделях [13, 20, 38], так и результатами лечения этого заболевания. Оперативные вмешательства на ЩЖ [12, 24, 33], а также адекватно выполненные радиойод— и(или) химиотерапия приводят к исчезновению или значительному уменьшению степени выраженности симптомов тиреотоксикоза [19, 31], снижению концентрации тироксина в крови [8, 49, 60] и улучшению качества жизни больных [8, 31, 49]. Лечебный эффект радионуклидов и тиреостатиков проявляется тем в большей степени, чем на более ранней стадии ДТЗ был проведен курс лечения [25, 32, 44, 46]. Это является основанием для разработки и совершенствования инструментальных и лабораторных методов диагностики ДТЗ.
Распознавание поздних стадий этого заболевания не встречает каких-либо затруднений [5, 6, 11]. Сочетание таких симптомов, как стойкая тахикардия, похудание при повышенном аппетите, диффузное увеличение щитовидной железы, экзофтальм, повышенная потливость, дрожание пальцев вытянутых рук (симптом Шарко-Мари) и большая пульсовая амплитуда при измерении артериального давления представляют собой патогномоничные признаки ДТЗ. Однако на ранних стадиях, когда клинические проявления тиреотоксикоза выражены не столь отчетливо, решающую роль приобретают данные лабораторных и инструментальных методов. В зависимости от целевого назначения, их можно схематично разделить на три основные группы:
1) определение характера и степени выраженности гормональных нарушений;
2)измерение титра аутоантител к макромолекулярным компонентам тиреоцитов;
3)оценка морфофункционального состояния ЩЖ с помощью методов диагностической радиологии.
а) Методы оценки гормональных сдвигов вдиагностикеДТЗ. Для этой цели применяют радиоиммунологическое и иммуноферментное измерение тироксина, трийодтиронина, ТСГ и тиреолюберина в крови [2, 33, 56, 63]. Патогномоничным признаком ДТЗ является резкое возрастание концентрации в крови тиреоидных гормонов [5, 6, 11], не сопровождающееся активизацией центрального звена нейро-эндок- ринной регуляции ЩЖ-гипоталамо-гипофи- зарной системы [10, 63]. Показано, что при ДТЗ, в отличие от тиреотоксикозов другого происхождения, уровень ТСГ и тиреолюберина обычно не превышает возрастные нормативы. В настоящее время считается абсолютно доказанным, что в основе резкого возрастания тироксина и трийодтиронина крови у больных ДТЗ лежат аутоиммунные нарушения [1,3, 11, 15, 65].
б) Методы определения циркулирующих аутоантител к ЩЖ. В 1958 году D.D.Adams с соавторами выявил в крови больных ДТЗ новый фактор: «длительно дей-
