
5 курс / Госпитальная педиатрия / Gurova_Lechebnoe_pitanie_detej_v_kriticheskix_sostoyaniyax
.pdf
Л е к ц и я
Лечебное питание детей в критических состояниях: современные подходы
å.å.ÉÛ Ó‚‡, Ö.à.í͇˜ÂÌÍÓ
ë‡ÌÍÚ-èÂÚ ·Û „Ò͇fl „ÓÒÛ‰‡ ÒÚ‚ÂÌ̇fl ωˈËÌÒ͇fl ‡Í‡‰ÂÏËfl ËÏ. à.à.å˜ÌËÍÓ‚‡
В лекции описаны особенности метаболизма у детей при критических состояниях: простом голодании и голодании при острой стрессовой реакции. Авторами представлены обоснованные подходы к выбору способов нутритивной поддержки пациентов, которая может осуществляться как специальными смесями для энтерального питания, так и растворами для парентерального питания. Одной из таких смесей для энтерального питания является «Берламин®Модуляр» (Berlin-Chemi, Германия). На примере указанной смеси представлены особенности состава полимерных сбалансированных смесей, использующихся для нутритивной поддержки больных детей.
Ключевые слова: метаболизм, критические состояния, голодание, дети, энтеральное питание
Dietotherapy of children in critical states:
Modern approaches
M.M.Gurova, E.I.Tkachenko
I.I.Mechnikov St.Petersburg State Pediatric Medical Academy
The lecture describes metabolic features in children in critical states: ordinary starvation and starvation under acute stressful reaction. The authors have presented valid approaches to choice of means of nutritious support of patients, which may be carried out both with special formulas for enteral feeding and with solutions for parenteral feeding. One of such formulas for enteral feeding is «Berlamin®Modular» (Berlin-Chemie, Germany). Composition features of balanced polymeric formulas using for nutritious support of sick children have been presented by the example of this formula.
Key words: metabolism, critical state, starvation, children, enteral feeding
Актуальность проблемы организации адекватной нутритивной поддержки связана с необходимостью поддер-
жания трофологического гомеостаза, являющегося основой существования организма как биологической системы.
В то же время при лечении пациентов в условиях развития острой стрессовой реакции врач сталкивается с проблемой несоответствия между значительным возрастанием потребностей организма в энергии и нутриентах при резком ограничении пищевой активности больного, снижении функциональных возможностей кишечника в усвоении нутриентов. Данная проблема усугубляется тем, что в случае болезни дети значительно сильнее, чем взрослые страдают при ограничении питания, что связано с рядом анатомо-физио- логических особенностей детского организма:
• небольшая масса (меньшие запасы питательных веществ);
Для корреспонденции:
Ткаченко Евгений Иванович, доктор медицинских наук, профессор, заведующий кафедрой пропедевтики внутренних болезней с курсом гастроэнтерологии и эндоскопии Санкт-Петербургской государственной медицинской академии им. И.И.Мечникова, главный гастроэнтеролог Комитета по здравоохранению Правительства Санкт-Петербурга
Адрес: 195067, Санкт-Петербург, Пискаревский пр., 47 Телефон: (812) 543-9538
Статья поступила 23.06.2004 г., принята к печати 05.10.2004 г.
•быстрые темпы роста, приводящие к повышенной потребности в энергии и пищевых субстратах;
•изменяющаяся потребность в нутриентах в разные возрастные периоды;
•незрелость нервной, эндокринной, иммунной систем организма;
•функциональная незрелость органов и систем;
•функция желудочно-кишечного тракта (ЖКТ) у детей нарушается сильнее, чем у взрослых, приводя к снижению переваривающей способности, абсорбции и метаболизма нутриентов.
Кроме того, при тяжелых заболеваниях изменения пищевого поведения детей (больные не могут или не хотят принимать пищу) встречаются значительно чаще.
Вышеизложенные особенности легли в основу общих требований к нутритивной поддержке при проведении неотложных лечебных мероприятий:
1. Соответствие питания принципу физиологической адекватности.
2. Оптимизация процессов интрагастрального и интраинтестинального пищеварения и всасывания пищевых нутриентов.
Материал подготовлен к печати к.м.н. С.Н.Денисовой.
28

гВ˜В·МУВ ФЛЪ‡МЛВ ‰ВЪВИ ‚ Н ЛЪЛ˜ВТНЛı ТУТЪУflМЛflı: ТУ‚ ВПВММ˚В ФУ‰ıУ‰˚
3.Дополнительное обеспечение организма макро-, микронутриентами и энергией.
4.Индивидуальное питание в соответствии с характером заболевания, сопутствующей патологией, исходным нутритивным статусом ребенка.
Наряду с этим необходима коррекция питания ребенка в зависимости от фазы течения патологического процесса, так как потребности организма в катаболическую фазу (период выраженных метаболических сдвигов и максимального использования адаптационных резервов) и анаболическую фазу (период активации репаративных процессов) различаются.
Все это необходимо учитывать при выборе способа нутритивной поддержки, которая может осуществляться как специальными смесями для энтерального питания (ЭП), так и растворами для парентерального питания (ПП). В настоящее время все больше внимания уделяется возможностям ЭП в связи с тем, что оно более физиологично, безопасно, доступно и экономично по сравнению с ПП. В то же время понимание возможностей каждого из этих методов, знание показаний и противопоказаний поможет устранить проявления белково-энергетической недостаточности, ограничить катаболическую реакцию организма в раннем постагрессивном периоде, снизить частоту инфекционных осложнений и уровень летальности.
Нарушение обмена веществ при развитии критических состояний
При развитии критических состояний происходит значительное изменение метаболических процессов, направленных на поддержание существования организма в новых, крайне неблагоприятных условиях, требующих максимального напряжения всех компенсаторных возможностей. В силу ряда анатомо-физиологических особенностей, включающих незрелость регулирующих систем, барьерных механизмов, систем детоксикации, проблема поддержания энергообеспечения детского организма, предотвращения развития кишечной недостаточности является такой же важной задачей, как и поддержание функции жизненноважных органов. В этих условиях адекватное проведение нутритивной поддержки необходимо для более быстрого восстановления функциональных возможностей с минимальными негативными последствиями для роста и дифференцировки растущих тканей.
При развитии острой стрессовой ситуации отмечается значительное увеличение потребностей организма в энергии и нутриентах. Изменение трофологического гомеостаза происходит в условиях несоответствия чрезмерной активации стресс-реализующих систем, приводящих к напряжению функционирования жизненноважных органов, и степени включения адаптационных механизмов. Эта особенность обусловливает различие метаболических изменений в условиях голодания при стрессе и простого голодания.
Простое голодание является результатом частичного или полного прекращения поступления энергетических субстратов в организм. Голодание может быть кратковременным (менее 72 ч) и длительным (более 72 ч). В результате мобилизации адаптационных резервов за периодом экстренной адаптации следует период, характеризующийся переходом на энергетически более экономные пути регуляции, что позволя-
|
|
|
|
|
|
|
Изменение гормональной |
Голодание |
|
|
Снижение |
|
|
|
регуляции (снижение уровня |
|
|
уровня глюкозы |
|
|
инсулина, повышение уровня |
||
|
|
|
|
|
|||
|
|
|
|
|
|
|
глюкагона) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Мобилизация из депо АК и жирных кислот
Усиление окисления
Усиление глюконеогенеза
свободных жирных кислот
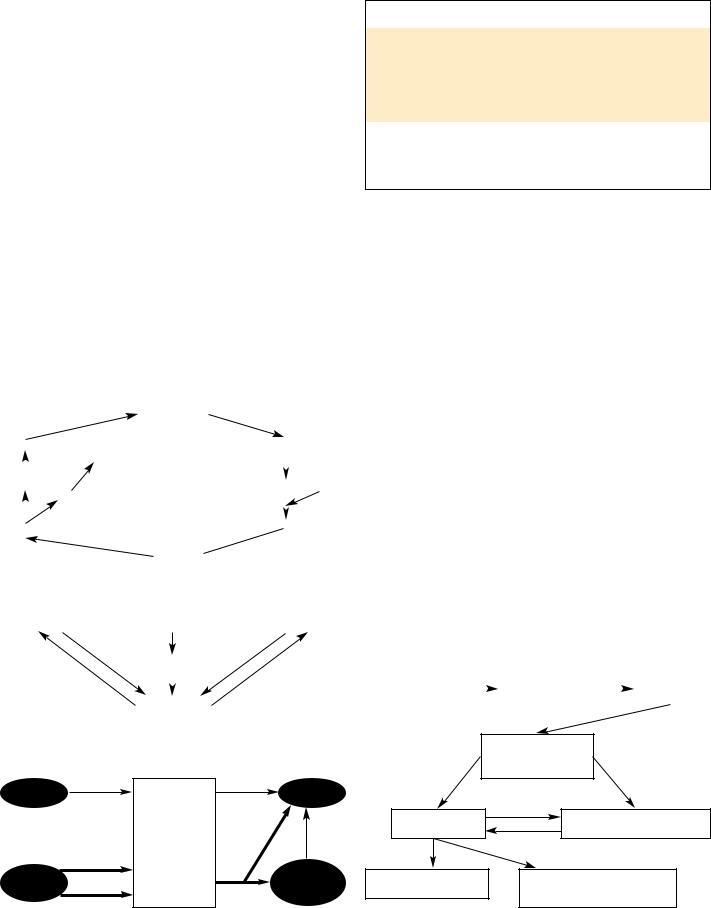
Рис. 1. Этапы быстрой энергетической адаптации при голодании.
ет поддерживать энергообеспечение жизненноважных органов и систем на относительно удовлетворительном уровне.
Основными компенсаторными механизмами, развивающимися при голодании, являются:
•снижение расхода энергии за счет уменьшения интенсивности основного обмена;
•в первые 24 часа расходуются запасы глюкозы, как источника энергии. В дальнейшем образование глюкозы происходит за счет активации глюконеогенеза;
•глюкоза, образующаяся в результате глюконеогенеза, обеспечивает энергией только глюкозозависимые ткани – мозг, эритроциты, костный мозг, периферические нервы, медуллярную ткань почек, остальные органы и ткани обеспечиваются энергией за счет окисления жирных кислот;
•при кратковременном голодании преимущественным источником энергии являются белки;
•при длительном голодании основным источником энергии становятся жиры, использование белков ограничивается
всвязи с необходимостью поддержания структуры и функции организма, так как потеря более 30% мышечной массы приводит к смерти;
•в случае продолжающегося голодания глюкозозависимые ткани, прежде всего мозг, начинают метаболизировать продукты окисления жирных кислот – кетоновые тела.
Процесс экстренной адаптации при голодании выглядит следующим образом (рис. 1, 2): расходование запасов гликогена приводит к снижению уровня глюкозы, изменению концентрации инсулина и глюкагона, последующей мобилизации аминокислот (АК), в первую очередь аланина из мышечной ткани, и повышению уровня свободных жирных кислот за счет жировых депо. В результате происходит усиление глюконеогенеза (энергообеспечение мозга и других глюкозозависимых тканей) и окисление жирных кислот (источник энергии для остальных тканей).
Мышцы |
АК |
|
|
|
|
|
Мозг |
|
|
|
|
|
|
||||
|
|
|
|
|
|
|||
|
|
Печень |
Кетоновые |
|||||
|
|
|
|
|
|
|||
|
|
|
|
|
Глюкоза |
|||
|
|
|
|
|
||||
|
|
|
тела |
|
|
|||
|
|
|
(глюконеогенез |
|
|
|||
|
|
|
|
|
|
|||
|
Жирные |
|
|
|
|
|
|
|
|
|
90%) |
|
|
|
|
|
|
|
кислоты |
|
|
|
|
|
|
|
|
|
|
|
|
|
Почки |
||
Источники |
|
|
|
|
|
|||
|
|
|
|
|
|
|||
|
|
|
|
|
|
|||
|
|
|
|
|
(глюконеогенез |
|||
жира |
|
|
|
|
|
|||
|
|
|
|
|
10%) |
|||
|
Глицерол |
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Рис. 2. Особенности метаболической адаптации на ранних фазах
голодания.
29
е.е.ЙЫ У‚‡, Ц.а.нН‡˜ВМНУ / ЗУФ УТ˚ ‰ВЪТНУИ ‰ЛВЪУОУ„ЛЛ, 2004, Ъ. 2, ‹5, Т. 28–45
На ранних фазах голодания повышается мобилизация АК из мышц (аланин), жирных кислот и глицерола из жировых депо, усиливается глюконеогенез (90% его осуществляется в печени, 10% – в почках). Мозг помимо глюкозы как основного источника энергии начинает метаболизировать кетоновые тела.
При кратковременном голодании основным субстратом для глюконеогенеза становится аланин. Превращение аланина в глюкозу происходит в глюкозоаланиновом цикле, через промежуточное образование пирувата (рис. 3). При этом аланин является единственной АК в человеческом организме, имеющей прямую корреляцию с содержанием пирувата.
Дополнительными субстратами для глюконеогенеза являются лактат, конечный продукт гликолиза (участвует в синтезе глюкозы в цикле Кори), и глицерол, образующийся при гидролизе триглицеридов (рис. 4).
При продолжающемся голодании происходят следующие компенсаторные изменения метаболизма: уменьшается распад белка, снижаются интенсивность глюконеогенеза и общий уровень метаболизма, повышается утилизация мозгом кетоновых тел, образующихся в результате окисления жирных кислот. Повышение содержания кетоновых тел является поворотным этапом метаболизма при голодании, в связи с
|
Печень |
|
Мышцы |
|
|
|
|
Глюкоза крови |
|
||
|
|
|
|
|
|
Глюкоза |
|
Глюкоза |
|
||
|
Мочевина |
|
|
|
|
|
|
|
|
|
|
|
|
|
Пируват |
|
|
Пируват |
|
NH2 |
|||
|
NH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Аланин |
|
|
|
|
|
|
|
|
Аланин 
Рис. 3. Глюкозоаланиновый цикл.
Лактат |
|
Триглицериды |
|
АК |
|
|
|
|
|
Таблица 1. Метаболические изменения, характерные для крат-
ковременного и длительного голодания
Кратковременное |
Основным источником энергии являются белки |
(менее 72 ч) |
Интенсификация глюконеогенеза |
голодание |
Глюконеогенез происходит преимущественно в печени (90%) |
|
Основным субстратом для глюконеогенеза является аланин |
|
Основным энергетическим субстратом для головного |
|
мозга является глюкоза |
Длительное |
Основным источником энергии являются жиры |
(более 72 ч) |
Интенсивность глюконеогенеза снижается |
голодание |
Глюконеогенез происходит преимущественно в почках |
|
Основным субстратом для глюконеогенеза становится |
|
глутамин |
|
Основным энергетическим субстратом для головного |
|
мозга становятся кетоновые тела |
|
|
тем что кетоновые тела блокируют полное окисление глюкозы, инактивируя пируватдегидрогеназу (фермент, необходимый для глюконеогенеза). В результате этого головной мозг переключается с метаболизма глюкозы в качестве энергетического субстрата на кетоновые тела, что уменьшает катаболизм белка (рис. 5).
Из приведенной схемы следует, что при продолжающемся голодании образуется некоторое количество глюкозы, однако в отличие от кратковременного голодания основным органом глюконеогенеза становятся почки, а основным субстратом для образования глюкозы – глутамин.
Суммарно основные изменения в разные периоды голодания представлены в табл. 1.
В том случае, если голодание продолжается, на фоне истощения источников жира вновь начинается катаболизм белков, в который вовлекаются структурные белки жизненноважных органов, что приводит к гибели организма.
Критические состояния – состояния, возникающие в результате воздействия особо вредных внешних факторов (травма, ожоги, оперативные вмешательства) или при неблагоприятном развитии уже имеющегося патологического процесса (сепсис, острый панкреатит), приводящие к грубым расстройствам метаболизма и жизненноважных физиологических функций, представляющие непосредственную угрозу для жизни пациента.
Развитие метаболического стресса, независимо от этиологического фактора, имеет сходные особенности системных реакций организма, выраженность которых во многом
Цикл Кори |
Глицерол |
Цикл |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
аланиновый |
Стрессорный |
|
|
Афферентные |
|
|
Гипоталамус |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
фактор |
|
|
пути |
|
|
||
|
|
|
|
|
|
|
|
|
|||
|
Глюкоза |
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
Рис. 4. Основные субстраты для глюконеогенеза. |
|
|
Эфферентные пути |
||
|
|
|
|
|
|
|
|
|
|
|
(стресс-реализующие |
АК |
|
|
|
|
системы) |
|
|
|
|
|
|
(аланин) |
|
Глюкоза |
Мозг |
|
|
Мышцы |
|
|
|
|
|
|
|
|
|
Системный ответ |
Местный ответ |
|
Печень |
|
Глюкоза |
(повышение синтеза цитокинов) |
|
|
|
|
|||
|
(глюконеогенез |
|
|
|
|
Жирные |
Кето- |
|
|
|
|
55%) |
|
|
|
||
кислоты |
новые |
|
|
|
|
|
Почки |
|
|
||
Источники |
|
тела |
Активация симпатической |
Активация эндокринной системы |
|
жира |
|
|
(глюконеогенез |
нервной системы |
(гипоталамо-гипофизарно- |
|
|
45%) |
|||
Глицерол |
|
|
|
надпочечниковая ось) |
|
|
|
|
|
||
|
|
|
|
|
|
Рис. 5. Метаболическая адаптация при продолжающемся голо- |
Рис. 6. Регуляторные изменения, происходящие в организме, в |
||||
дании, направленная на сохранение запасов белка. |
ответ на действие стрессорного фактора. |
||||
30
гВ˜В·МУВ ФЛЪ‡МЛВ ‰ВЪВИ ‚ Н ЛЪЛ˜ВТНЛı ТУТЪУflМЛflı: ТУ‚ ВПВММ˚В ФУ‰ıУ‰˚
обусловлена состоянием нутритивного статуса к моменту развития критического состояния. Так, на начальном этапе основное значение приобретает нейроэндокринный ответ, обеспечивающий быструю адаптацию организма к стрессу (рис. 6).
Активация афферентных путей связана с раздражением болевых, сенсорных (зрительных, слуховых, обонятельных)
ивисцеральных (баро- и хеморецепторов, рецепторов растяжения) рецепторов. Переработка афферентных сигналов
иподготовка к эфферентному ответу происходит на разных уровнях центральной нервной системы (ЦНС), однако основную интегрирующую роль в его осуществлении играет
Таблица 2. Характеристика основных эфферентных путей в ре-
ализации стрессового ответа.
Симпатическая |
• повышение частоты пульса, |
нервная система |
• периферическая вазоконстрикция, |
|
• гипергидроз, |
|
• замедление гастроинтестинальной моторики, |
|
• гипергликемия |
Адреналин, |
• немедленный кардиоваскулярный, |
норадреналин |
гастроинтестинальный ответ и реакция со стороны |
|
ЦНС, |
|
• стрессиндуцированная супрессия выделения |
|
инсулина из поджелудочной железы, |
|
• периферическая резистентность клеток к инсулину |
|
(нарушается его захват), |
|
• стимуляция секреции глюкагона |
Гормоны гипофиза |
|
Передний гипофиз: |
Повышение синтеза кортикостероидов: |
АКТГ |
• восстанавливают объем экстрацеллюлярной жидкости |
|
• напрямую действуют на жировую ткань: активируют |
|
высвобождение свободных жирных кислот |
|
• способствуют развитию гипергликемического |
|
состояния за счет мобилизации АК из скелетной |
|
мускулатуры, стимуляции продукции глюкагона |
СТГ |
Напрямую или через соматомедины |
|
• тормозит действие инсулина |
|
• уменьшает захват глюкозы мышечной тканью |
|
• повышает уровень свободных жирных кислот |
|
за счет стимуляции липолиза в жировой ткани |
|
• повышает поступление АК в ткани при возобновлении |
|
адекватного орального питания (анаболический |
|
эффект) |
ТТГ |
Повышает потребление кислорода и уровень |
|
метаболизма |
Задний гипофиз: |
|
АДГ |
• уменьшает клиренс свободной воды и выделение |
|
мочи |
|
• вызывает высвобождение глюкагона и снижение |
|
уровня инсулина (прямое влияние на островковые |
|
клетки поджелудочной железы) |
Ренин-ангиотензин- |
Развитие гипонатриемии, гиперволемии, алкалоза |
альдостероновая |
|
система |
|
Цитокины: |
Вырабатываются различными типами клеток в месте |
|
действия повреждающего фактора или инфекции |
|
Помимо местного воздействия вызывают |
|
генерализованные системные эффекты и действуют |
|
как «раневые гормоны» |
ИЛ1 |
• стимулирует гранулопоэз |
|
• индуцирует лихорадку |
|
• повышает синтез белков в острой фазе |
ТНФα |
• вызывает гиперинсулинемию |
• действует на гипоталамус, дополняя и усиливая |
|
|
работу других афферентных путей нервной системы |
|
• основной фактор, опосредующий действие |
|
эндотоксина |
|
• регулирует энергообмен и белковый метаболизм |
|
в мышцах, прямо влияет на липолиз и продукцию |
|
белков острой фазы в печени |
|
• необходим для миграции и активации нейтрофилов |
|
• является потенциальным фактором ангиогенеза |
|
|
Стресс
Активация стрессреализующих систем
|
Повышение уровня |
|
|
|
Понижение уровня |
|
||
|
глюкагона |
|
|
|
инсулина |
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
• усиление глюконеогенеза |
|
|
|
• гипергликемия |
||||
• усиление липолиза |
|
|
|
• нарушение синтеза белка |
||||
• повышенное высвобождение |
|
|
|
• развитие отрицательного |
||||
свободных жирных кислот |
|
|
|
азотистого баланса |
||||
из жировых депо |
|
|
|
• уменьшение липогенеза |
||||
•повышенный катаболизм мышечной ткани с высвобождением АК, которые становятся субстратами глюконеогенеза
Рис. 7. Метаболические изменения, возникающие в начальной
фазе острой стрессовой реакции.
гипоталамус. Эфферентный ответ реализуется через активацию нервной и эндокринной систем с повышением активности симпатической нервной системы, высвобождением гипофизарных гормонов (адренокортикотропный гормон – АКТГ, гормон роста и антидиуретический гормон – АДГ) и повышением синтеза цитокинов (табл. 2). При этом ведущее значение в острой фазе стресса отводится нервной системе, как системе быстрого реагирования, тогда как цитокиновый ответ является по времени отсроченным. Метаболические эффекты активации стресс-реализующих систем во многом связаны с изменениями содержания инсулина и глюкагона (рис. 7).
Таким образом, при ограниченном поступлении основных пищевых веществ и энергии метаболическая адаптация в условиях стресса направлена на обеспечение органов и тканей организма энергией и структурными субстратами за счет утилизации собственных запасов. Этот процесс опосредуется активацией стресс-реализующих систем (адренергической, гипоталамо-гипофизарной системы, цитокинов и других локальных медиаторов), приводящих к повышению уровня катаболических гормонов (глюкагона, катехоламинов, кортикостериодов). В результате происходит усиление глюконеогенеза, для которого субстратами становятся белки мышечной ткани, и развитие гипергликемии как необходимого условия для энергообеспечения тканей в условиях кислородного голодания.
Вто же время при сохраняющемся патологическом процессе адаптация в критических состояниях приводит к состоянию гиперкатаболизма, в результате чего происходит развитие выраженной белково-энергетической недостаточности.
Вусловиях гиперкатаболизма метаболизм основных нутриентов изменяется следующим образом.
Характеристика метаболизма глюкозы при простом голодании и голодании в условии развития острой стрессовой реакции представлена в табл. 3.
Происходит усиление синтеза глюкозы в печени, обусловленное тем, что глюкоза как энергетический субстрат может метаболизироваться в условиях гипоксии. Главными потре-
31

е.е.ЙЫ У‚‡, Ц.а.нН‡˜ВМНУ / ЗУФ УТ˚ ‰ВЪТНУИ ‰ЛВЪУОУ„ЛЛ, 2004, Ъ. 2, ‹5, Т. 28–45
Таблица 3. Сравнительная характеристика метаболизма глюко-
зы при простом голодании и при голодании в условиях стресса
|
Простое голодание |
Стрессовая реакция |
Глюконеогенез |
↑ |
↑↑↑ |
Гликолиз |
↓ |
↑↑↑ |
Окисление глюкозы |
↓ |
↓ |
Обмен глюкозы |
↓ |
↑↑↑ |
|
|
|
Таблица 4. Сравнительная характеристика белкового метаболиз-
ма при простом голодании и при голодании в условиях стресса
|
Простое голодание |
Стрессовая реакция |
|
|
|
Липолиз в жировой ткани |
↑↑↑ |
↑↑ |
Окисление липидов |
↑↑↑ |
↑ |
Обмен жирных кислот |
↓ |
↑↑ |
Таблица 5. Сравнительная характеристика метаболизма жиров
при простом голодании и при голодании в условиях стресса
|
Простое голодание |
Стрессовая реакция |
|
|
|
Протеолиз |
↓ |
↑↑↑ |
Синтез белка |
↓ |
↑ |
Окисление АК |
↓ |
↑↑↑ |
бителями глюкозы являются головной мозг, иммунокомпетентные клетки, фибробласты, грануляционная ткань, ткани, пораженные патологическим процессом.
Особенности белкового метаболизма при простом голодании и голодании в критических состояниях отображены в табл. 4.
Основным ответом организма на стресс является системный катаболизм белков. При этом степень катаболизма белка при критических состояниях очень высока и может достигать 260 г в день, что соответствует дневной потере примерно 1 кг мышечной массы.
Кроме того, для этого состояния характерны следующие изменения: повышение синтеза белков в печени как следствие активации системы цитокинов; снижение синтеза альбумина; повышение транскапиллярных потерь альбумина.
В результате усиления глюконеогенеза возросшие знергетические потребности обеспечиваются за счет окисления жиров, которые являются главным энергетическим субстратом для печеночных клеток. При критических состояниях жиры не могут полностью метаболизироваться и это приводит к нарушению кетогенеза и повышенному синтезу провоспалительных лейкотриенов и цитокинов, повреждающих органы и системы (табл. 5).
Лабораторные и клинические показатели при простом голодании и голодании при стрессовых состояниях суммированы в табл. 6.
Гиперкатаболизм с развитием белково-энергетической недостаточности при критических состояниях сопровождается изменениями со стороны всех органов и систем организма.
При критических состояниях практически все гормональные и медиаторные изменения связаны с повышением уровня циклического аденозинмонофосфата (цАМФ) в лимфоидных клетках, что приводит к нарушению регуляции и снижению активности иммунной системы, определяемых как стрессиндуцированная иммунная дисфункция (табл. 7). В том случае, если у пациента имеет место белково-энерге- тическая недостаточность, предшествующая стрессу, то изменения со стороны иммунной системы характеризуются следующими особенностями:
Таблица 6. Различия между простым голоданием и голоданием
при стрессе
Показатель |
Простое голодание |
Стрессовое голодание |
|
|
|
Энергетические затраты |
Понижены |
Повышены |
Альбумин |
В норме |
Снижен |
Трансферрин |
Умеренно снижен |
Значительно снижен |
Преальбумин |
– « – |
– « – |
Масса тела |
Понижена |
Может быть нормальной |
|
|
за счет развития отека |
Общий жир тела |
Понижен |
Понижен |
Белок тела |
– « – |
– « – |
Общая вода |
Незначительно повышена |
Значительно повышена |
Внеклеточная вода |
– « – |
– « – |
Азотистый баланс |
Отрицательный |
Сильно отрицательный |
Показатели воспаления |
Нормальные |
Повышены |
|
|
|
Таблица 7. Влияние гормонов и медиаторов при остром стрессе
на цАМФ клеток лимфоидной ткани и иммунный ответ
Гормон/медиатор |
Изменения при |
Эффект |
Влияние |
|
остром стрессе |
на цАМФ |
на иммунный |
|
|
|
ответ |
|
|
|
|
Адреналин/норадреналин |
Повышается |
Повышает |
Снижает |
Кортикостероиды |
Повышаются |
Повышают |
Снижают |
Тиронин |
Снижается |
Снижает |
Снижает |
Инсулин |
Может снижаться |
Повышает |
– « – |
|
или повышаться |
|
|
Простагландин Е2 |
Повышается |
– « – |
– « – |
Гормон роста |
– « – |
Неизвестно |
Повышает |
Гистамин |
– « – |
Повышает |
Снижает |
•изменением функции клеточного звена иммунной системы с уменьшением процессов пролиферации в лимфатических органах, атрофией тимуса, селезенки и тимусзависимых зон в лимфатических узлах;
•уменьшением уровня Т-клеток в периферической крови;
•периферической лимфопенией;
•повышением уровня плазматических клеток;
•снижением функциональной активности В-клеток, даже при отсутствии количественных изменений, в связи с продукцией антител (АТ) с низкой аффинностью к специфическим антигенам (АГ).
Развитие стрессиндуцированной иммунной дисфункции приводит к появлению тяжелой инфекции у детей с нарушенным нутритивным статусом, вызванной оппортунистической грамотрицательной флорой.
Помимо изменений, связанных с развитием стресса, причиной дисфункции иммунной системы является дефицит определенных нутриентов – специфических АК, жирных кислот, витаминов, микроэлементов (табл. 8).
В связи с тем что катаболизм белка происходит прежде всего за счет скелетной мускулатуры, при критических состояниях отмечается значительное снижение мышечной массы. Белковое истощение влияет на структуру дыхательных мышц, приводя к уменьшению массы диафрагмальной мышцы и снижению силы дыхательных мышц. Развивающееся нарушение функции дыхания со снижением объема вентиляции легких у пациента увеличивает продолжительность искусственной вентиляции легких.
Неконтролируемый системный стресс является одной из причин развития полиорганной недостаточности как конечной стадии гиперметаболического ответа при критических состояниях. Развивающееся при этом острое повреждение легких (острый респираторный дистресс синдром), сердечно-сосудистой, почечной, печеночной систем, откло-
32

гВ˜В·МУВ ФЛЪ‡МЛВ ‰ВЪВИ ‚ Н ЛЪЛ˜ВТНЛı ТУТЪУflМЛflı: ТУ‚ ВПВММ˚В ФУ‰ıУ‰˚
Таблица 8. Влияние дефицита различных нутриентов на состоя-
ние иммунной системы
Нутриенты |
Влияние на иммунный ответ |
Дефицит АК с разветвленной цепью |
Нарушение лимфопоэза со снижением |
(изолейцина и, в особенности, |
тимической и периферической |
валина) |
популяции лимфоцитов |
Дефицит серосодержащих АК |
Истощение лимфоцитарного пула |
(метионина и цистеин-цистина) |
в тимусе, лимфатических узлах, |
|
селезенке |
Дефицит фенилаланина |
Нарушение нормального процесса |
и триптофана |
образования АТ, снижение уровня АТ |
Избыток ненасыщенных |
Угнетение образования АТ, |
и полиненасыщенных жирных |
уменьшение специфической |
кислот |
цитотоксичности и ингибирование |
|
митогенной активности |
Дефицит любых витаминов |
Вызывает гуморальные и клеточно- |
|
опосредованные иммунные дефекты |
Дефицит меди |
Нарушение адекватного ответа |
|
ретикулоэндотелиальной ткани |
|
на инфекцию |
Дефицит цинка |
Нарушение нормального |
|
функционирования Т-клеток, |
|
макрофагов и гранулоцитов |
|
|
нения со стороны ЖКТ являются ведущей причиной смерти в 75% случаев.
Однако если патофизиология легочной, сердечно-сосудис- той, почечной и печеночной недостаточности изучены достаточно давно, то особенности вовлечения ЖКТ при развитии критических состояний стали понятны только в последнее время.
В случае развития белково-энергетической недостаточности в первую очередь нарушается функция органов с интенсивными процессами обмена, к которым относится ЖКТ. Это связано с тем, что питание тонкой кишки на 50%, а толстой – на 80% обеспечивается за счет внутриполостного субстрата, который является мощным стимулом для роста и регенерации ее клеточных элементов.
При голодании отмечаются следующие изменения со стороны ЖКТ:
•нарастающие явления атрофии слизистой оболочки тонкой кишки;
•угнетение секреции пищеварительных желез ЖКТ;
•развитие синдрома избыточной колонизации тонкой кишки;
•истончение пристеночного слоя слизистых наложений и повреждение щеточной каемки энтероцитов;
•нарушение процессов внутриполостного, пристеночного, мембранного пищеварения;
•развитие дефицита субстратов, необходимых для регенерации кишечного эпителия (глутамина, кетоновых тел,
β-гидроксимасляной кислоты);
•снижение моторной активности ЖКТ.
При критических состояниях, в постагрессивном периоде, повреждение ЖКТ усугубляется воздействием следующих факторов:
•централизацией кровообращения, приводящей к развитию циркуляторной гипоксии и дефициту энергии клеток слизистой оболочки ЖКТ;
•усилением симпатических регуляторных влияний, неблагоприятно отражающихся на кишечной перистальтике, кровообращении, местных эндокринных и паракринных регулирующих механизмах;
•развития кишечного пареза, усиливающего водно-элек- тролитные нарушения.
|
|
Критическое |
|
|
Лечение |
||||
|
|
состояние |
|
|
|
антибиотиками |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
Мезентериальная гипоперфузия, |
|
Иммунодепрессия, |
|
||||||
развитие гипоэргоза слизистой |
|
метаболический |
|
||||||
оболочки кишечника |
|
иммунодефицит |
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Снижение колонизационной |
||
|
|
|
|
|
|
|
резистентности кишечника |
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Повреждение слизистой |
|
|
Развитие кишечного |
||
|
|
|
|
дисбактериоза с преобладанием |
|||
|
|
оболочки кишечника |
|
|
|||
|
|
|
|
грамотрицательных анаэробов |
|||
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Развитие синдрома острой |
|
|
Абсорбция и портальная |
||
|
|
|
|
транслокация микробов |
|||
|
|
кишечной недостаточности |
|
|
|||
|
|
|
|
и токсинов |
|||
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Развитие белково- |
|
|
Повреждение печени, развитие |
||
|
|
энергетической |
|
|
системной воспалительной |
||
|
|
|
|
||||
|
|
недостаточности |
|
|
реакции |
||
|
|
|
|
|
|
|
|
Полиорганная
недостаточность
Рис. 8. Последовательность развития патологических измене-
ний в ЖКТ при критических состояниях.
В результате нарушений основных функций ЖКТ развивается синдром острой кишечной недостаточности, который определяется как сочетанное нарушение двигательной, секреторной, переваривающей и всасывательной функций кишечника. На этом фоне происходит снижение барьерных свойств кишечной стенки с развитием восходящего дисбиоза, явлений эндогенной микробной интоксикации за счет повышенного образования биологически активных веществ, цитокинов и транзиторной транслокации микробов в кровь. Таким образом, развитие острой кишечной недостаточности замыкает порочный круг, поддерживая гиперкатаболизм и способствуя развитию полиорганной дисфункции (рис. 8).
Современные подходы к энтеральному питанию при критических состояниях
Выраженность гиперметаболического ответа при критических состояниях зависит не только от тяжести и характера патологического процесса, но и от адекватного питания в этот период. Кроме того, большое значение имеет исходное состояние нутритивного статуса, так как в случае его дефицита пациенты имеют меньшие адаптационные резервы в организме, большее число осложнений, повышенную летальность, более длительный срок пребывания в стационаре (табл. 9).
Таким образом, к основным целям нутритивной поддержки при проведении интенсивной терапии относятся поддержание трофологического гомеостаза, предотвращение развития острой кишечной недостаточности, поддержание тро-
33
е.е.ЙЫ У‚‡, Ц.а.нН‡˜ВМНУ / ЗУФ УТ˚ ‰ВЪТНУИ ‰ЛВЪУОУ„ЛЛ, 2004, Ъ. 2, ‹5, Т. 28–45
Таблица 9. Острофазовая реакция у пациентов с достаточным
питанием и у пациентов с тяжелой степенью недостаточности питания
Показатель |
Достаточное питание |
Недостаточное питание |
Катаболизм белка |
Соответствует |
Не соответствует |
|
потребностям |
потребностям |
Мышечная сила |
Адекватна |
Неадекватна |
|
заболеванию |
заболеванию |
Септические осложнения |
Редкие |
Частые |
Пролежни |
Редкие |
Появляются часто |
Заживление |
Нормальное |
Замедленное |
послеоперационной раны |
|
|
Пребывание в стационаре |
Обычное |
Длительное |
Реабилитационная |
Нормальная |
Ухудшенная |
способность |
|
|
|
|
|
фического гомеостаза тонкой кишки для предупреждения развития несостоятельности кишечного барьера и микробной агрессии кишечного происхождения, создание условий для процессов восстановления и роста тканей.
Для сохранения нормальной функции слизистой оболочки различных отделов кишечника, экзокринной функции поджелудочной железы и других желез пищеварительного тракта необходимо поступление питательных субстратов в просвет ЖКТ. Нутриенты, поступающие энтеральным путем, создают условия для роста и регенерации эпителия, нормализуют моторную активность ЖКТ, восстанавливают функциональную активность кишечника, способствуют нормализации выработки энтеральных гормонов.
Таким образом, ранняя и адекватная нутритивная поддержка больных в критических состояниях является необходимым условием для выживания пациента. В связи с тем что в интенсивной медицине нередко возникают ситуации, когда пациенты по тем или иным причинам не хотят, не могут или не должны получать питание естественным оральным путем, возникает необходимость в проведении искусственного лечебного питания (ИП).
Основными его принципами являются своевременное начало проведения ИП, определение оптимальных сроков проведения ИП, адекватное ИП с учетом норм потребления основных пищевых веществ и энергии.
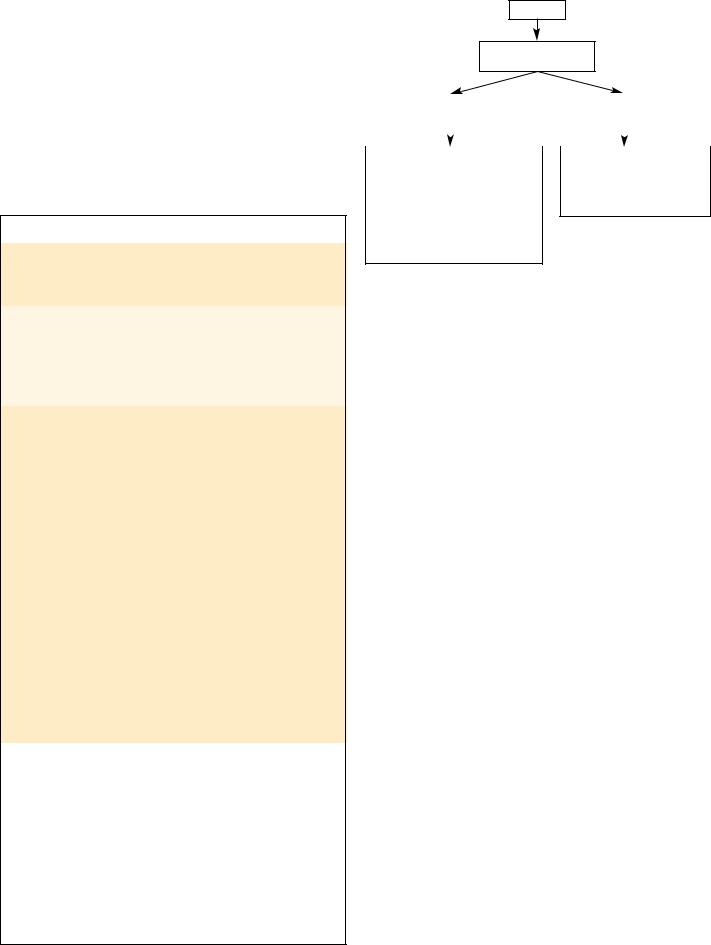
Выбор способа проведения ИП зависит от оценки состояния питания пациента, необходимости выполнения активной нутритивной поддержки и от состояния ЖКТ (рис. 9).
При выборе метода проведения интенсивного лечебного питания больных во всех случаях следует отдавать предпочтение более физиологичному ЭП. Энтеральное питание определяется как искусственно осуществляемое введение питательных субстратов в ЖКТ. По сравнению с ПП оно более физиологично, не требует строгих стерильных условий, практически не вызывает опасных для жизни осложнений, кроме того, в 5–8 раз дешевле ПП.
ЭП имеет физиологические преимущества. При его проведении моторная активность ЖКТ приближается к физиологической. Если скорость введения питания ниже 3 ккал/мин, то скорость опорожнения желудка зависит от калорийности пищевой нагрузки. Корректируя скорость и калорийность вводимого питания, можно добиться относительно устойчивого равновесия между количеством вводимых в желудок питательных веществ, объемом желудочной секреции и скоростью опорожнения желудка. При повышенной калорийной нагрузке и осмолярности питания скорость
опорожнения желудка уменьшается, что может способствовать развитию таких осложнений, как рвота и аспирация. В этой связи наиболее оптимальным является использование растворов с энергетической плотностью 1 ккал/мл. При ЭП сохраняется сократительная активность желчного пузыря, поддерживается энтеральная регуляция ЖКТ с сохранением нормальной секреции холецистокинина и экзокринной функции поджелудочной железы, а также происходит уменьшение числа внутриэпителиальных лимфоцитов, эпителиальной экспрессии антигенов II класса комплекса гистосовместимости, что обусловливает эффективность ЭП при воспалительных заболеваниях кишечника.
Кроме того, этот вид питания способствует благоприятным модифицирующим влияниям на кишечную флору, что положительно сказывается на функционировании толстой кишки и является профилактикой инфекционных осложнений, также отмечается более низкий термический эффект питания (повышение энергозатрат после приема пищи) по сравнению с ПП.
Назначение раннего ЭП в постагрессивном периоде имеет следующие преимущества:
•позволяет эффективно предотвращать дистрофические
иатрофические процессы в слизистой оболочке ЖКТ;
•стимулирует моторно-эвакуаторную активность желудка
икишечника, препятствуя развитию кишечного пареза и функциональной кишечной непроходимости;
•восстанавливает и поддерживает ферментную активность пищеварительных секретов, а также гомеостазирую-
Оценка состояния питания пациента
Нормальное |
|
|
Нормальное питание, |
|
|
|
Пониженное |
||||||||||
питание |
|
|
но высокий риск |
|
|
|
|
|
питание |
||||||||
|
|
|
|
|
|
|
развития его |
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
недостаточности |
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Назначение |
|
|
Показана активная |
|
|
|
|
|
|
|
|||||||
традиционного |
|
|
нутритивная |
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
||||||||
лечебного питания |
|
|
поддержка |
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
Возможно ли |
|
|
|
|
|
|
|
|
||
Да |
|
|
|
|
|
|
|
|
|
|
|
Нет |
|||||
|
|
|
естественное |
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
питание? |
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Лечебный рацион + |
|
|
|
|
|
|
|
|
Функционирование |
||||||||
дополнительное |
|
|
|
|
|
|
|
|
|
|
|
ЖКТ |
|||||
питание |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Нет |
|
|
Частично |
|
|
|
|
|
|
Да |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Полное ПП |
|
|
Зондовая полуэле- |
|
|
|
Зондовая полимерная |
||||||||||
|
|
ментная диета + |
|
|
|
|
|
диета |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
периферическое ПП |
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
> 5 дней |
|
|
|
< 5 дней |
|
|
< 4 нед |
|
|
|
> 4 нед |
||||||
Центральное |
|
|
Периферическое |
|
|
|
|
Наложение |
|||||||||
|
|
|
|
|
ЭП |
|
|
||||||||||
питание |
|
|
|
питание |
|
|
|
|
|
|
стомы |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Рис. 9. Алгоритм выбора тактики нутритивной поддержки.
34

гВ˜В·МУВ ФЛЪ‡МЛВ ‰ВЪВИ ‚ Н ЛЪЛ˜ВТНЛı ТУТЪУflМЛflı: ТУ‚ ВПВММ˚В ФУ‰ıУ‰˚
щую функцию тонкой кишки, предотвращая развитие острой кишечной недостаточности;
•препятствует контаминации микрофлорой проксимальных отделов кишечника (устраняет синдром избыточного роста микроорганизмов);
•снижает возможность транслокации микрофлоры из кишечника в кровь;
•увеличивает мезентериальный и печеночный кровоток;
•препятствует возможности развития патологических энтеральных рефлексов;
•снижает частоту стрессорных эрозивно-язвенных поражений ЖКТ;
•позволяет относительно быстро купировать катаболическую направленность обмена.
Показаниями к проведению ЭП являются:
•состояния, сопровождающиеся гиперметаболизмом: сепсис, травматические повреждения, ожоги, массивные оперативные вмешательства, осложнения послеоперационного периода;
•заболевания ЖКТ (синдром короткой кишки, воспалительные заболевания кишечника, заболевания печени и поджелудочной железы, синдром мальабсорбции, стенозы различных отделов ЖКТ);
•неврологические заболевания: инфекционные заболевания ЦНС, черепно-мозговая травма, заболевания, протекающие с явлениями дисфагии, новообразования;
•онкологические заболевания: в период проведения химиотерапии и радиотерапии;
•психические заболевания: анорексия, тяжелые формы депрессии;
•заболевания, характеризующиеся прогрессирующей органной недостаточностью: дыхательной, сердечной, почечной, печеночной, коматозные состояния;
•тяжелые острые экзогенные отравления и инфекционные заболевания.
Противопоказаниями к проведению ЭП являются:
•полная кишечная непроходимость;
•анурия;
•неукротимая рвота, не корректирующаяся соответствующей терапией;
•высокопродуктивный проксимальный желудочно-кишеч- ный свищ;
•отсутствие функции кишечника вследствие кишечной недостаточности, тяжелого воспаления и т.д.;
•продолжающееся желудочно-кишечное кровотечение, шок.
Диарея и синдром мальабсорбции являются относительными противопоказаниями для проведения ЭП, так как изменение скорости введения питания и коррекция состава лечебных смесей позволяют справиться с этими состояниями.
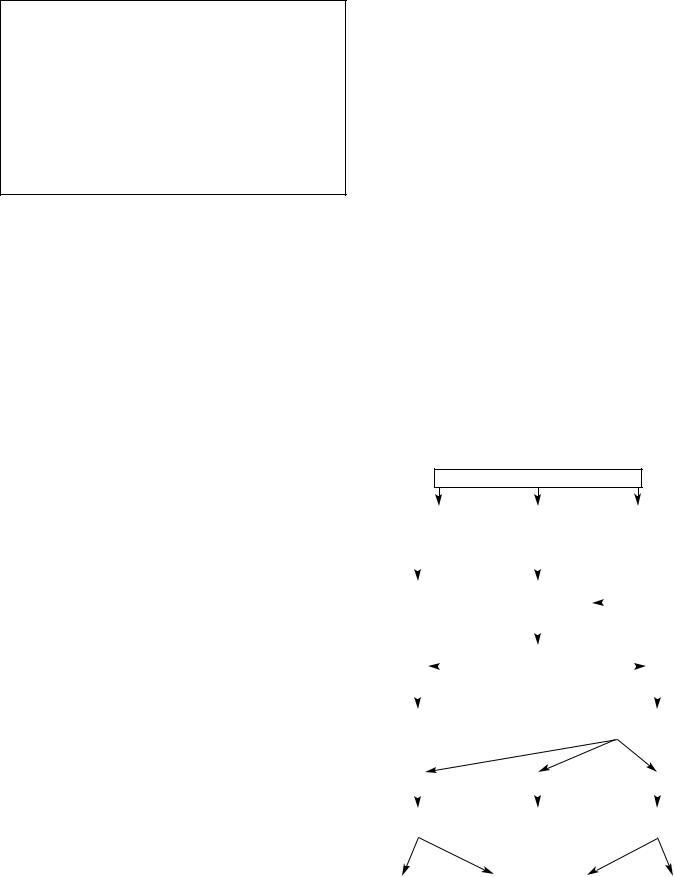
Пути введения ЭП могут различаться в зависимости от основной патологии и предполагаемой длительности кормления, места размещения зонда (рис. 10). Изменение положения зонда (желудок, двенадцатиперстная кишка, тощая кишка) способствует достижению компенсации нарушенных функций пищеварительного тракта.
Несмотря на значительное разнообразие предлагаемых доступов для проведения ЭП их можно условно разделить на две большие группы (табл. 10):
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Нутритивная поддержка |
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
Зондовое питание |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Обычное питание |
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Зонд |
|
|
|
|
Зонд |
|
|
|
|
Зонд |
|
|
|
Дополнительное |
|
|
|
Питание |
||||||||||||||||||||||
|
|
|
|
|
в двенадцати- |
|
|
|
|
|
|
|
|
питание |
|
|
|
смесями |
||||||||||||||||||||||||
|
в тощей |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||
|
|
|
|
|
перстной |
|
|
в желудке |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
кишке |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
кишке |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Хирургическая еюностомия |
|
|
|
Расширенная гастростомия |
|
кишке тощей в Зонд нос через |
|
|
Расширенная гастростомия |
|
|
|
Назодуоденальный зонд |
|
Гастростома |
|
Эзофагостома |
|
|
|
Фарингостома |
|
|
Назогастральный зонд |
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Хирургическая |
|
эндоскопическая |
Чрескожная |
иглы помощью с |
проводимого катетера, |
использованием С |
|
доступом Открытым |
|
|
|||
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
Рис. 10. Пути введения ЭП.
•неоперативные доступы – трансназальные доступы (назогастральный, назодуоденальный, назоеюнальный), относительно малотравматичные, но пригодные только для проведения кратковременного (не более 4-х недель) ЭП;
•оперативные доступы – введение зондов с помощью различных оперативных методик: чрескожной эндоскопии и
сприменением хирургических доступов (эзофагостомия, гастростомия, еюностомия).
У детей наиболее часто используется назогастральный путь проведения ЭП. Размеры зонда (от 4 до 10F) подбираются в зависимости от массы ребенка и его возраста. Рекомендуется выбирать зонд с наименьшим внешним диаметром. Наиболее безопасными материалами для изготовления зондов считаются поливинилхлорид, полиуретан, силикон.
Преимущества назогастрального доступа связаны с его простотой и относительной физиологичностью. При введении зонда через нос в желудок для ориентировочной глубины введения измеряют расстояние от кончика носа до пупка ребенка.
Для дуоденального или еюнального кормления используют утяжеленные зонды. Во избежание их смещения при кормлении необходима фиксация с помощью лейкопластыря к щеке и к поверхности уха. Смена зондов производится каждые 3 дня, если он введен в желудок, и каждые 8 дней, если он введен в дуоденоеюнальную область. Силиконовые зонды могут использоваться без смены до 3 мес. В том случае, если энтеральное кормление планируется более 3 мес – показана гастростомия.
Несмотря на разнообразие лечебных продуктов для ЭП,
при выборе смеси необходимо учитывать особенности ос-
35

е.е.ЙЫ У‚‡, Ц.а.нН‡˜ВМНУ / ЗУФ УТ˚ ‰ВЪТНУИ ‰ЛВЪУОУ„ЛЛ, 2004, Ъ. 2, ‹5, Т. 28–45
Таблица 10. Характеристика различных методов проведения ЭП |
|
|
||
|
|
|
|
|
Метод |
Показания |
Противопоказания |
Осложнения |
Особенности |
Трансназальный доступ |
Кратковременное (менее 4 нед) |
Непроходимость желудка |
Кровотечение |
Физиологическое сходство |
|
проведение ЭП при различных |
или кишечника, |
Установка зонда в просвете |
с нормальным питанием |
|
патологических состояниях, |
Неукротимая рвота |
бронха |
Относительно простая техника |
|
в том числе у пациентов |
|
Прободение ЖКТ |
установления зонда |
|
с патологией ротоглотки |
|
Пролежни в носоглотке, |
|
|
и пищевода |
|
пищеводе |
|
|
|
|
Легочные осложнения |
|
|
|
|
(пневмонии, ателектазы) |
|
Чрескожный |
Необходимость проведения |
Выраженный асцит |
Перитонит |
Метод не всегда возможен |
эндоскопический |
длительного (более 4 нед) ЭП |
Выраженная гепатомегалия |
Кровотечение |
и требует определенных |
доступ |
|
Ожирение высокой степени |
Желудочно-кишечно-кожный |
навыков для выполнения |
|
|
Выраженная портальная |
свищ |
|
|
|
гипертензия |
Перистомальная инфекция |
|
|
|
Фарингеальная |
или фасциит |
|
|
|
или эзофагеальная |
Инфекции |
|
|
|
непроходимость |
Аспирация содержимого |
|
|
|
Различные анатомические |
желудка в бронхи |
|
|
|
дефекты, препятствующие |
Непроходимость зонда |
|
|
|
эндоскопии |
|
|
Хирургический доступ |
При невозможности |
|
Раневая инфекция |
Возможность раннего начала |
|
проведения зонда |
|
Свищ брюшной стенки |
питания после операции |
|
эндоскопическим путем |
|
Непроходимость зонда |
|
|
|
|
Случайное удаление зонда |
|
|
|
|
Заворот кишок |
|
|
|
|
Перитонит |
|
|
|
|
|
|
новного заболевания и возможности ЖКТ в ее усвоении |
ним относятся пациенты, получающие антибиотики, ново- |
|||
(рис. 11). Характеристика смесей для ЭП представлена в |
рожденные дети, больные с пониженной секрецией желудоч- |
|||
табл. 11. В зависимости от способности ЖКТ усваивать нут- |
ного сока, пациенты с ожогами или получающие иммуносу- |
|||
риенты, вводимые энтеральным путем, используются следу- |
прессивную терапию, истощенные дети, больные, находящи- |
|||
ющие способы доставки питания (табл. 12). |
еся на длительном искусственном питании, пациенты с мас- |
|||
При проведении ЭП применение специальных насосов повы- |
сивными травматическими повреждениями. |
|||
шает переносимость и безопасность нутритивной поддержки. |
Причинами, приводящими к осложнению ЭП, относятся: |
|||
Их использование особенно полезно при введении энергетичес- |
• нарушения проведения ЭП (неадекватная компенсация |
|||
ки плотных растворов, в условиях, когда питание должно быть |
дефицита питательных веществ, энергии, жидкости); |
|||
проведено в точно установленное время, при ограничении объ- |
• инвазивность метода, приводящая к снижению защит- |
|||
ема питания для растворов с повышенной осмолярностью. |
ных физиологических механизмов; |
|||
Для предупреждения инфекционных осложнений при про- |
• технические ошибки, возникающие при установлении |
|||
ведении ЭП следует обращать внимание на следующие ме- |
зонда. |
|||
ры предосторожности: |
Наиболее распространенные осложнения представлены в |
|||
• в системе, применяющейся для ЭП, должно быть как мож- |
табл. 13. Среди осложнений чаще встречаются изменения |
|||
но меньше соединений для профилактики инфицирования; |
со стороны ЖКТ. |
|||
• питание должно быть приготовлено только на рекомен- |
В результате нарушения моторики желудка, кишечника |
|||
дованный период; |
может произойти регургитация с последующей аспирацией |
|||
• регулярное промывание зондов. |
и развитием легочных осложнений (аспирационной пневмо- |
|||
Кроме того, необходимо выделять пациентов, относящих- |
нии, ателектазов). Этому состоянию предшествуют появле- |
|||
ся к группе риска по развитию инфекционных осложнений. К |
ние дискомфорта в животе, вздутие живота и тошнота. Ре- |
|||
|
|
|
|
гургитация может возникнуть при отсутствии сознания или |
|
|
|
|
кашлевого рефлекса, при неврологических расстройствах, |
|
Смеси для ЭП |
|
при нарушениях психического статуса, при проведении ис- |
|
|
|
|
|
|
|
|
|
|
кусственной вентиляции легких. |
|
|
|
|
|
|
Содержат цельный |
|
|
|
|
Содержат |
|
Узконаправленные |
|||||||||
|
|
|
белок |
|
модифицированный |
|
смеси |
||||||||||
|
|
|
|
|
|
|
|
|
|
|
белок |
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
содержания Без волокон |
|
содержанием С волокон |
|
|
|
(АК) Элементные |
|
|
Полуэлементные трипептиды) и -(ди |
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Рис. 11. Типы смесей для энтерального зондового питания.
Таблица 11. Особенности состава смесей для ЭП в зависимости
от характера заболевания
Патологическое состояние |
Особенности состава смеси для ЭП |
|
|
Дыхательная |
Изменено соотношение углеводов и жиров |
недостаточность |
в пользу жиров, в результате чего |
|
уменьшается образование углекислого газа |
Почечная недостаточность |
Уменьшено содержание белка, электролитов, |
|
жидкости, увеличена калорийность |
Критические состояния |
Применяется дополнительное обогащение |
|
смеси глутамином, ω -3 жирными кислотами, |
|
аргинином |
Печеночная недостаточность |
Дополнительно вводятся разветвленные АК, |
|
уменьшено содержание ароматических АК |
Сердечная недостаточность |
Уменьшено содержание натрия |
|
|
36
е.е.ЙЫ У‚‡, Ц.а.нН‡˜ВМНУ / ЗУФ УТ˚ ‰ВЪТНУИ ‰ЛВЪУОУ„ЛЛ, 2004, Ъ. 2, ‹5, Т. 28–45
Таблица 12. Способы доставки ЭП |
|
|
|
|
|
Метод |
Характеристика |
Примечания |
Болюсное питание |
Осуществляется 4–6 раз в день, приближено |
Применяется при беспокойстве пациента, если нельзя |
|
к естественному ритму приема пищи. Отмеренный объем |
применить насос, не вводится через тонкую кишку |
|
смеси вводится с помощью шприца со скоростью |
На фоне болюсного кормления наиболее часто возникает |
|
не более 30 мл/мин |
диарея |
Периодическое (сеансовое) питание |
Питание проводится в течение 24-часового периода |
Назначается при отсутствии диареи, синдрома |
|
по 4–6 ч с 2–3-часовыми перерывами |
мальабсорбции, операций на ЖКТ |
Ночное питание |
Осуществляется в течение ночи |
Применяется как дополнение к пероральному приему пищи |
|
|
при ожоговой болезни, синдроме короткой кишки, |
|
|
воспалительных заболеваниях кишечника. Необходимо |
|
|
дополнительное введение жидкости. Может применяться |
|
|
в домашних условиях |
Непрерывное питание |
Питательный раствор поступает в организм постоянно |
Назначается при наличии сомнений в сохранности |
|
в течение суток |
пищеварительной и всасывательной функций ЖКТ |
|
|
|
Таблица 13. Осложнения ЭП |
|
|
|
|
|
Осложнения со стороны |
Механические |
Метаболические |
ЖКТ (30–38%) |
осложнения (2–10%) |
и инфекционные |
|
|
осложнения |
Спастические боли |
Ринит, отит, паротит, |
Нарушение метаболизма |
в животе, вздутие |
фарингит, эзофагит |
кальция, магния, |
живота |
|
фосфора |
Тошнота и рвота |
Легочная аспирация |
Нарушения баланса |
|
|
жидкости |
Эзофагеальный |
Эрозии пищевода |
Гиперосмолярные |
рефлюкс |
|
состояния |
Диарея |
Смещение зонда |
Гипергликемия |
|
|
и гипогликемия |
Нарушение всасывания |
Закупорка зонда |
Микробная контаминация |
Гастродуоденальное |
Прободение |
Микробная колонизация |
кровотечение |
|
и инвазия |
|
|
|
Появление диареи на фоне проведения ЭП чаще всего вызвано неправильным выбором смеси или режима кормления. В этом случае изменение режима введения и уменьшение осмолярности смеси будет достаточным для нормализации стула. В том случае, если после указанных мероприятий диарея сохраняется, необходимо исключить другие факторы: применение антибиотиков, развитие клостридиальной инфекции, развитие другой инфекции микробного или вирусного происхождения, проявления кишечной недостаточности. Тактика ведения больного при появлении у него во время проведения ЭП диареи представлена на рис. 12.
Таким образом, тщательное наблюдение за больным и коррекция выявляемых нежелательных изменений являются самыми эффективными способами профилактики осложнений.
Основными смесями для проведения ЭП как в больницах, так и в домашних условиях являются полимерные питательные смеси.
В полимерных питательных смесях источником азота является цельный белок, углеводный компонент состоит из крахмала или мальтодекстрина, не содержит лактозу, в качестве источника жиров используются растительные масла, смеси обогащены витаминами, минералами и микроэлементами, осмолярность составляет около 300 мосмоль, энергетическая плотность – 1 ккал/мл, концентрация азота – 5–7 г/л, соотношение небелковых калорий и азота колеблется от 150 : 1 до 200 : 1 ккал на 1 г азота.
К сбалансированным полимерным смесям относятся «Берламин®Модуляр» (Германия), «Изокал» (Нидерланды), «Нутрилан» (Германия), «Супро плюс 2640» (США–Бельгия), «Нутризон» (Россия–Нидерланды), «Осмолит» (США), «Нутрен 1,0» (Швейцария) и многие другие.
Особенности состава полимерных сбалансированных смесей представлены на примере продукта «Берламин®Модуляр» (Berlin-Chemi, Германия). Основной модуль «Берламин®Модуляр» может применяться в качестве перорального и зондового ЭП. Препарат характеризуется сбалансированным составом. В 100 г смеси содержится 14,4 г белков, 15 г жиров и 61 г углеводов. Белок представлен как растительным, так и животным компонентом (50% на основе молочного и 50% на основе соевого белка). Такое сочетание белков максимально полно обеспечивает организм всеми незаменимыми АК, поскольку использование только растительного белка не обеспечивает достаточным количеством
Диарея
Посев кала на клостридии
|
Положительный |
|
|
|
|
|
|
|
|
Отрицательный |
|
|||||
|
результат |
|
|
|
|
|
|
|
|
|
результат |
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Лечение клостридиальной |
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|||||||||
инфекции |
|
|
|
|
|
Выявление лекарств, |
||||||||||
|
|
|
|
|
|
|
которые могут вызвать диарею |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Положительный |
|
|
|
Отрицательный |
||||||||
|
|
|
|
результат |
|
|
|
|
|
результат |
||||||
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
Если возможно, проводится |
|
|||||||||||||
|
|
коррекция лечения |
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
Изменение скорости инфузии |
||||||||
|
|
|
|
|
|
|
|
|
и режима питания (переход |
|||||||
|
|
|
|
|
|
|
|
с болюсного или периодического |
||||||||
|
|
|
|
|
|
|
|
|
|
на непрерывное питание) |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Есть эффект |
|
|
|
|
|
|
|
|
Нет эффекта |
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
Продолжение ЭП |
|
|
|
|
|
|
|
|
|||||||
|
на подобранном режиме |
|
|
|
|
|
|
|
|
|||||||
Использование элементных и полуэлементных смесей
|
Есть эффект |
|
Нет эффекта |
|
|
|
|
|
|
Продолжение ЭП |
|
|
|
|
на подобранном режиме |
|
|
|
|
|
|
|
|
|
|
|
|
Переход на ПП |
|
|
|
|
|
|
Рис. 12. Тактика врача при появлении диареи у больного, нахо-
дящегося на ЭП.
38
