
Добавил:
Sekretar
kiopkiopkiop18@yandex.ru
Вовсе не секретарь, но почту проверяю
Опубликованный материал нарушает ваши авторские права? Сообщите нам.
Вуз:
Предмет:
Файл:
Изотонический коэффициент сильного электролита в разбавленном растворе
Равен числу ионов, на которые диссоциирует одна структурная единица
Степень диссоциации кислоты рассчитывается по формулеКакой раствор характеризуется максимальным осмотическим давлением при одинаковой температуре
0,01 М раствор хлорида бария
Гипотонический раствор характеризуется в сравнительном плане
Меньшей осмолярной концентрацией
Плазмолиз это -
Сморщивание клеток
Константа диссоциации зависит
От температуры
С увеличением температуры растворимость газа
Уменьшается
Осмотическое давление 0,02 молярного раствора хлорида кальция при нормальных условиях составляет (ответ дать с точностью до сотых)
"136,12"
Осмотическое давление раствора 0,15М раствора хлорида натрия (физиологического раствора) при 37°С составляет (ответ дать с точностью до сотых)
"772,83"
Рассчитайте осмолярную концентрацию раствора, изотоничного крови, при 37°С. Посм крови - 772,8 кПа. (ответ дать с точностью до сотых)
",3"
Осмотическое давление раствора, содержащего хлорид натрия (0,01 М) и глюкозу (0,01 М) при нормальных условиях составляет (ответ дать с точностью до сотых, разделитель - запятая).
"68,06"
Изменение температуры кипения 0,5 моляльного водного раствора хлорида натрия равно (ответ дать с точностью до сотых). Е воды=0,52 град*кг/моль. Ответ дать с точность до сотых, разделитель - запятая
",52"
Если рН раствора равен 8, то концентрация ионов Н+ равна:
10 -8
рН 0,0001н раствора КОН равен:
10
рН 0,0001 н раствора азотной кислоты равен
4
рН сантинормального раствора гидроксида натрия равен
12
Для вычисления рН раствора слабой кислоты используют формулу
pH=-lg альфа C
Как можно увеличить степень диссоциации уксусной кислоты
разбавлением
рН крови в норме
7,36 – 7,42
Щелочной резерв крови – это
число мл СО2 в 100 мл крови
рН желудочного сока пациента составляет 1,3. Ему следует порекомендовать
щелочную минеральную воду
Как можно изменить константу диссоциации пропановой кислоты
изменением температуры
Вычислить рН в 0,005 М растворе серной кислоты Ответ дать с точность до целых
"2"
Плотность раствора глюкозы 1г/мл. Рассчитать массовую долю (в процентах) сантимолярного раствора глюкозы. (ответ дать с точностью до сотых, разделитель - запятая).
",18"
Молярная концентрация 10% раствора глюкозы равна (плотность =1г/см3) (ответ дать с точностью до сотых, разделитель - запятая).
",56"
рН децимолярного раствора аммиака (рК аммиака=4,75) равен
11,125
Указать потенциальную кислотность раствора уксусной кислоты, если степень диссоциации 0,3, Кд уксусной кислоты=1,78*10 -5
1,4*10 -4
Раствор сильного электролита (рН =12) разбавили в 10 раз. Чему равен рН полученного раствора?
рН=11
pK(H2CO3)= 6.1. При физиологическом значении рН крови =7,4 соотношение [HCO3 -] / [CO2] равно
20/1
В фосфатном буферном растворе при добавлении сильной кислоты изменению рН противодействует
K2HPO4
Буферный раствор можно приготовить
частичной нейтрализацией аммиака
pK(H2PO4 -)=6.8. При физиологическом значении рН крови 7,4 соотношение [HPO42 -]/[H2PO4 -] равно
4/1
Какую кислоту – угольную или лимонную – лучше взять для приготовления буферного раствора, стойко сохраняющего рН=3,15, если Кд угольной кислоты=8*10 -7, Кд лимонной кислоты=8,20*10 -4
лимонную кислоту
При алкалозе рН крови
рН > 7,36
Какую смесь следует выбрать для приготовления буферного раствора с рН=9,2, чтобы раствор имел большую буферную емкость и по щелочи и по кислоте?
боратную Кд Н3ВО3=6,0 *10 -10
Если к ацетатному буферному раствору добавить соляную кислоту, то
концентрация уксусной кислоты увеличится, ацетата натрия уменьшится
В бикарбонатном буферном растворе изменению рН при добавлении сильной кислоты противодействует
соль
Как изменится рН буферного раствора, содержащего в исходном растворе по 0,07 моль экв. соли и кислоты, если в раствор добавить 100 мл воды?
не изменится
Если слабая кислота нейтрализована на 50%, то
рН равен рК
Рассчитать рН аммонийного буфера, полученного сливанием равных объемов 0,1 н раствора аммиака и 0,01 н раствора хлорида аммония. рК аммиака=4,75 (Ответ дать с точностью до сотых).
10,25
В бикарбонатном буферном растворе возрастанию рН противодействует
H2CO3
Если рН буферного раствора > рКд слабой кислоты, то система более устойчива
к добавлению кислоты
Рассчитать рН бикарбонатного буфера, полученного сливанием равных объемов 0,2 н раствора бикарбоната натрия и децинормального раствора угольной кислоты. рК угольной кислоты=6,1 Ответ дать с точностью до десятых, разделитель - запятая
6,4
Рассчитать рН бикарбонатного буфера, полученного смешиванием 200 мл 0,2 н раствора угольной кислоты и 100 мл 0,2 н раствора гидроксида калия. рК угольной кислоты=6,1 (ответ дать с точностью до сотых, разделитель -запятая).
6,1
Фосфатный буфер является основным буфером мочи. В фильтрате 80% фосфатов присутствует в виде аниона НРО42 - , а 20% в виде аниона Н2РО4 -. Кд Н2РО4 - =1,6*10 -7. Рассчитать рН мочи Ответ дать с точностью до десятых, разделитель - запятая
7,4
Если рН буферного раствора больше рК сопряженной кислоты, что нужно добавить в систему, чтобы рН стал равен рК
сопряженную кислоту
В комплексном соединении K4[Fe(CN)6] заряд иона комплексообразователя равен:
+2
В каком из растворов комплексных соединений концентрация лиганда (аниона аминокислоты аспарагина) наибольшая (молярные концентрации растворов равны)?
[Mg(Asn)2] KH=1,0*10 -4
В комплексном соединении [Pt(NH3)2Cl2 ] заряд внутренней сферы равен:
0
В комплексном соединении (NH4)2[PtCl4] лигандами являются ионы:
хлора
В каком растворе потенциал водородного электрода имеет большее значение?
0,1 н HCl
В комплексном соединении К2[PtCl6] комплексообразователем является ион:
платины
Определить направление ОВР: С2Н5ОН + НАД+ ; СН3СОН + НАДН + Н+ (ацетальдегид/этанол)= -0,20 В; (НАД+/НАДН)= -0,320 В
справа налево
С каким из анионов аминокислот: аспарагина, аланина или глицина ион меди образует более прочное комплексное соединение? Константы нестойкости соответственно равны 1,2*10 -15; 4,0*10 -18; 1,4*10 -8:
аланинатом
Какая система является окислителем в реакции фумарат + лактат ; сукцинат + пируват (пируват/лактат)= -0,18 В; (фумарат/сукцинат)= -0,031 В.
фумарат/сукцинат
Хингидронный электрод используют в кислых средах. хг=0,699 В. Выберите верное утверждение:
максимальное значение Eхг=0.699В
Как можно увеличить потенциал водородного электрода?
добавить кислоты
Стеклянный электрод применяется для:
определения рН раствора
Константа нестойкости комплексных соединений не зависит от:
концентрации
Электрохимический ряд металлов (ряд напряжений) – это последовательность металлов, расположенных в зависимости от:
электродных потенциалов
Электрохимическая реакция протекает самопроизвольно, если ЭДС элемента:
больше 0
Рассчитайте ЭДС гальванического элемента по значениям равновесных потенциалов электродов Cu = 0,34 В; Zn = -0,76 B Ответ дать с точностью до десятых, разделитель - запятая
1,1
Как изменится величина равновесного потенциала водородного электрода, помещенного в раствор уксусной кислоты, если нейтрализовать кислоту?
Уменьшится
Платиновый электрод находится в растворе, содержащем пируват и лактат при рН=7. Какая реакция протекает в системе при уменьшении равновесного потенциала?
восстановление
Рассчитать потенциал водородного электрода в 0,1н растворе уксусной кислоты, pK CH3COOH = 4,75. Ответ дать с точностью до сотых, разделитель - запятая
-0,17
Как изменится потенциал платинового электрода, помещенного в раствор солей CrCl2 и CrCl3, при разбавлении раствора водой?
Не изменится
Рассчитать ЭДС элемента, состоящего из насыщенного каломельного электрода и водородного электрода, опущенного в 0,01 н раствор соляной кислоты. Екалом=0,244 В. Ответ дать с точностью до тысячных, разделитель - запятая
,362
Рассчитать потенциал хингидронного электрода в 0,01 н растворе уксусной кислоты наполовину нейтрализованной щелочью. рК кислоты =4,75; хг=0,699 В. Ответ дать с точностью до тысячных, разделитель - запятая
,419
Какая система является акцептором протонов в реакции фумарат +лактат ; сукцинат + пируват (пируват/лактат)= -0,18 В; (фумарат/сукцинат)= -0,031 В.
фумарат/сукцинат
Как изменится потенциал водородного электрода в бикарбонатном буферном растворе при добавлении к этому раствору соли NaHCO3.
Уменьшится
Поглощение вещества всей массой фазы называется:
абсорбцией
Поглощение вещества поверхностью фазы называется
адсорбцией
Адсорбция – экзотермический процесс, поэтому при увеличении температуры величина адсорбции:
уменьшается
Выберите верное утверждение:
атомы и молекулы на границе раздела фаз обладают большей энергией по сравнению с атомами и молекулами в глубине фазы
Величина поверхностной энергии уменьшается при:
уменьшении площади поверхности
Чем лучше адсорбат растворяется в данном растворителе, тем он адсорбируется из этого растворителя:
хуже
Согласно правилу Траубе-Дюкло поверхностная активность с увеличением длины углеводородного радикала на одну CH2 - группу
увеличивается в 3-3.5 раза
К ПАВ относятся вещества, которые
уменьшают поверхностное натяжение на границе раздела фаз
Из предложенных ионов: K+, Ca+2, Al+3 минимальной адсорбционной способностью обладает:
K+
Согласно правилу Дюкло-Траубе большей поверхностной активностью обладает
пентановая кислота
На поверхности твердого хлорида серебра преимущественно адсорбируются ионы
серебра
Положительной адсорбцией обладают вещества
поверхностно активные
Согласно правилу Панета-Фаянса из раствора преимущественно адсорбируются
ионы, входящие в состав кристаллической решетки адсорбента
Холестерин в крови адсорбируется
положительно
Катионит применяют для адсорбции
положительно заряженных ионов
При хемосорбции частицы удерживаются на поверхности адсорбента за счет
химического взаимодействия
Величина поверхностной активности входит в уравнение адсорбции
Гиббса
Величина предельной адсорбции входит в уравнение адсорбции
Ленгмюра
Хроматографические методы основаны на
различной способности веществ к адсорбции
Коллоидная химия – это наука, изучающая:
гетерогенные, высокодисперсные системы
Порог коагуляции - это:
минимальная концентрация электролита, при которой наблюдается явная коагуляция
В соответствии с правилом Шульце-Гарди коагулирующее действие оказывают ионы:
с противоположным зарядом по отношению к заряду коллоидных частиц
Капля крови – это:
золь
Какие ионы оказывают максимальное коагулирующее действие при добавлении к положительно заряженным золям:
PO43-
Золь термодинамически устойчив:
в присутствии стабилизатора
Если заряд коллоидных частиц положителен, то при электрофорезе они перемещаются:
к катоду
Молоко - это
эмульсия
Туман - это
аэрозоль
Аэрозоли – это дисперсные системы с:
твердой дисперсной фазой и газовой дисперсионной средой
Способность к светорассеянию (конус Тиндаля) характерна для
коллоидных растворов
Эмульсии – это дисперсные системы с:
жидкой дисперсной фазой и жидкой дисперсионной средой
Мицелла - это
частица золя
Золи – это дисперсные системы с:
твердой дисперсной фазой и жидкой дисперсионной средой
Для стабилизации эмульсии прямого типа необходим
гидрофильный эмульгатор
Золь можно получить следующими способами
реакцией ионного обмена, в которой образуется осадок
Коллоидные частицы Fe(OH)3 в водном растворе FeCl3:
заряжаются положительно
Коллоидные частицы CuS в водном растворе Na2S:
имеют отрицательный заряд
Коллоидная частица AgI в водном растворе Ag(NO3) при электрофорезе перемещается:
к катоду
Пептизация – это:
переход свежеосажденного осадка в свободнодисперсное состояние
Противоионы находятся
в адсорбционном и диффузном слое
Потенциалопределяющие ионы находятся
в адсорбционном слое
Седиментационная устойчивость это:
способность частиц дисперсной фазы противостоять действию силы тяжести
Заряд коллоидной частицы имеет такой же знак, как и:
заряд потенциалопределяющих ионов
Агрегативная устойчивость это:
способность частиц дисперсной фазы сохранять определенный размер
формулесоответствует название
2-амино-3-гидроксипропановая кислота
К какому классу относится
сложные эфиры
К какому классу относится соединение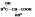
карбоновые кислоты
Название гетероциклического соединения
тиофен
К оксосоединениям не относится
Общая формула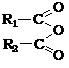
ангидридов карбоновых кислот
Соединениеотносится к классу
альдегидов
Формулесоответствует название
3,5 дигидрокси пентаналь
Название гетероциклического соединения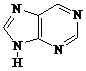
пурин
Название гетероциклического соединения
пиримидин
Наиболее устойчивой конформацией гександиона-2.5 является конформация:
заторможенная
Наиболее устойчивой конформацией ментола (5-метил-2-изопропил-циклогексанола-1) является конформация:
кресло
Наиболее устойчивой конформацией циклогексанкарбоновой кислоты является конформация:
кресло
Химическое строение молекулы определяется
природой и последовательностью связей и атомов в молекуле
Конформация молекулы определяется
поворотом молекулы вокруг сигма-связи
Конфигурация молекулы определяется
типом гибридизации атомов углерода
Молекула какого соединения обладает большей энергией сопряжения:
каротин
Молекула какого соединения обладает большей энергией сопряжения:
циклогексатриен-1,3,5
Молекулы каких соединений обладают большей энергией сопряжения:
ароматические
К гетероциклическим ароматическим соединениям относится
имидазол
К гетероциклическим ароматическим соединениям относится
пурин
Кислотные свойства наиболее выражены у
пропантриола-1,2,3
Формулаотображает строение аминокислоты:
серин
Формулаотображает строение аминокислоты:
аланин
При значении рН раствора равном рI аминокислоты данная аминокислота существует в растворе в виде:
биполярного иона
К кислым аминокислотам относится:
аспарагиновая кислота
К аминокислотам основного типа относится:
лизин
Кислая среда образуется при растворении в воде аминокислоты:
глутаминовая кислота
К нейтральным относится аминокислота:
глутамин
Аминокислоты являются мономерами
белков
Изоэлектрическая точка глутаминовой кислоты
в кислой среде
Щелочная среда образуется при растворении в воде аминокислоты:
аргинин
Изоэлектрическая точка гистидина
в щелочной среде
Изоэлектрическая точка лизина
в щелочной среде
У аминокислот основного типа изоэлектрические точки в области рН
больше 7
У аминокислот кислотного типа изоэлектрические точки в области рН
меньше 7
При рН крови =7,4 аспарагиновая кислота существует в виде
аниона
При рН крови =7,4 лизин существует в виде
катиона
При рН раствора меньших, чем изоэлектрическая точка, аланин существует в виде
катиона
При рН раствора больших, чем изоэлектрическая точка, лизин существует в виде
аниона
При растворении в воде дипептида Лиз-Сер получается среда
щелочная
При растворении в воде дипептида аланил-гистидин получается среда
щелочная
При растворении в воде дипептида Глу-Гли получается среда
кислая
В соответствии с правилом Вант-Гоффа, как и во сколько раз в среднем изменится скорость реакции при повышении температуры на 10° C:
увеличится в 3 раза
Энергия активации разложения лекарственного вещества в присутствии ингибитора:
увеличивается
Константа химического равновесия <b>не</b> зависит от
концентраций реагирующих веществ
При понижении температуры равновесие эндотермической реакции:<br/> PCl5 (г) ; PCl3 (г) + Cl2 (г) - Q
сместится влево
Выражение константы равновесия для обратимой химической реакции:<br/> CuO (т) + H2 (г) ; Cu (т) + Н2О (г) имеет вид
Константа скорости прямой реакции: 2 СO(г)+ О2(г)→ 2 СО2(г)+ Q при уменьшении общего объёма системы в 3 раза
не изменится
Скорость прямой реакции: 2 NO(г)+ Cl2(г)→ 2 NOCl(г) при уменьшении концентрации NO в 5 раз
уменьшится в 25 раз
Фермент - это
катализатор биохимической реакции
В каком из растворов равной молярной концентрации комплексных соединений пиридина с ионами металлов кадмия, меди или цинка концентрация лиганда наибольшая, если константы нестойкости соответственно равны
1,2*10 -2
Какое из комплексных соединений с аминокислотой глицином является наименее устойчивым, если константы нестойкости комплексов соответственно равны:
KH= 1*10 -4
Наиболее сильные кислотные свойства проявляет соединение:
фенол
Наиболее сильные кислотные свойства проявляет соединение:
2,2-дихлорэтанол-1
Наиболее слабые основные свойства проявляет соединение:
аммиак
Наиболее сильные основные свойства проявляет соединение:
метанамин
Выберите НЕ правильное утверждение.
Растворы ВМС при длительном хранении подвергаются тиксотропии
ВМС называются соединения
Молекулярные массы которых превышают десятки и сотни тысяч единиц
Выберите НЕ правильное утверждение.
Для образования растворов ВМС требуется стабилизатор
К биополимерам НЕ относятся
Жиры
Лёгкость растворения ВМС связана с
Наличием лиофильных групп
Термодинамическая устойчивость водных растворов ВМС связана с
Наличием гидратной оболочки у макромолекул
Растворению высокомолекулярных соединений предшествует
Неограниченное набухание
ВМС природного происхождения
Гликоген, гемоглобин, желатин, агар-агар
Свойства коллоидных растворов и растворов ВМС схожи по
Оптическим свойствам
Свойства истинных растворов и растворов ВМС схожи по
Самопроизвольности образования
Процесс набухания высокомолекулярных соединений сопровождается
Диффузией растворителя в полимер
К специфическим свойствам растворов высокомолекулярных соединений НЕ относится:
Самопроизвольность образования
Более сильное высаливающее действие на раствор белка оказывает
Ацетат лития
Более интенсивное желатинирование (гелеобразование) происходит при температуре
10 -С
Более интенсивное желатинирование (гелеобразование) фибриногена крови (pI 5,4)происходит при pH
5,4
Процесс набухания коллагена соединительной ткани (pI 6,0) медленнее будет происходить при pH
6,0
Процесс набухания коллагена соединительной ткани быстрее будет происходить при температуре
70 -С
Более интенсивное высаливание фибриногена крови (pI 5,4)происходит при pH
5,4
Более интенсивное желатинирование (гелеобразование) происходит в присутствии
Сульфата натрия
Процесс набухания миозина скелетных мышц медленнее будет происходить в присутствии
Сульфата натрия
Процесс желатинирования высокомолекулярных соединений сопровождается
Переходом раствора ВМС в студень
К какому электроду при электрофорезе будет передвигаться белок каталаза крови (pI 7) в растворе аммиака, наполовину нейтрализованного соляной кислотой? рКаммиака=4,75 Рассчитать рН раствора
к аноду, рН = 9.25
К какому электроду при электрофорезе будет передвигаться белок химотрипсин сока поджелудочной железы с (pI 8,6) в сантимолярном растворе аммиака. Кдисс(NН3)=1,810 -5. Рассчитать рН раствора
к аноду, рН = 10.6
Белок с pI 3 поместили в 0,01 М раствор соляной кислоты. К какому электроду при электрофорезе будет передвигаться белок ? Рассчитать рН раствора
к катоду, рН = 2
К какому электроду при электрофорезе будет передвигаться белок миозин мышц (pI 5) в 0,005М растворе серной кислоты. Рассчитать рН раствора
к катоду, рН = 2
К какому электроду при электрофорезе будет передвигаться белок с pI9,8 в аммонийном буферном растворе, содержащем 0,06 моль аммиака и 0,03 моль хлорида аммония? Кдисс. (NH3) = 1,810 -5. Рассчитать рН раствора
к катоду, рН = 9.55
Альбумин куриного яйца имеет значение изоэлектрической точки 4,8. К какому электроду при электрофорезе будет передвигаться белок в растворе уксусной кислоты, наполовину нейтрализованной щелочью? рКСН3СООН=4,8. Рассчитать рН раствора
белок неподвижен, рН = 4.8
Рассчитайте соотношение концентраций компонентов в бикарбонатном буферном растворе, в котором глобулин (pI 5,8) находится в изоэлектрическом состоянии. Кдисс. (H2СО3) = 810 -7. Введите ответ с точностью до десятых.
,5
Рассчитайте соотношение концентраций компонентов цитратного буферного раствора, в котором концентрация цвиттер-иона пепсина желудочного сока максимальна. рI пепсина 2,08; рКлимоннойкислоты=3,1 Введите ответ с точностью до десятых.
,1
В каком растворе можно электрофоретически разделить аминокислоты глицин рI 6,1 и глутаминовую кислоту pI
0,01М растворе лимонной кислоты рК=3,1
Рассчитать концентрацию соляной кислоты в растворе, в котором глутамин (pI 3) электрофоретически неподвижен. Введите ответ с точностью до тысячных.
,001
В реакцию со свежеосажденным гидроксидом меди (II) не вступает
этанол
В реакцию с водным раствором щелочи вступает
этантиол
Какое соединение обладает наиболее сильными кислотными свойствами:
орто-гидроксибензойная кислота (салициловая)
В молекуле имидазола сопряженное электронное облако, охватывающее все атомы цикла содержит электронов:
6
Какой тип сопряжения в молекуле пиримидина?
П,П-
У какой молекулы энергия сопряжения больше:
циклогексатриен-1,3,5
Пентандион-1,2 относится к классу:
Кетонов
Гександиаль относится к классу:
альдегидов
К гетероциклическим ароматическим соединениям относится:
пурин
К карбоциклическим ароматическим соединениям относится:
антрацен
С точки зрения теории Брёнстеда, вода - это:
амфолит
Пиррол:
проявляет кислотные свойства
Пиридин:
проявляет основные свойства
Имидазол:
является амфолитом
Соседние файлы в папке Химия
