

ХРОМАТОГРАФИЯ
Хроматогра́фия — физико-химический метод разделения и анализа смесей веществ, основанный на различиях в процессах сорбции и десорбции разделяемых веществ между подвижной и неподвижной фазами, что приводит к различию в скорости движения этих веществ относительно неподвижной фазы.
Тип хроматографии |
Особенности |
|
|
Неподвижная фаза — твёрдый адсорбент; разделение обусловлено различием в молекулярной адсорбции разделяемых |
|
Адсорбционная |
веществ на поверхности зёрен адсорбента. Полярные вещества удерживается сильнее. |
|
|
||
|
|
|
Распределительная |
Разделение веществ осуществляется в результате различия в коэффициентах распределения (взаимодействия) веществ |
|
и обращённо- |
между подвижной и неподвижной фазами. Сильнее удерживаются неполярные вещества. |
|
фазовая |
|
|
|
Неподвижная фаза — пористый сорбент или гель с контролируемым размером пор. Разделение смеси веществ |
|
Эксклюзионная |
осуществляется за счёт различия в размерах молекул веществ и/или их форме и способности проникать в поры |
|
|
неподвижной фазы. |
|
Ионообменная |
Неподвижная фаза — катионит или анионит. Разделение смеси веществ осуществляется за счёт обратимого |
|
взаимодействия ионизирующихся веществ с ионными группами сорбента. |
||
|
||
Афинная |
Разделение смеси биологически активных соединений осуществляется за счёт высокоспецифичных биохимических |
|
взаимодействии с комплементарными сорбционными центрами неподвижной фазы. Данный метод широко |
||
(биоспецифическая) |
||
используется для выделения полипептидов, белков и др. макромолекул биологически активных соединений. |
||
|
Неподвижная и/или подвижная фаза содержат комплексообразователь и разделение смеси веществ осуществляется за |
|
Лигандообменная |
счёт различия в константах комплексообразования веществ и/или коэффициентах распределения комплексов между |
|
|
подвижной и неподвижной фазами. |
61
ЖИДКОСТНАЯ ХРОМАТОГРАФИЯ |
|||
|
|
3 |
|
|
|
6 |
|
|
2 |
5 |
|
|
1 |
||
|
4 |
||
|
|
||
|
|
8 |
|
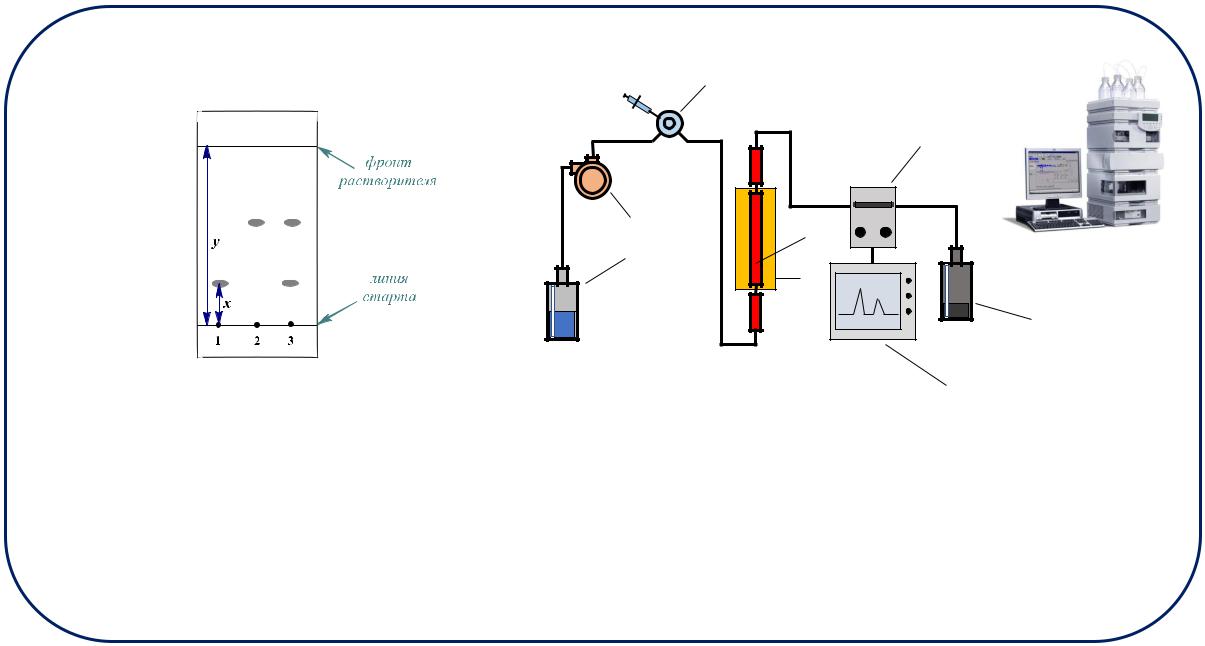
Схема одномерной восходящей хроматограммы |
|
7 |
|
(1 и 2 — стандартные вещества, 3 — |
|
||
Схема жидкостного хроматографа. 1 — резервуар |
|||
анализируемая смесь веществ). |
|||
с растворителем; 2 — насос с датчиком давления; 3 — |
|||
|
|||
|
ручной или автоматический инжектор (автосемплер) — |
||
|
устройство для ввода пробы; 4 — термостат; 5 — |
||
|
хроматографическая колонка; 6 — детектор; 7 — |
||
|
устройство сбора и обработки данных; 8 — резервуар для |
||
|
отработанного растворителя. |
||
62
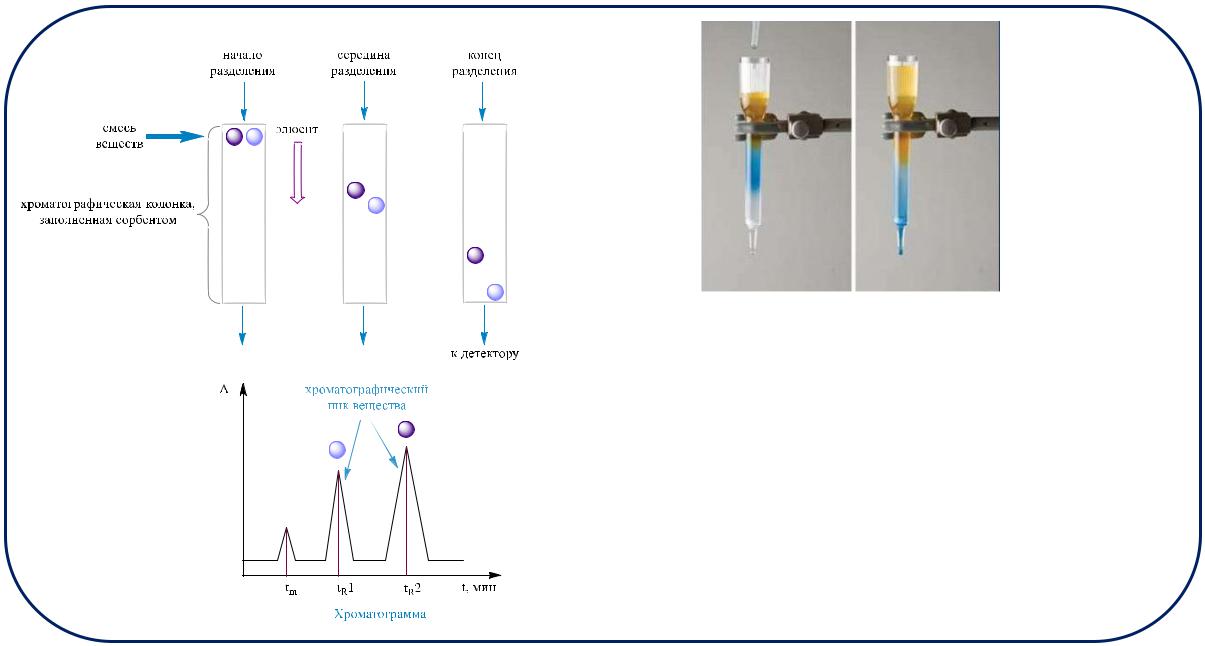
Разделение феррицианида калия и красителя цибакрона голубого на сорбенте сефадексе (сшитый декстран)
Условная схема разделения двух гипотетических веществ, которые перемещаются в слое сорбента с разной скоростью и хроматограмма.
tm — “мёртвое время” — время удерживания несорбирующегося вещества;
tR1 и tR2 — времена удерживания 1-го и 2-го компонента смеси соответственно.
63
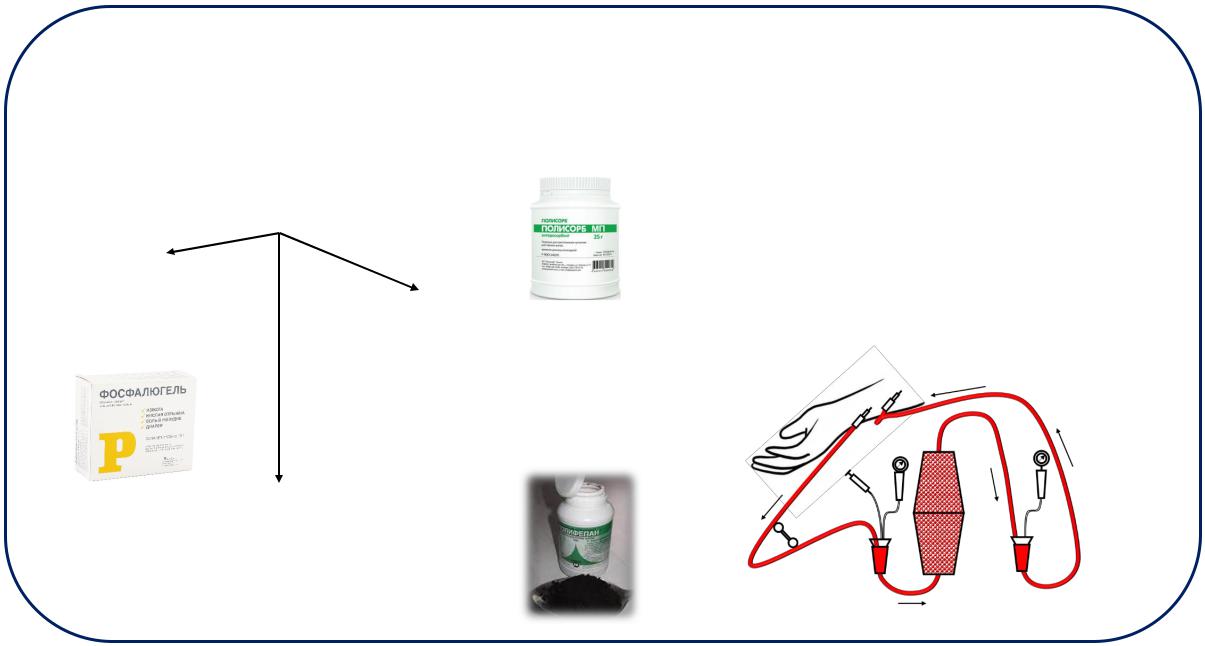
Применение сорбционных процессов в медицине
Энтеросорбция — метод, основанный на адсорбции и выводе из организма в ЖКТ экзогенных веществ, микроорганизмов и токсинов с помощью энетеросорбентов.
«Альмагель», |
|
«фосфалюгель» |
|
(Al(OH)3, MgO, AlPO4). |
Полифункциональный |
|
Энтеросорбент «Полисорб» |
|
(SiO2) |
«Полифепан» — продукт гидролиза лигнина (углеводных компонентов древесины)
Гемосорбция — инвазивный метод детоксикации, заключающийся в очистке крови от токсинов, аллергенов и других вредных веществ путём их адсорбции. В качестве сорбентов используют гемосорбенты
— сорбенты, обладающие свойством поглощадь и прочно удерживать находящиеся в крови токсины
64

Для какой аминокислоты валин или изолейцин больше коэффициент скорости продвижения по хроматографической бумаге?
65
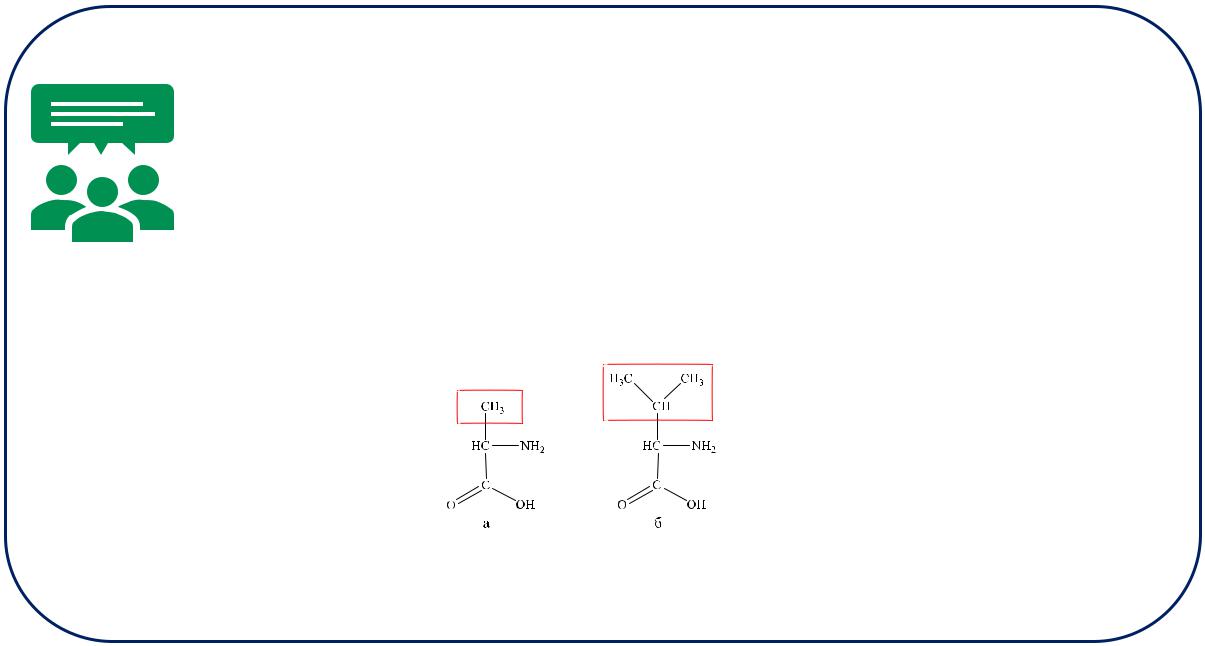
Для валина. Хроматография используется для анализа состава смесей веществ, основанного на различии сродства веществ к неподвижной и движущейся фазам. Хроматографическая бумага — полярная неподвижная фаза, элюентом (подвижной фазой) — является смесь растворителей преимущественно неполярной природы. Молекулы аминокислот являются дифильными. Чем больше неполярный фрагмент молекулы, тем быстрее она будет перемещаться по хроматографической бумаге при элюировании.
66

Фосфатный буферный раствор (рН = 7,6), содержащий альбумин, α -глобулин, β- глобулин, γ-глобулин, пропустили через хроматографическую колонку с анионитом. Используя значения ИЭТ белков, определите, в какой последовательности вымывались белки из колонки.
Белок |
ИЭТ |
альбумин |
4,64 |
α-глобулин |
4,80 |
β-глобулин |
5,20 |
γ-глобулин |
6,40 |
67

Адсорбция белка на ионите определяется значением и знаком заряда его молекулы, дипольным моментом, ориентацией макромолекул на поверхности и другими факторами. При рН > pI белок заряжен отрицательно, при рН=pI суммарный заряд равен 0, а при рН < pI белок заряжен положительно. В рассматриваемом случае все белки имеют отрицательный заряд, но с увеличением разности (рН−pI) возрастает значение отрицательного заряда молекул белков и, соответственно, увеличивается их способность к адсорбции на анионите. При элюировании десорбция белков будет проходить в порядке увеличения адсорбционной способности: γ-глобулин, β-глобулин, α-глобулин, альбумин.
68

В какой последовательности будут выходить белки из хроматографической колонки, если пропустить через колонку с анионитом аммонийный буферный раствор (рН=9,25), содержащий смесь глобулинов крови: α-глобулин (рI 4,8), β-глобулин (рI 5,2), γ-глобулин (рI 6,4).
69

Решение.
рН(9,25) > pI → заряд отрицательный у всех трех белков, → все адсорбируются на анионите.
Чем больше разница рН и pI, тем больше величина отрицательного заряда, тем
больше адсорбция
Последовательность выхода из колонки:
γ-глобулин (рI 6,4), β-глобулин (рI 5,2), α-глобулин (рI 4,8)
70
