
2 курс / Микробиология 1 кафедра / Доп. материалы / Mikra_Teoria_dlya_2_kolka
.pdf
3) По механизму действия:
- Антибиотики, нарушающие синтез клеточной стенки. Эти препараты блокируют пенициллин связывающий белок, который обеспечивает встраивание предшественника пептидогликана
в клеточную стенку. Происходит
истощение клеточной стенки и накопление предшественника пептидогликана в бактерии, что ведет к аутолизу. При неправильной дозировке возможно образование L-форм.
- Антибиотики, нарушающие
синтез белка.
Наиболее многочисленная группа
препаратов.
- Антибиотики — ингибиторы синтеза нуклеиновых кислот.
Основные мишени: ингибирование синтза предшественников
нуклеиновых кислот,
ингибирование репликации ДНК, ингибирование РНК-полимеразы.
Все препараты этой группы,
представленные на рисунке (кроме
рифампицина) являются синтетическими.
- Антибиотики, нарушающие
молекулярную организацию и синтез клеточных мембран.
Большинство противогрибковых препаратов относятся к этой
группе, так как одним из немногочисленных отличий клеток грибов от клеток человека являются эргостеролы (компонент ЦПМ грибов).
Лекарственная устойчивость.
Антибиотикорезистентность — это устойчивость микробов к антимикробным
химиопрепаратам.
Бактерии следует считать резистентными, если в организме невозможно создать ту концентрацию препарата, которая их убьет.
Резистентность может быть природной и приобретенной:
Природная устойчивость.
-в результате отсутствия соответствующей мишени (например, микоплазмы не имеют клеточной стенки, поэтому не чувствительны ко всем препаратам, действующим на этом
уровне);
-в результате бактериальной непроницаемости для данного препарата (например, грамотрицательные микробы менее проницаемы для крупномолекулярных соединений, чем грамположительные бактерии, так как их наружная мембрана имеет «маленькие» поры).
Приобретенная устойчивость.
Генетические основы приобретенной резистентности поддерживаются генами резистентности (r-генами)). Приобретенная лекарственная устойчивость может возникать и распространяться в
популяции бактерий в результате:
-мутаций в хромосоме бакерии с последующей селекцией (например, произошла мутация, обеспечившая бактерии устойчивость к антибиотикам; остальные бактерии погибли, а эта выжила и дала потомство резистентных бактерий).
-переноса трансмиссивных плазмид резистентности (R-плазмид) в результате конъюгации;
-переноса транспозонов, несущих r-гены (транспозоны могут мигрировать с хромосомы на плазмиду и обратно, а также с плазмиды на другую плазмиду, таким образом передавая r- гены дочерним клеткам или при рекомбинации другим бактериям);
Реализация приобретенной устойчивости:
-модификация мишени антибиотика (фермент-мишень может быть так изменен, что его функции не нарушаются, но способность связываться с химиопрепаратом резко снижается или
может быть включен «обходной путь» метаболизма, т. е. в клетке активируется другой
фермент, который не подвержен действию данного препарата);
-«недоступность» мишени за счет снижения проницаемости клеточной стенки и клеточных мембран или «эффлюко-механизма», когда клетка как бы «выталкивает» из себя антибиотик;
-инактивация препарата бактериальными ферментами (например, бета-лактамазы,
разрушающие бета-лактамное кольцо антибиотика с образованием неактивных соединений;
Преодоление антибиотикорезестентности:
-применять антибиотики строго по показаниям, избегать их использования с профилактической целью;
-через 10—15 дней антибиотикотерапии менять препарат;
-по возможности использовать препараты узкого спектра действия;
-ограниченно применять антибиотики в ветеринарии и не использовать их как фактор роста.
Предупредить развитие антибиотикорезистентности у бактерий практически невозможно.

Определение чувствительности к антибиотикам:
1) Метод диффузии в агар.
На питательную среду (на основе агара) засевают исследуемый микроб, а затем вносят антибиотики. Обычно препараты вносят или в специальные лунки в агаре, или на поверхности посева раскладывают диски с антибиотиками («метод дисков»). Учет результатов проводят через сутки по наличию или отсутствию роста микробов вокруг лунок (дисков). Метод дисков
— качественный и позволяет оценить, чувствителен или устойчив микроб к препарату.
2) Затем проводят метод серийных разведений:
Определение чувствительности бактерий к антибиотикам методом серийных разведений.
Данным методом определяют минимальную концентрацию антибиотика, ингибирующую рост исследуемой культуры бактерий. Это количественные метод, которые позволяет рассчитать
дозу препарата. Вначале готовят основной раствор, содержащий определенную концентрацию
антибиотика в специальном растворителе. Из него готовят все последующие разведения в бульоне (в объеме 1 мл), после чего к каждому разведению добавляют по 1 петле
бактериальной суспензии. В последнюю пробирку вносят 1 мл бульона и 0,1 мл суспензии
бактерий (контроль культуры). Посевы инкубируют при 37 °С до следующего дня, после чего отмечают результаты опыта по помутнению питательной среды, сравнивая с контролем
культуры. Последняя пробирка с прозрачной питательной средой указывает на задержку
роста исследуемой культуры бактерий под влиянием содержащейся в ней минимальной ингибирующей концентрации (МИК) антибиотика.
Принципы рациональной антибиотикотерапии.
Микробиологический принцип.
-определение возбудителя;
-назначение препаратов широкого спектра действия;
-по результатам исследования назначают препарат узкого спектра действия.
Фармакологический принцип.
-фармакокинетика и фармакодинамика препарата;
-дозы препаратов (в 2-3 раза больше МИК)
-оптимальные пути введения препарата.
Клинический принцип.
-учитывают состояние больного (тяжесть инфекции, иммунный статус, пол, наличие
беременности, возраст и т.п.)
-при назначении комбинации из нескольких препаратов следует знать, насколько эффективным и безопасным для пациента будет сочетание данных препаратов (возможно суммирование их токсических эффектов).
Эпидемиологический принцип.
-разные штаммы (один вид, выделенный из одного источника) могут иметь разную резистентность.
-резистентность может приобретаться и теряться.
Фармацевтический принцип.
- срок годности, условия хранения и стоимость препарата.
Осложнения антибиотикотерапии:
1) Осложнения со стороны макроорганизма:
Токсическое действие препаратов.
-общетокическое (полиены, имидазолы);
-нейротоксическое (например, гликопептиды и аминогликозиды оказывают ототоксическое действие, вплоть до полной потери слуха за счет воздействия на слуховой нерв);
-нефротоксическое (полиены, полипептиды, сульфаниламиды);
-угнетение кроветворения (тетрациклины, сульфаниламиды, левомицетин); -гепатогенное (тетрациклин);
-тератогенное, т.е. на эмбрион (аминогликозиды, тетрациклины нарушают развитие костей, хрящей у плода и детей);
-для новорожденных (левомицетин/хлорамфеникол).
Предупреждение осложнений состоит в отказе от противопоказанных данному пациенту препаратов, контроле за состоянием функций печени, почек и т. п.
Дисбиоз (дисбактериоз).
Предупреждение осложнений состоит в назначении, по возможности, препаратов узкого спектра действия, сочетании лечения основного заболевания с противогрибковой терапией (например, назначением нистатина), витаминотерапей, применением эубиотиков и т. п.
Воздействие на иммунную систему.
-аллергические реакции (проявляются в виде сыпи, зуда, крапивницы, отека Квинке, редко
анафилактический шок);
-гиперчувствительность замедленного типа (сульфаниламиды).
-иммунодепрессивным действием и развитие вторичного иммунодефицита.
Предупреждение осложнений состоит в тщательном сборе аллергоанамнеза и назначении препаратов в соответствии с индивидуальной чувствительностью пациента.
Эндотоксический шок (терапевтический).
Возникает при лечении инфекций, вызванных грамотрицательными бактериями. Введение антибиотиков вызывает разрушение клеток и высвобождение больших количеств эндотоксина, обладающего пирогенным действием (повышает температуру).
Взаимодействие с другими препаратами.
- потенцирование действия или инактивации других препаратов (например, эритромицин стимулирует выработку ферментов печени, которые начинают ускоренно метаболизировать
лекарственные средства разного назначения).
2) Побочное воздействие на микроорганизмы.
-образование L-форм и персистирующих форм микробов;
-формирование антибиотикозависимости (редко) и антибиотикорезистентности (достаточно
часто).

ЭКОЛОГИЯ МИКРОБОВ
! Выучить только по несколько представителей на каждый биотоп !
Функциями нормальной микрофлоры кишечника являются:
1.Колонизационная резистентность - конкуренция с патогенными микробами, стимуляция местного иммунитета;
2.Синтетическая функция - способность бактерий продуцировать витамины, гормоны,
антибиотики; 3.Детоксикация различных метаболитов;
4.Обменная функция - участие бактерий в метаболизме белков, углеводов, липидов, нуклеиновых кислот, солей, желчных кислот и других жизненно важных веществ; 5.Пищеварительная – усиление физиологической активности ЖКТ.
Микробиота – это эволюционно сложившееся сообщество разнообразных микроорганизмов,
населяющих открытые полости организма человека, определяющее биохимическое,
метаболическое и иммунологическое равновесие макроорганизма.
Эубиоз - совокупность микробных популяций, населяющих естественные биотопы здорового
человека.
Под биотопом принято понимать участок слизистой оболочки, кожи или орган
макроорганизма с однотипными условиями существования микробных сообществ.
Дисбиоз (дисбактериоз – только бактерии) качественное и количественное изменение состава нормальной микрофлоры макроорганизма.
Стерильные в норме ткани и органы здорового человека:
-внутренние органы;
-головной и спинной мозг;
-альвеолы легких;
-внутреннее и среднее ухо;
-кровь, лимфа, спинномозговая жидкость;
-матка, почки, мочеточники и моча в мочевом пузыре.
Микрофлореа полости рта:
-бактероиды;
-вибрионы;
-фузобактерии;
-спирохеты.
Микрофлора желудка:
-лактобактерии;
-бифидобактерии;
-бактероиды;
-стрептококки
-дрожжеподобные грибы;
-Helicobacter pylori.
Микрофлора двенадцатиперстной и тонкой кишки:
-молочнокислые бактерии (лактобактерии);
-бифидобактерии;
-бактероиды;
-энтерококки;
Микрофлора толстой кишки:
1)Анаэробы (до 96-98 %):
-бактероиды (особенно Bacteroides fragilis);
-анаэробные молочнокислые бактерии (например, Bifidobacterium);
-клостридии (Clostridium);
-анаэробные стрептококки;
-фузобактерии;
-эубактерии;
-вейлонеллы.
2) Аэробы и факультативные анаэробы (до 14%):
-грамотрицательные колиформные бактерии (прежде всего кишечная палочка);
-энтерококки;
-в небольшом количестве: стафилококки, протеи, псевдомонады, лактобациллы, грибы рода
Candida.
Наружная часть уретры человека:
-коринебактерии;
-микобактерии;
-грамотрицательными бактерии фекального происхождения;
-неспорообразующие анаэробы (пептококки, пептострептококки, бактероиды).
Состав нормальной влагалищной микрофлоры половозрелой женщины:
-лактобактерии;
-клостридии;
-анаэробные стрептококки (пептострептококки);
-стафилококки;
-аэробные гемолитические стрептококки группы В;
-колиформные бактерии;
-дифтероиды;
Нормальная микрофлора кожи:
1) Резидентная микрофлора кожи (постоянная):
-Staphylococcus epidermidis;
-Staphylococcus aureus;
-Micrococcus spp.;
-Sarcina spp.;
-коринеформные бактерии;
-Propionibacterium spp.
2) Транзиторная микрофлора кожи (непостоянная):
-Streptococcus spp.;
-Peptococcus spp.;
-Bacillus subtilis;
-Escherichia coli;
-Enterobacter spp.;
-Acinetobacter spp.;
-Lactobacillis spp.;
-Candida albicans и многие другие.
Нормальная микрофлора верхних дыхательных путей:
1)Резидентная микрофлора носа : - коринебактерии (дифтероиды); - нейссерии;
- коагулазо-отрицательне стафилококки; - альфа-гемолитическими стрептококки.
2)Транзиторная микрофлора:
-Staphylococcus aureus;
-Escherihia coli;
-бета-гемолитические стрептококки.
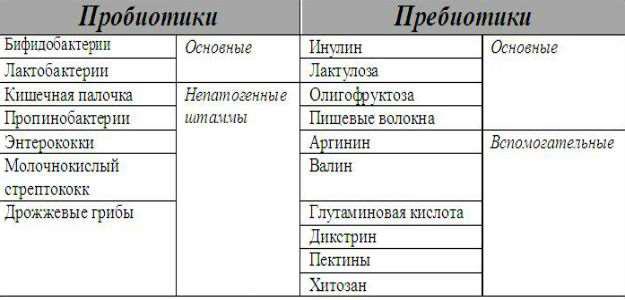
Препараты для нормолизации микрофлоры:
Пробиотики (эубиотики)– это непатогенные для человека микроорганизмы, которые способны
восстанавливать нормальную микрофлору органов, а также губительно воздействовать на патогенные и условно-патогенные бактерии.
Пребиотиками называются вещества, которые не всасываются в тонкой кишке, но создают
благоприятные условия и стимулируют рост нормальной микрофлоры толстого кишечника.
Синбиотики – это лекарственные препараты, которые содержат комбинацию из пробиотиков и пребиотиков.
Симбиотики – это лекарственные препараты, в состав которых входит несколько видов микроорганизмов-пробиотиков или несколько штаммов одного и того же типа бактерии.
Селективная деконтаминация - это избирательное удаление из пищеварительного тракта аэробных бактерий и грибов для повышения сопротивляемости организма к инфекционным агентам.
Селективную деконтаминацию проводят путем назначения для приема внутрь малоадсорбируемых химиопрепаратов, подавляющих аэробную часть микрофлоры и не
влияющих на анаэробы, например комплексное назначение ванкомицина, гентамицина и
нистатина.
Представители нормальной микрофлоры при снижении сопротивляемости организма вызывают гнойно-воспалительные процессы, т.е. нормальная микрофлора может стать
источником аутоинфекции, или эндогенной инфекции. Когда микробы - комменсалы
оказываются при транслокации в непривычных местах обитания, они могут вызывать различные нарушения.
Исследование воды:
Загрязненность воды определяется по общей микробной обсемененности и обнаружению санитарно-показательных микроорганизмов — индикаторов наличия выделений человека или животных.
В соответствии с нормативами:
1.Общее микробное число воды не должно превышать 100 микробов в 1 мл исследуемой воды;
2.Общие колиформные бактерии должны отсутствовать в 100 мл исследуемой воды;
3.Термотолерантные колиформные бактерии должны отсутстовать в 100 мл исследуемой
воды;
4.Споры сульфитредуцирующих клостридий не должны определяться в 20 мл исследуемой
воды;
5.Колифаги не должны определяться в 100 мл исследуемой воды; 6. Цисты лямблий не
должны определяться в 50 мл исследуемой воды.
Кроме того, загрязненность воды оценивается по обнаружению патогенных микробов с фекально-оральным механизмом передачи (энтеровирусы, энтеробактерии, холерные
вибрионы и др.).
Определение общего микробного числа:
Общее микробное число (ОМЧ) воды - общее число мезофильных аэробных и факультативно анаэробных микроорганизмов в 1 мл воды, способных образовывать колонии на питательном .
1)При исследовании водопроводной воды засевают 2 чашки.
2)Культивируют и подсчитывают число выросших колоний:1 бактерия размножается и обрузует 1 колонию;таким образом можно составить пропорцию и узнать, сколько бактерий
было в 1 мл исследуемой воды.

Определение общих и термотолерантных колиформных бактерий:
Общие колиформные бактерии (ОКБ) - грамотрицательные, оксидазоотрицательные, не образующие спор палочки, ферментирующие лактозу.
Термотолерантные колиформные бактерии (ТКБ) входят в число общих колиформных
бактерий, обладают всеми их признаками и, но способны ферментировать лактозу при
температуре (44 ± 0,5) °С .
Количество этих бактерий выражают двумя показателями:
Коли-индекс - количество кишечных палочек, обнаруженных в 1 л воды.
Коли-титр - наименьшее количество воды, в котором обнаруживают присутствие кишечной палочки (коли-титр и коли-индекс - это один показатель, различно выраженный).
Для выявления в воде БГКП можно пользоваться двумя методами: титрационным и методом
мембранных фильтров.
Титрационный метод: для исследования воды используют среду накопления глюкозопептонную (ГПС).
- Исследуемую воду засевают с разным разведением.
- Затем культивируют и при наличии
помутнения в колбах или пробирках из них
производят посев петлей на сектора среды Эндо в чашках Петри.
- Культивируют и из подозрительных колоний
делают мазки.
- При наличии грамотрицательных палочек ставят пробу на оксидазную активность.
Положительная проба на оксидазу дает право
дать отрицательный ответ. Отрицательная проба на оксидазу свидетельствует о наличии в воде БГКП. В этом случае вычисляют коли-
индекс и коли-титр с помощью стандартных
таблиц.
