

Первый Санкт-Петербургский государственный медицинский университет им. акад. И. П. Павлова
Кафедра общей и биоорганической химии
Аминокислоты,пептиды,белкивводныхрастворах. Аминокислотныеибелковыебуферныесистемы.
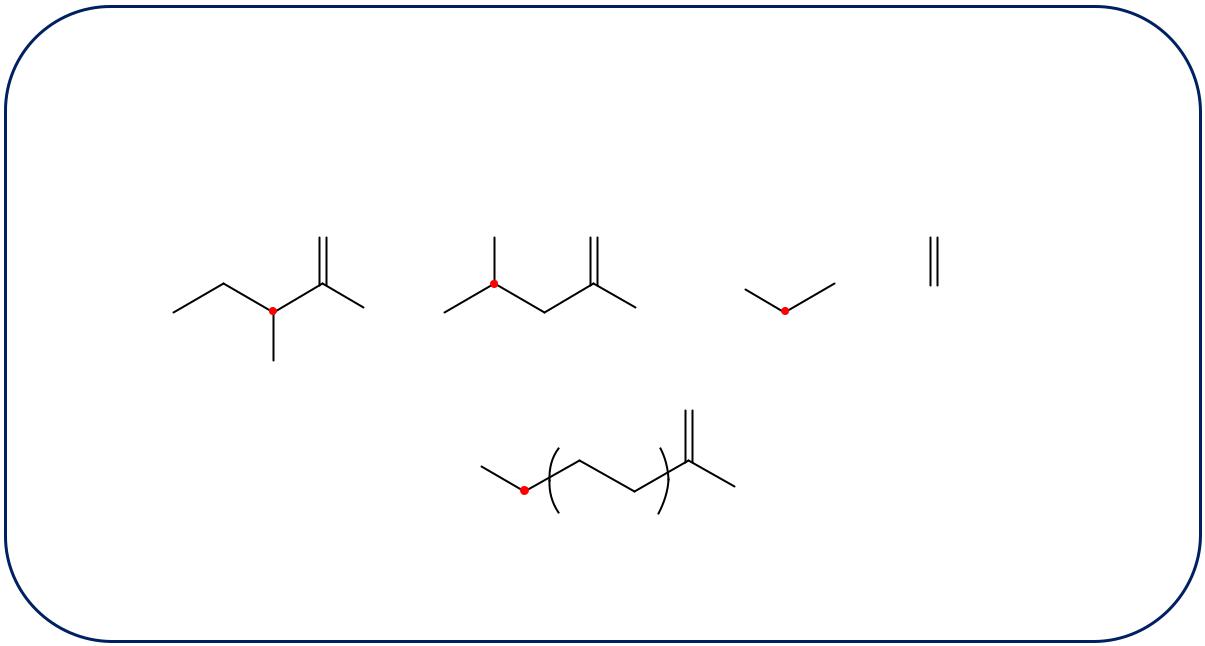
Классификации аминокислот
1. В зависимости от взаимного расположения амино- и карбоксильной групп: α-, β-, γ-, δ-, ε-, и ω- аминокислоты.
O |
NH2 |
O |
α |
|
|
H2N |
|
OH |
β |
OH |
||
γ |
||||
|
|
|
NH2
|
O |
|
H2N |
|
OH |
ω |
n |
O
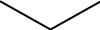
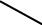 OH
OH
2
α-Аминокислоты
структурные |
α-аминокислоты |
источник |
|
||
компонентыбелков |
биорегуляторы |
энергии |
α-Аминокислоты — органические гетерофункциональные соединения, молекулы которых содержатодновременноаминогруппуи карбоксильнуюгруппупри одноматомауглерода.
общая |
|
|
|
атом α углерода |
|
H2N |
|
CH |
|
COOH |
|
формула |
|
|
|||
|
|
||||
|
|
|
R |
|
боковой радикал |
Общий фрагмент всех α-аминокислот (для глицина R = H)
Природных — более300.
Протеиногенных — 21 α-аминокислота (включая одну иминокислоту — пролин).
3
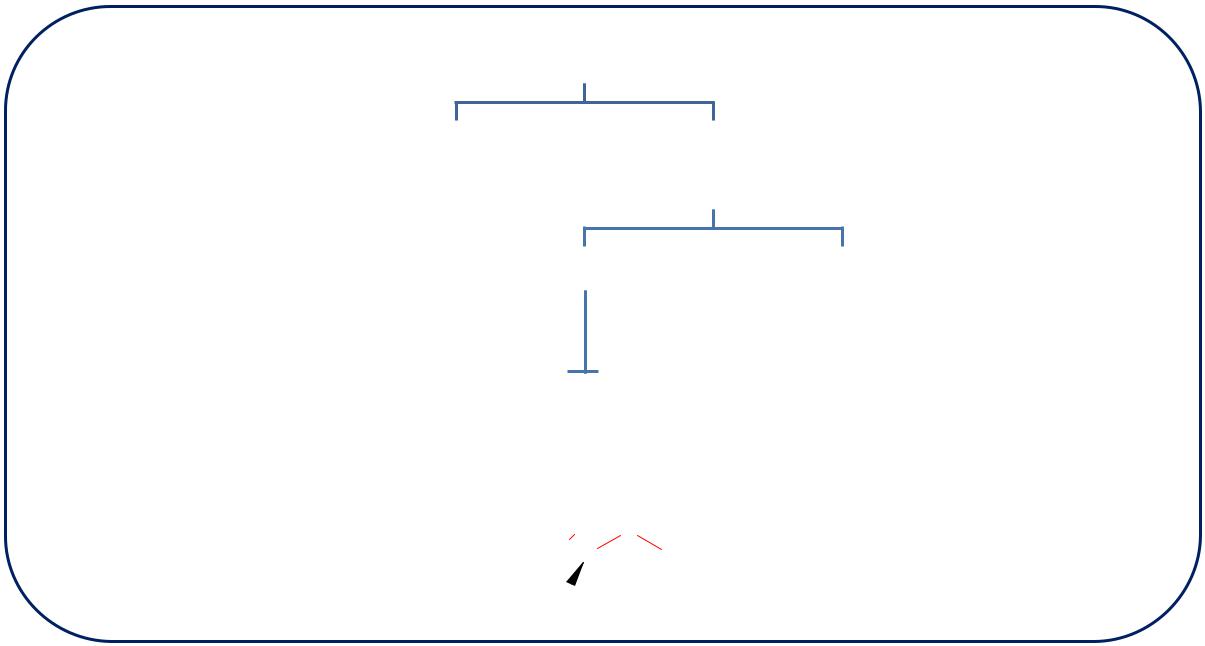
2. По природе бокового радикала
Аминокислоты
Неполярные Полярные (гидрофобные) (гидрофильные)
Ионогенные Неионогенные
ПоложительноОтрицательнозаряженные заряженные
В данной классификации глицин — исключение, так как он не имеет бокового радикала. Молекула сильно полярна и оптически неактивна.
O
H С
С

H2N 
 С OH
С OH
H Глицин, Гли
Gly
4
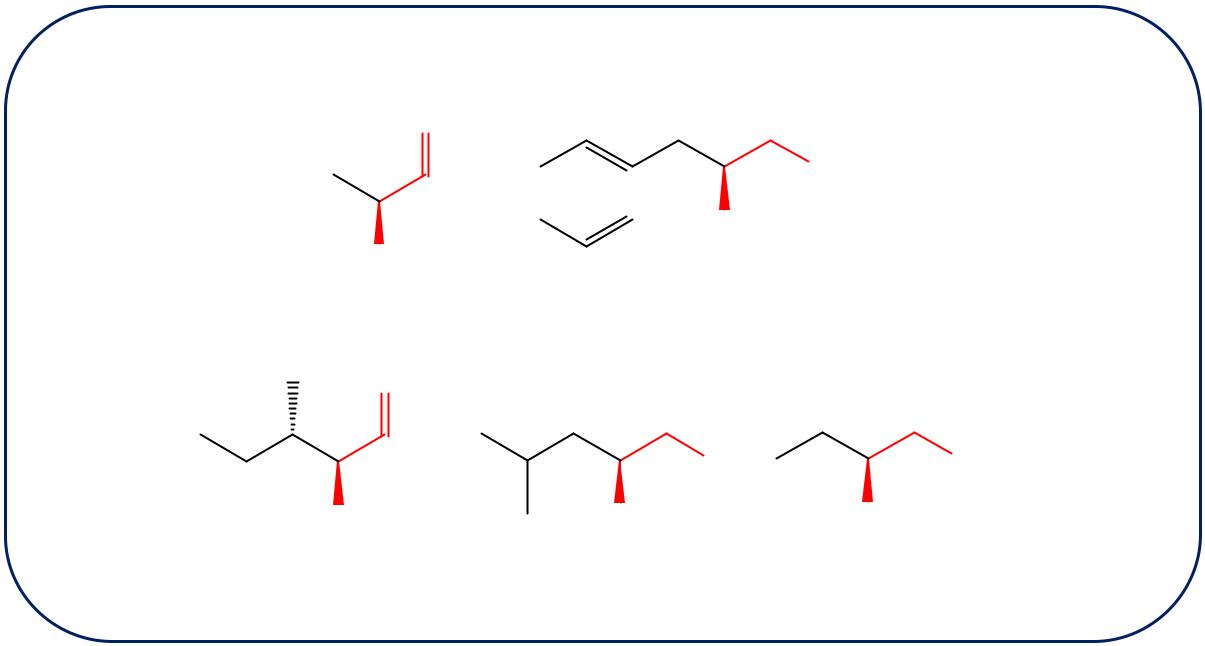
2.1 Аминокислоты с неполярными (гидрофобными) радикалами
O
 OH
OH
NH2
Аланин, Ала
Ala
O
 OH
OH
NH2
Изолейцин, Иле
Ile
|
|
|
|
|
O |
|
|
|
|
|
||
|
|
|
|
|
|
|
|
OH |
||||
|
|
|
|
|
NH2 |
|||||||
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|||
|
Фенилаланин, Фен |
|
|
|
|
|
||||||
|
|
|
Phe |
|
|
|
|
|
||||
|
|
O |
|
|
O |
|||||||
|
|
|
|
|||||||||
|
|
|
|
OH |
|
|
|
|
OH |
|||
|
|
|
|
|
|
|
|
|||||
|
NH2 |
|
NH2 |
|||||||||
Лейцин, Лей |
Валин, Вал |
|||||||||||
|
Leu |
|
Val |
|||||||||
5
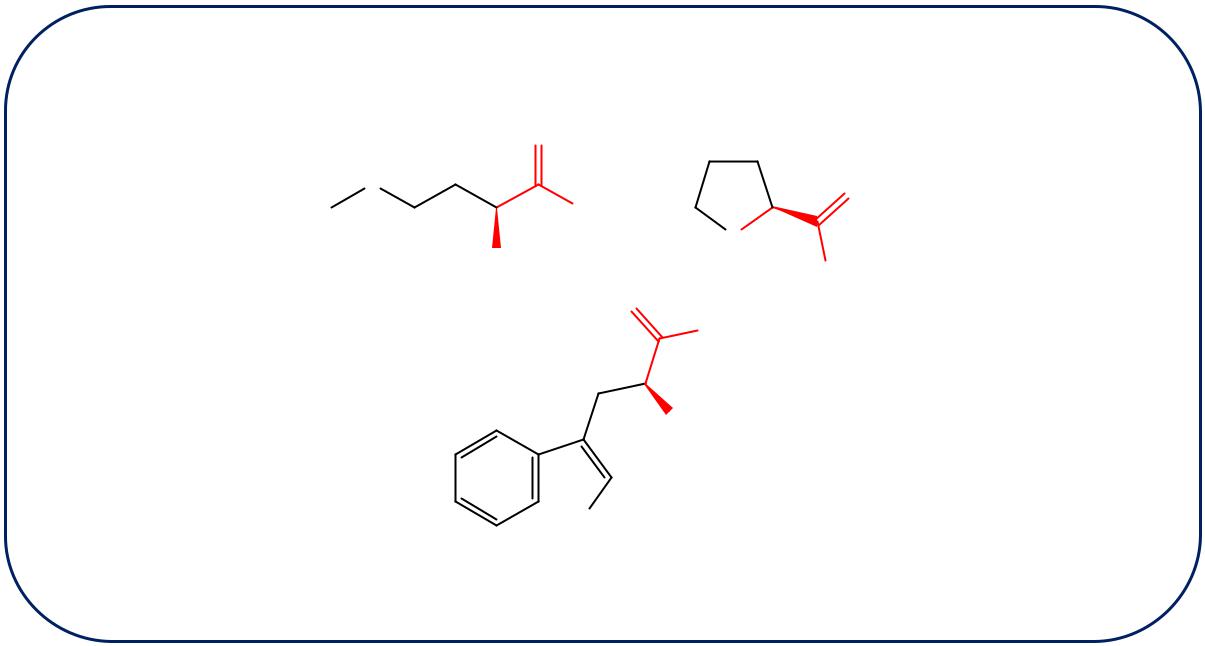
2.1 Аминокислоты с неполярными (гидрофобными) радикалами
|
|
O |
S |
|
O |
|
|
|
|
|
OH |
|
|
N |
|
NH2 |
H |
|
OH |
|
|
|
Метионин, Мет
Met
O |
|
Пролин, Про |
|
OH |
Pro |
|
|
NH2
 N
N
H
Триптофан, Три
Trp
6
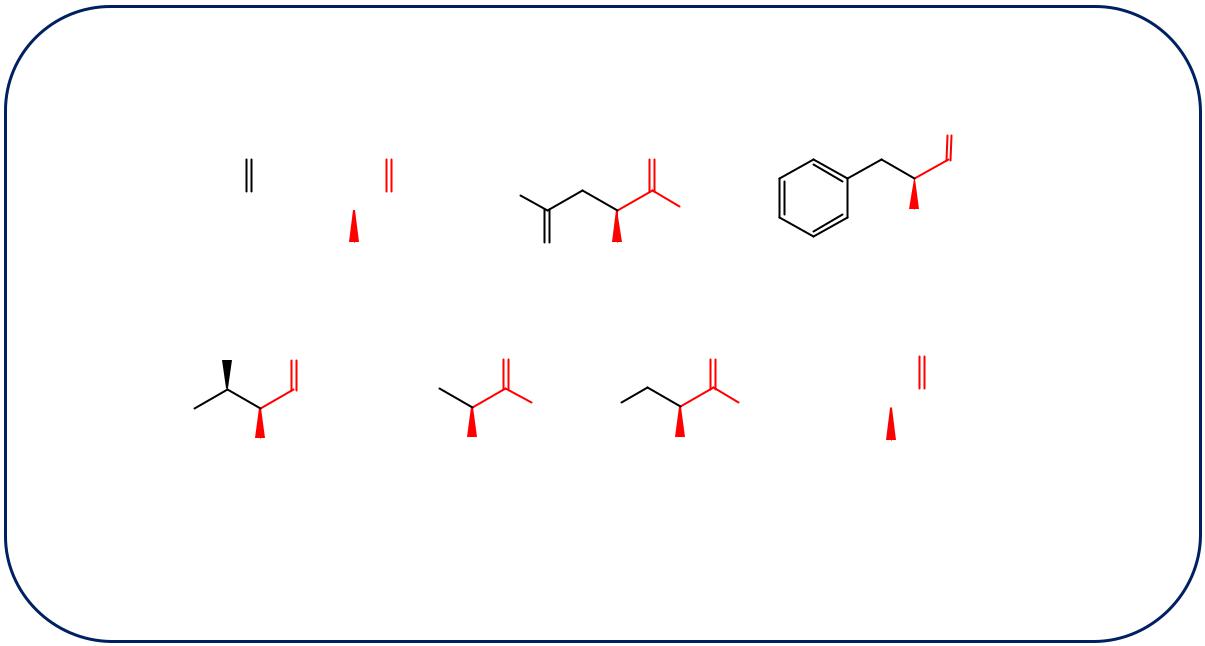
2.2 Аминокислоты с полярными неионогенными радикалами
O O
H2N 

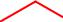 OH
OH
NH2
Глутамин, Глн
Gln
OH O
 OH HO
OH HO
NH2
O
H2N
OH
HO
O NH2
Аспарагин, Асн
Asn
O |
|
O |
OH |
HS |
OH |
NH2 |
|
NH2 |
Треонин, Тре |
Серин, Сер |
Цистеин, Цис |
|
Ser |
Cys |
||
Thr |
O
 OH
OH
NH2
Тирозин, Тир
Tyr
O
HSe
 OH
OH
NH2
Селеноцистеин, Se-Цис
Sec
7
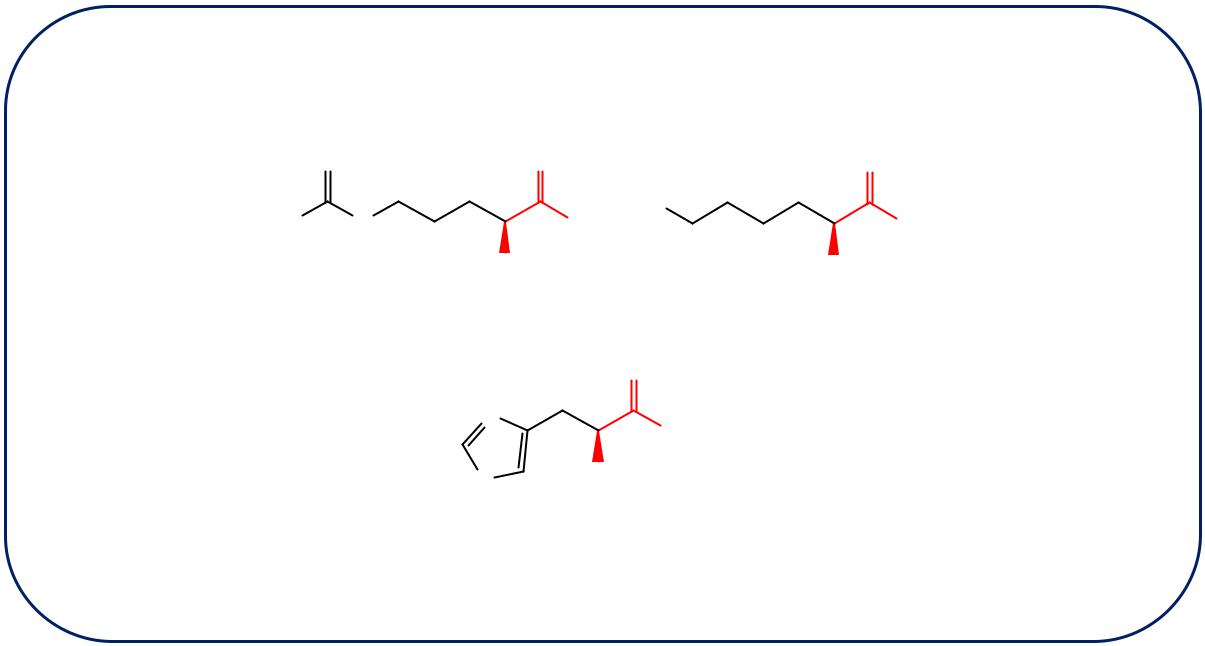
2.3. Аминокислоты с полярными ионогенными радикалами
2.3.1. Положительно заряженный в растворе радикал
|
NH |
O |
O |
H2N |
N |
OH |
H2N |
OH |
|||
|
H |
|
|
|
|
NH2 |
NH2 |
Аргинин, Арг |
Лизин, Лиз |
Arg |
Lys |
|
O |
N |
OH |
|
|
HN |
NH2 |
Гистидин, Гис
His
8
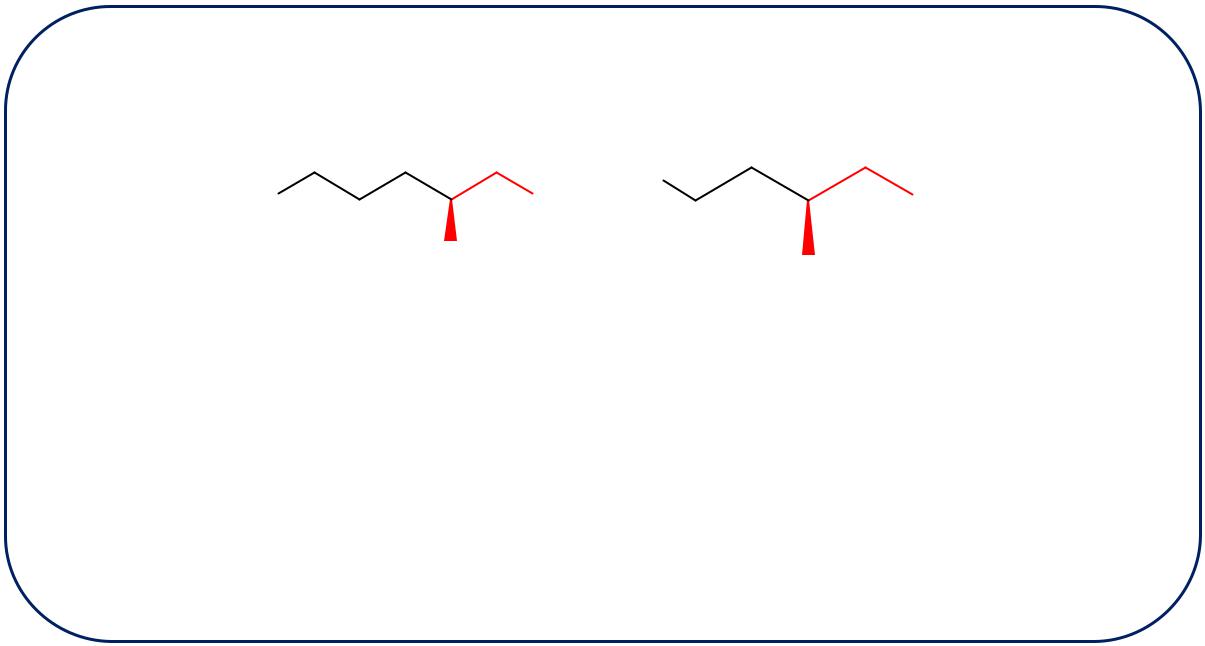
2.3 Аминокислоты с полярными ионогенными радикалами
2.3.2 Отрицательно заряженный в растворе радикал
O |
|
O |
|
|
|
|
O |
||||||
|
HO |
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|||
HO |
|
|
|
OH |
|
|
|
OH |
|||||
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NH2 |
O |
|
|
|
|
|
|||
|
|
|
|
NH2 |
|||||||||
Глутаминовая кислота, Глу |
|
|
|
||||||||||
Аспарагиновая кислота, Асп |
|||||||||||||
|
|
|
Glu |
|
|
|
Asp |
||||||
3.По биологической роли (заменимые и незаменимые)
—заменимые аминокислоты (Ала, Асп, Асн, Глу, Глн, Про, Гли, Сер) — синтезируются в организме;
—незаменимые аминокислоты (Вал, Лей, Иле, Мет, Фен, Три, Лиз, Se-Цис) — должны поступать с пищей;
—частично заменимые аминокислоты (Гис, Арг) — синтезируются медленно и в недостаточном количестве, особенно в детском возрасте;
—условно заменимые аминокислоты (Цис, Тир) — синтезируются из незаменимых аминокислот Мет и Фен, соответственно.
9
Физические свойства аминокислот
•Белые кристаллические вещества;
•высокие температуры плавления (более 200 °С);
•растворимы в воде;
•α-АК (кроме глицина) являются хиральными, оптически активны.
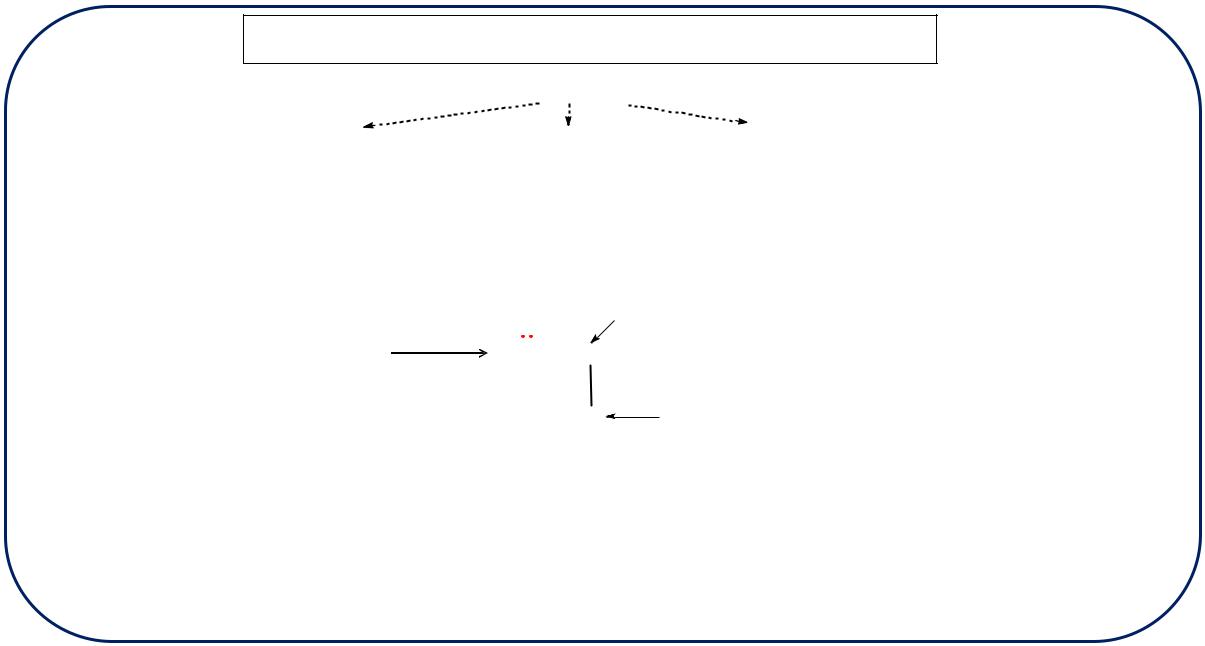
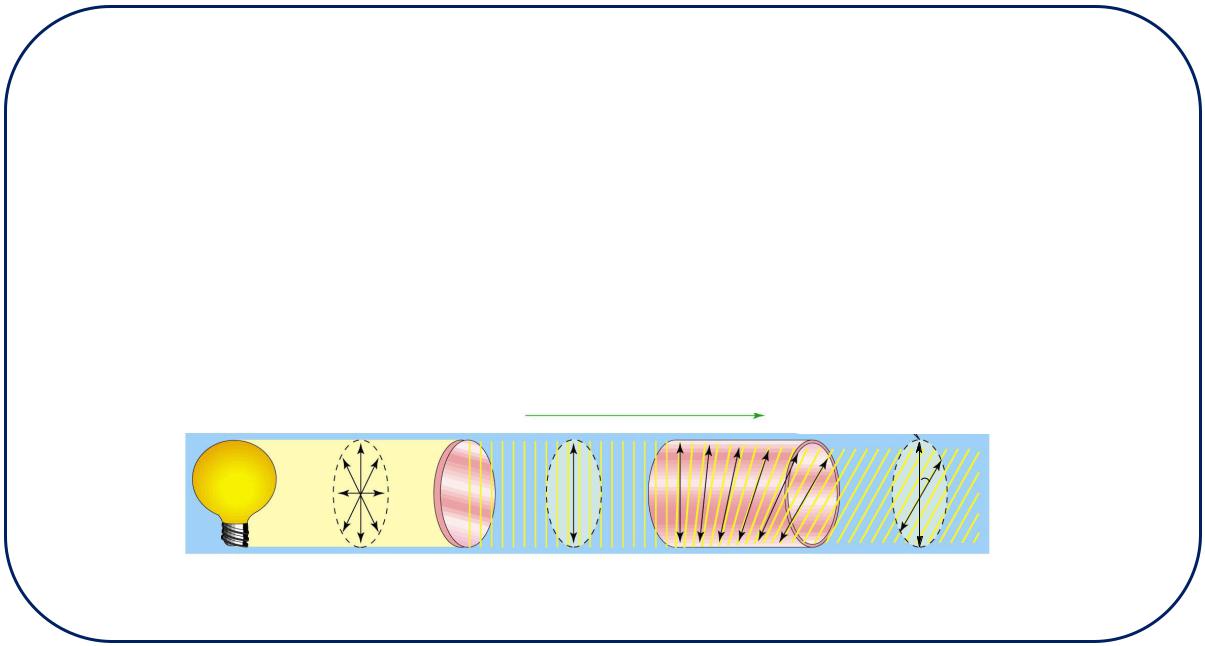
Оптическая активность — способность раствора или кристалла хиральной молекулы вращать плоскость плоскополяризованного света на определенный угол α.
Направление распространения света
Поворот плоскости поляризации
α
Источник |
Обычный |
Поляризатор |
Плоскополяризованный |
Трубка, содержащая |
Плоскополяризованный |
|
света |
свет |
свет |
оптически активное |
свет |
||
|
||||||
|
|
|
|
соединение |
|
1
0
