

Мономерные и олигомерые белки
|
. |
Белки – полимеры,состоящиеиз19 |
-а – аминокислотодной |
иминокислоты - пролина. |
|
Общформулааминокислотя
Радикалываминокисразделяютсяотах |
на: |
|
1Анионные. группы |
– СОО- |
|
2Катионн. группые |
|
– NH4+ |
3Полярные. незаряженныеОН |
|
|
4Непонярные. группыСН3 |
|
|
Аминокислотысодержащиеанионные,катионные, |
полярные |
|
незаряженные группы – гидрофильные. |
||
Неполярные группы – гидрофобные.
1Первичная. структурабелка |
|
Линейныйполимер,состоящийизаминокислот,соединённых |
|
пептиднойсвязьюмеждуа |
-карбоксильной -аминогруппой. |
2Вторичная. структурабелка
Альфаспираль Спираль,образовалинейнымполимеромаминокислотная,скрепленная водороднымисвязямимеждукислородомкарбоксильнойгруппы атомомводородааминогруппычетвотаминокислотыертойго

3Тре. стичнаяруктурабелка
Конформационныеизменениязасчетсвязеймежрадикаламиу
аминокислот |
|
|
|
1Ионная. связь |
– междуположительноотрицательнозаряженными |
||
радикалами |
|
|
|
2Водородная. связь |
|
|
– межгидрофнезаряженнойуилюбольн |
другойгидрофильной |
|
||
3Дисульфидная. связь |
|
|
– междудвумяостаткамицистеина |
4Гидрофобные. взаимодействия |
– междувсемигидрофобными |
||
радикалами. |
|
|
|
Конформацилабильноннаясть |
– свойствобелковизменятьсвою |
||
конформацию засчетразрываоднихобразованиядругихсвязей. |
|||
Нативная конформация – активная конформация белка. |
|||
Лиганды активныйцентр. |
|
||
Активныйцентр |
– учабелкас, токпецифическисвязываемый |
||
определеннмолекул( ой |
|
|
лигандом). |
Комплиментарность – пространственноехимическоесоответствие взаимповерхностейдйствующих
Роль лигандов функционированиибелков
Сложный белок – имеетвсвоемстроениинебелковую |
часть |
Гемоглобин (простетическая группа гем) |
|
1Альбумин. |
– переносжирных |
кислот |
|
|
2.Трипсин – расщеплениебелков |
|
|
||
Структурныеаналоги |
лигандов – усиливающиефункциибелка |
– |
||
агонисты,ослабляющиефункциибелка |
– антагонисты. |
|
||
АнтагонистыМ |
холинорецепторов – атропин |
|
||
Агонисты Н холинорецепторов – дитилин |
|
|||
Состоятизнесколькихполипептидныхцепей( |
протомеров), |
|||
соединёнгидрофобными,ио водороднымиых |
|
связями. |
||
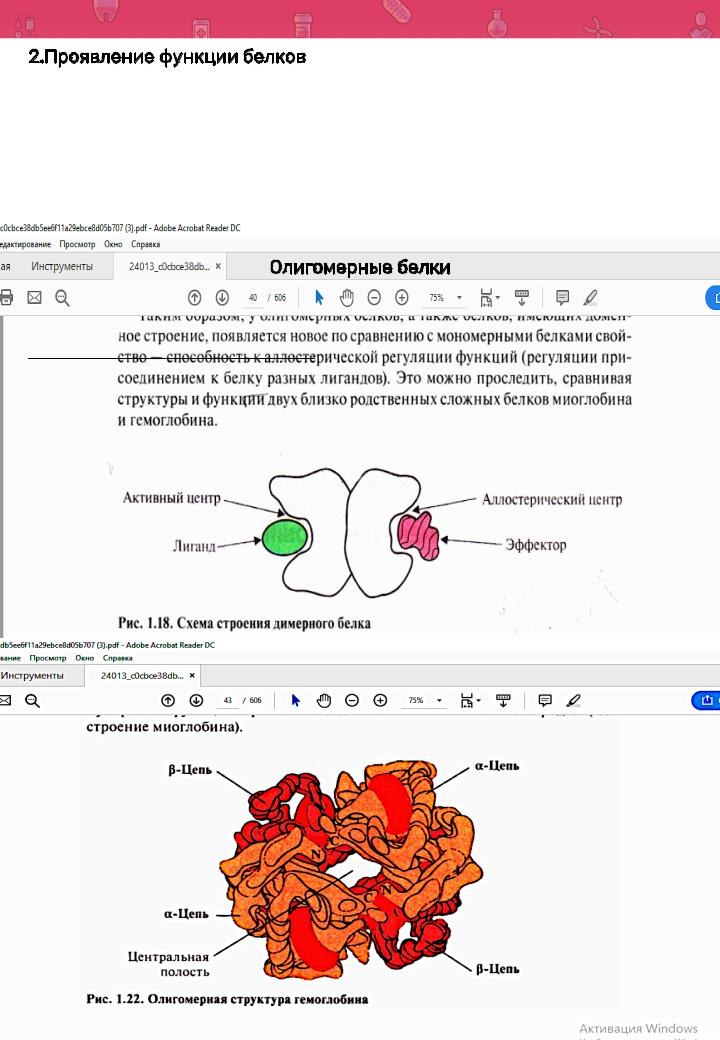
Четвертичная структурабелка |
. |
|
||
Гетеродимеры - разные протомеры Гомодимеры - одинаковые протомеры
Аллостецентрвыполняетрегуляторнуюическийфункцию.
Регуляцияприпомощиаллостерическогоцентраноситназвание аллостерической регуляции Эффекторы – актингибиторываторы.
2а2 b цепи4 |
гема. |

1)Гемоглобинэмбрио(2альфа2эпсилон)альный
2)Гемоглобинфет(2альфа2гамма)ный 3)Гемогловзрослого(альфа22б)етаин
ГисЕ7 |
– правильнориентО2длявзаяимодциясжел, ействиязом |
|
||
увеличиваетсродство |
гема с02,уменьшаетсродствоСО |
. |
||
Гис F8 – прочнофиксирует |
гем вактивном |
центре |
||
Активныйцентробразовангидрадикаламиофобнымидляпрепятствия |
|
|||
попавоокисленияданияыжелезав |
геме. |
|||
ИоныН+ |
|
протонируют гемоглобинумегоньшаютсродство |
|
|
кислородом. |
|
|
||
ЭффектБора |
– увеличениеколичествавысвобождаемогокислорода |
|
||
зависимостиотувеличенколичестваН+эр троцитахя |
|
|||
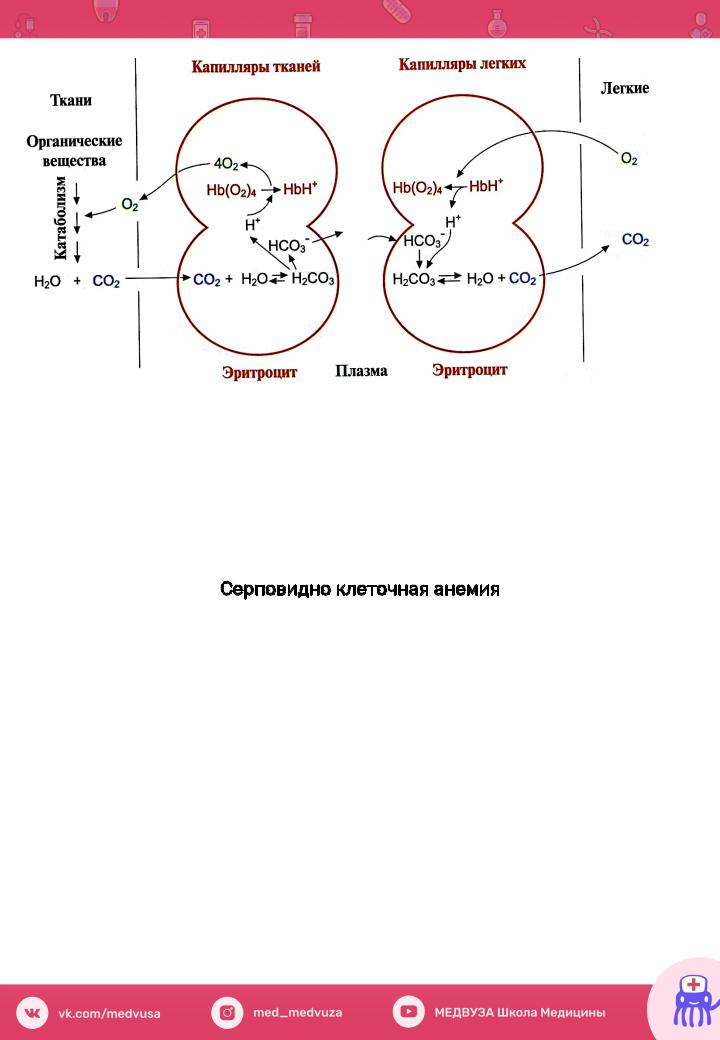
Чеминтенсфизнагрузкаичвнее,тбольшескаямобразуетсяСО2и |
|
|
Н+,темлегчегемоглобинотдаеткислородтка ям |
. |
|
Регуляция2,3БФГ |
. |
|
2,3 БФГсвязываясь |
дезоксигемоглобином вцентральнойполостив |
|
капиллярахткан,умесродствоньшаетйгемоглобинаккислороду |
. |
|
Обусловлена замвгемнгидрофильнойоглобаминокислотые (глутаминовой кислоты)нагидрофобнуюВалин( )вшестомположении бетацепи.
