
книги / Материаловедение и технологии современных и перспективных материалов
..pdfИзолированная система. Направление любого физико-химиче- ского процесса определяется характером взаимодействия системы с окружающей средой: dS/dt ≥ 0, где dS – энтропия.
Для изолированной системы характерно стремление к увеличению энтропии, т.е. самопроизвольность процессов. Это необратимые процессы.
Изолированные системы формируются при таких процессах, как:
•смешение, растворение, взаимная диффузия;
•смешение и разделение газов;
•загрязнение и очистка особо чистых веществ.
Взакрытой системе процессы самопроизвольны, если ∆G =
=∆H – T∆S < 0, т.е. T∆S > ∆H и ∆S > ∆H/T.
При ∆S < 0 возможна консервативная самоорганизация (супрамолекулярная химия и фазовые переходы): происходит в условиях, близких к термодинамическому равновесию.
Примеры – явления упорядочения в системах высокомолекулярных соединений при равновесных условиях (в частности, образование ДНК):
•наносостояние вещества;
•образование сложной структуры в процессе кристаллизации;
•кристаллизация (полигонизация);
•спекание, рекристаллизация в поликристаллических системах;
•образование магнитных и ферроэлектрических доменов;
•мартенситные превращения (упорядочение, сегрегация);
•нагрев;
•спинодальный распад, самораспространяющийся высокотемпературный синтез (СВС);
•полимеризация.
Открытая система (диссипативная система): dS/dt << 0, возможная диссипативная самоорганизация. Диссипативная система,
или диссипативная структура (от лат. dissipatio – рассеиваю, раз-
рушаю) – это открытая система, которая оперирует вдали от термодинамического равновесия. Иными словами, это устойчивое состояние, возникающее в неравновесной среде при условии диссипации
31
(рассеивания) энергии, которая поступает извне. Диссипативная сис-
тема иногда называется еще стационарной открытой системой или неравновесной открытой системой.
1.3.2.Диссипативная самоорганизация (синергетический подход)
Определение, данное Г. Хакеном в 1980-е гг. в рамках синергетики: «Самоорганизация – процесс упорядочения (пространственного, временного или пространственно-временного) в открытой системе, за счет согласованного взаимодействия множества элементов ее составляющих».
Характеристики диссипативной системы:
•открытая (наличие обмена энергией/веществом с окружающей средой);
•содержит неограниченно большое число элементов (подсис-
тем);
•имеется стационарный устойчивый режим системы, в котором элементы взаимодействуют хаотически (некогерентно);
•новое состояние существует только при безостановочном потоке энергии/вещества в систему. При увеличении интенсивности обмена система проходит через ряд следующих критических переходов; в результате структура усложняется вплоть до возникновения турбулентного хаоса.
Примерами открытых систем являются:
•поведение фотонов в лазерах;
•динамика биологических популяций (рис. 1.16);
•конвекция воздушных масс (рис. 1.17);
•поведение жидкости в турбулентных системах, ячейки Бенара
(рис. 1.18);
•волны в плазме;
•химические колебательные реакции (Белоусов–Жаботинский) (рис. 1.19, 1.20).
32

На рис. 1.16 показано соотношение числа волков и зайцев в некотором гипотетическом заповеднике, где на огражденной территории живут только эти представители фауны, а флоры здесь много. Поскольку волки – хищники, то могут в данном заповеднике питаться только зайцами, а жертвы-зайцы питаются только травкой. В конечном счете нас интересует, будет ли такое экологическое сообщество устойчиво сосуществовать в заповеднике. Экспериментальные данные, полученные в реальной многокомпонентной и открытой среде с множеством неучтенных взаимодействий, указывают на факт наличия устойчивых колебаний популяций, свидетельствуют о том, что модель работоспособна и оправдывает надежды по предсказанию.
Рис. 1.16. Динамика популяций хищников и их жертв – самоорганизация в биологии
Циркуляционные потоки в атмосфере и океанах Земли – это пример самоорганизации на Земле (см. рис. 1.17). Общей циркуляцией атмосферы называют замкнутые течения воздушных масс в масштабах полушария или всего земного шара, приводящие к широтному и меридиональному переносу вещества и энергии в атмосфере. Главной причиной возникновения воздушных течений в атмосфере служит неравномерное распределение тепла на поверхности Земли, что приводит к неодинаковому нагреванию почвы и воздуха в различных поясах земного шара. Таким образом, солнечная энергия является первопричиной всех движений в воздушной оболочке Земли.
Ячейки Бенара – самоорганизация в физических явлениях. Ячейки Бенара, или Рэлея–Бенара – возникновение упорядоченности
33

Рис. 1.17. Пример диссипативной самоорганизации систем – циркуляционные потоки
ватмосфере и океанах Земли
ввиде конвективных ячеек в форме цилиндрических валов или правильных шестигранных структур в слое вязкой жидкости с вертикальным градиентом температуры, т.е. равномерно подогреваемой снизу (см. рис. 1.18). В качестве жидкости используется, как правило, силиконовое масло.
Рис. 1.18. Ячейки Бенара
Реакция Белоусова–Жаботинского – химическая реакция, в которой возникают хаотические автоколебательные процессы. В настоящее время найдены многие реакции с таким свойством. В 1951 г. Б.П. Белоусов обнаружил автоколебания в реакции окисления бромата калия КBrO3 малоновой кислотой HOOC–H2–COOH в кислотной среде в присутствии катализатора – ионов церия Ce3+. Течение реак-
34

ции меняется со временем и раствор периодически меняет цвет от бесцветного (Ce3+) к желтому (Ce4+) и обратно (см. рис. 1.19). Эффект еще более заметен в присутствии индикатора pH ферроина. Наиболее эффектно выглядит колба, если вместо лимонной кислоты использовать малоновую, а вместо ионов церия ионы железа Fе2+. Тогда раствор в колбе может часами со строгой как часы периодичностью изменять цвет во всем видимом диапазоне от рубиново-красного до не- бесно-голубого.
Рис. 1.19. Реакция Белоусова–Жаботинского
Сообщение Белоусова было встречено в научных кругах скептически, поскольку считалось, что автоколебания в химических системах невозможны. Некоторые конфигурации возникают при реакции Белоусова–Жаботинского в тонком слое в чашке Петри (см. рис. 1.20).
Рис. 1.20. Узоры в чашке Петри, возникающие при реакции Белоусова– Жаботинского
35
В 1961 г. механизм реакции Белоусова был объяснен аспирантом Анатолием Жаботинским, но эта работа оставалась малоизвестной до 1968 г. В 1969 г. Жаботинский с коллегами обнаружили, что если реагирующую смесь «разлить» тонким плоским слоем, в нем возникают волны изменения концентрации, которые видны невооруженным глазом в присутствии индикаторов (см. рис. 1.20). Таким образом, имеется автоколебательный процесс изменения концентрации четырехвалентного церия с одновременным варьированием цвета – на поверхности раствора появляются поверхностные волны (химические спиральные волны).
1.3.3. Теория катастроф
Возникновение нового качества происходит на основании усиления малых случайных движений элементов – флуктуаций. В теории неравновесной термодинамики новая структура всегда является результатом раскрытия неустойчивости в результате флуктуаций. Можно сказать о «порядке через флуктуации». Таким образом, пороговый характер самоорганизации связан с переходом из одного стационарного состояния в другое. Потеря системой устойчивости называется катастрофой.
Катастрофа – это скачкообразное изменение, возникающее при плавном изменении внешних условий. Иллюстрацией к потере устойчивости может быть положение шарика на сложной траектории
(рис. 1.21).
Переход к новому состоянию под действием флуктуации называется явлением бифуркации. Например, если «бутылку» с сообщением бросить в реку точно на середину, она проплывет через правый или левый рукав в зависимости от случайного действия около точки «волнореза» В (рис. 1.22). В сложных системах параметр (характеристика или свойство системы) X может изменяться под действием управляющего (или возмущающего) параметра λ. Рассмотрим диаграмму (X, λ). Оказывается, что при малых λ существует одно решение, характеризующее термодинамически устойчивое состояние,
36
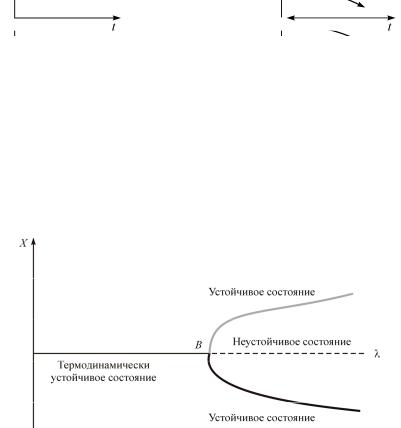
а при больших λ существует два устойчивых состояния с разными значениями X. Переход к новому состоянию при λкр под действием флуктуации называется явлением бифуркации.
а |
б |
в |
Рис. 1.21. Устойчивое (а), локально устойчивое (б) и неустойчивое (в) состояние системы (шарика)
Рис. 1.22. Термодинамически устойчивое и неустойчивое состояние системы около точки «волнореза»
Значение элементарной теории катастроф состоит в том, что она сводит огромное многообразие ситуаций, встречающихся на практике, к небольшому числу стандартных схем, которые можно детально
37
исследовать раз и навсегда. Сейчас теория катастроф широко применяется в механике конструкций, метеорологии, аэродинамике, оптике, теории кооперативных явлений, квантовой динамике. Но главное заключается в том, что эта теория подводит эффективную стандартную базу под описание качественных изменений в нелинейных уравнениях, моделирующих системы, далекие от равновесия. Она является основой анализа в теории бифуркаций, в теории переходов термодинамических систем в новые структурные состояния.
Исторический процесс роста населения мира, его внутренняя устойчивость, сокращение периодов колебаний (численности и пространственного распределения населения) на фоне общей тенденции роста и даже примерное количество периодов, предположительно, объясняются синергетической моделью. Прохождение глобальной системы населения земного шара через состояние асимптотической неустойчивости, через «момент обострения», естественно, рождает вопрос об образах будущего. Что можно ожидать? Каким будет демографический переход для всего человечества? И переход куда? Возникает возможность попадания в длительный процесс падения численности и рассредоточения населения по пространству. Возможно частичное вымирание человечества и сохранение лишь «золотого миллиарда», проживающего в «глобальной деревне». Возобновление закона роста возможно лишь после длительного прохождения «петли затухания» процессов, «ухода в прошлое» и децентрализации. Варианты развития Земли с «человечеством» и «без человечества».
1.4. Физико-химические принципы конструирования новых материалов
1.Принцип периодичности – закономерное изменение свойств материалов в соответствии с периодичностью свойств составляющих их элементов (закон Д.И. Менделеева).
2.Принцип структурного дизайна – создание новых кристалли-
ческих структур на основе использования кристаллохимических осо-
38
бенностей элементов путем сочетания различных стандартных структурных блоков (супрамолекулярные, гибридные материалы, соединения внедрения в графит).
3.Принцип химического, термодинамического и структурного подобия – предсказание свойств неизвестных материалов по аналогии с их известными представителями.
4.Принцип непрерывности и соответствия компонентов рав-
новесной системы, ограничения числа независимых параметров состояния в равновесной системе – использование правила фаз Гиббса для предсказания условий получения материалов.
5.Принцип структурного разупорядочения и непостоянства состава твердофазных соединений – существование равновесных
инеравновесных дефектов, а также областей гомогенности по катионам и анионам во всех фазах, составляющих материалы (зависимость функциональных свойств от типа и концентрации дефектов – суперионики, полупроводники, высокотемпературные сверхпроводники).
6.Принцип химического, структурного и фазового усложнения состава – коррекция функциональных характеристик за счет легирования или создания композитов.
7.Принцип химической, гранулометрической и фазовой одно-
родности – создание высокогомогенных на уровне химического состава и размера зерен матреиалов с одним и тем же фазовым составом для любой анализируемой области (методы химической гомогенизации).
8.Принцип эквивалентности источников беспорядка в условиях минимизации свободной энергии (принцип А. Вейла) – твердофазный материал в равновесных условиях приобретает тот вид дефектов, который при наименьших энергетических затратах обеспечивает максимальное увеличение энтропии (уменьшение коэффициента термического расширения оксида кремния при легировании оксидом олова).
9.Принцип одинакового эффекта различных физико-химических воздействий – химическое модифицирование и различные энергетические (тепловые и нетепловые) воздействия, которые могут привес-
39
ти к одному и тому же результату (получение сплавов расплавлением или механическим легированием в твердом состоянии).
10.Принцип неравноценности объема и поверхности (И.В. Та-
нанаев) – существование для материалов зависимости «состав– структура–дисперсность–свойство» (материалы с различным размером зерен).
11.Принцип синергетического эффекта различных физико-
химических воздействий – суммарный эффект различных воздействий может приводить к качественно новому результату (совместное действие температуры и микроволн, ультразвука и температуры, механоактивация).
12.Принцип метастабильного многообразия – существование целого ряда метастабильных материалов одного и того же состава, но со своим набором свойств (углеродные материалы).
13.Принцип симметрии (принцип Кюри). Природа осуществила деление на симметричные части и золотые пропорции. В частях проявляется повторение строения целого.
Пьер Кюри в начале нашего столетия сформулировал ряд глубоких идей симметрии. Он утверждал, что нельзя рассматривать симметрию какого-либо тела, не учитывая симметрию окружающей среды, а скалярные термодинамические силы не могут оказывать влияние на векторные тензорные.
Закономерности «золотой» симметрии проявляются в энергетических переходах элементарных частиц, в строении некоторых химических соединений, в планетарных и космических системах,
вгенных структурах живых организмов. Эти закономерности есть
встроении отдельных органов человека и тела в целом, а также проявляются в биоритмах и функционировании головного мозга и зрительного восприятия.
Прежде всего, П. Кюри показал, что у конечных фигур (геометрических) существует всего семь групп симметрии (так называемых предельных групп). Смысл слова «предельный» означает, что тела вращения могут рассматриваться как фигуры, получаемые в результате бесконечного увеличения числа граней многогранников. Пре-
40
