
Термодинамика
Что такое энтальпия системы?
– теплосодержание системы.
Самопроизвольно протекают процессы…
– которые идут с увеличением энтропии.
Энтропия тем больше чем…
– больше неупорядоченность системы.
Открытая система по отношению к окружающей среде…
– обменивается с ней массой и энергией.
Что такое внутренняя энергия?
– сумма энергий всех микрочастиц системы, без кинетической и потенциальной.
Что такое энтальпия системы?
– сумма
внутренней энергии и работы расширения

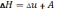 ,
где
,
где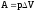
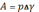 .
.
Изолированная система…
– не обменивается с окружающей средой ни массой, ни энергией
Уравнение для расчета свободной энергии Гиббса:
– 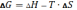
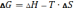 .
.
Чем измеряется тепловой эффект реакции в изобарных условиях?
– изменением энтальпии.
Как меняется энтропия системы, если протекает самопроизвольный спонтанный процесс?
– увеличивается.
Комплексные соединения
Чем определяется заряд комплексного иона
– Зарядом внешней сферы, взятым с обратным знаком
Что такое координационное число
– Число связей, связывающих центральный атом (комплексообразователь) с лигандами
Роль атомов и катионов металла в комплексных соединениях
– Центральный атом, комплексообразователь
Какие частицы играют роль лигандов
– Анионы электролитов и нейтральные молекулы
Тип связи в комплексные соединения
– Ковалентная, донорно-акцепторная
Степень окисления комплексообразователя в К[А1(ОН)4]
– +3
Какие частицы играют роль комплексообразователя
– Атомы и катионы металлов
Найти комплексообразователь в К3[А1(ОН)6]
– А13+
Определить координационное число в K2[Zn(OH)4]
– 4
Указать частицы лиганды в комплексе K2[Be(S04)2]
– их дентантность S042-, лиганд бидентантный
Чему равно координационное число в [Cu(NH3)4(OH)2]
– 6
Комплексная соль K4[Fe(CN)6]. Определить внешнюю и внутреннюю сферу
– К+ - внешняя сфера [Fe(CN)6]4- - внутренняя сфера
Что характеризует дентатность лиганда
– Число связей центрального атома с лигандом
14. K3[Fe(SCN)6]
– C.O. железа - +3
15. K2[Zn(SO4)2]
– координационнное число – 4
Осмос
Какие условия нужны для возникновения осмоса
– Контакт двух растворов с разной концентрацией через полупроницаемую мембрану.
Закон Вант-Гоффа для осмотического давления
– P=CRT – для неэлектролитов (сахароза, глюкоза)
– R=iCRT – для электролитов (соли, кислоты, щелочи)
Уравнение для расчета осмотического давления
– KCl – P=2CRT
– CuCl2 – P=3CRT
– AlCl3 – P=4CRT
– Al2(SO4)3 – P=5CRT
Укажите раствор с наибольшим осмотическим давлением
– AlCl3 (распадается на наибольшее число ионов)
Формула для расчета изотонического коэффициента
– Зависит от степени диссоциации электролита
– і=1+α(δ-1)
Чему равен pH крови в норме
– pH=7.35-7.45
Что такое «депрессия крови»
– Понижение температуры замерзания плазмы крови по сравнению с водой
Что такое гемолиз
– Разрыв оболочек эритроцитов, помещенных в гипотонический раствор
Что такое плазмолиз
– Сжатие эритроцитов, помещенных в гипертонический раствор
Формула для расчета осмотического давления
– P=CRT
Формула для повышения температуры кипения сахарозы
– Δtкип=Em
Как изменится температура кипения воды, если в ней растворить некоторое количество сахара
– Повысится
От каких факторов зависит осмотическое давление раствора
– От молярной концентрации растворенного вещества
Какой раствор NaCl изотоничен крови
– 0,9% NaCl
Как изменится температура замерзания, если добавить растворенное вещество
– Понизится
Какие растворы называют гипотонические
– Растворы, осмотическое давление которых меньше чем у крови
Изотонические растворы по отношению друг к другу
– Имеют одинаковые осмотические давления
Какие растворы называют гипертоническими
– Растворы, осмотическое давление которых больше чем у крови
Укажите причину отеков
– Уменьшается осмотическое давление крови
Что такое онкотическое давление крови
– Давление крови, обусловлено белками
Чему равно осмотическое давление крови
– P=7,7 – 8 атм
Укажите раствор для лечения гнойных ран
– Гипертонический, 2% NaCl
Укажите физиологические растворы
– 0,9%- NaCl
– 5% - глюкозы
Каким методом можно определить осмотическую концентрацию раствора
– Криометрия
25. От чего не зависят коллигативные свойства
- от природы вещества
