- •Саратовский государственный технический университет
- •Краткий очерк истории развития физической химии
- •Разделы физической химии
- •1 Основы термодинамики
- •1.1 Природа энергии
- •1.2 Энергетические эффекты в химических реакциях
- •1.3 Энтальпия
- •1.4 Закон Гесса
- •1.5 Теплоты образования
- •1.6 Измерение изменений энергии, калориметрия
- •1.7 Теплотворная способность топлив и пищи
- •1.8 Потребление энергии: тенденции и перспективы
- •2 Химическая кинетика. Химическое равновесие
- •2.1 Скорость химических реакций
- •2.2 Зависимость скорости реакции от концентрации. Закон действия масс
- •2.3 Влияние температуры на скорость реакции. Правило Вант-Гоффа
- •2.4 Химическое равновесие и его смещение
- •2.4.1 Влияние изменения концентрации веществ на смещение химического равновесия
- •2.4.2 Влияние изменения давления на смещение химического равновесия, если в реакции участвуют газообразные вещества
- •2.4.3 Влияние изменения температуры на смещение химического равновесия
- •3 Свободная энергия. Энтропия и равновесие
- •3.1 Самопроизвольные процессы
- •3.2 Самопроизвольные процессы и изменение энтропии
- •3.3 Интерпретация энтропии на молекулярном уровне
- •3.4 Вычисление изменений энтропии
- •3.5 Функция свободной энергии
- •3.6 Свободная энергия и константа равновесия
- •4 Аналитические выражения основых законов термодинамики
- •4.1 Термодинамическая система и термодинамические функции.
- •Первый закон термодинамики
- •4.2 Второй закон термодинамики. Теорема Карно
- •4.3 Постулат Планка. Абсолютное значение энтропии
- •4.4 Характеристические функции. Приложение второго закона термодинамики
- •4.4.1 Изохорно-изотермический потенциал
- •4.4.2 Изобарно-изотермический потенциал
- •4.4.3 Уравнение максимальной работы (уравнение Гиббса-Гельмгольца)
- •4.4.4 Термодинамические потенциалы. Характеристические функции. Условия равновесия
- •4.5 Фазовые переходы. Уравнение Клайперона-Клаузиуса
- •4.5.1 Фазовые переходы первого рода. Плавление. Испарение
- •5 Поверхностные явления. Адсорбция
- •5.1 Изотеормы адсорбции газов. Уравнение Генри
- •5.2. Уравнение Лэнгмюра. Адсорбция смеси газов
- •5.3 Уравнение изотермы адсорбции паров Брунауера, Эммета и Теллера (уравнение бэт)
- •6 Правило фаз гиббса. Равновесие гетерогенных систем
- •6.1 Однокомпонентные системы
- •6.2 Двухкомпонентные системы с одной фазой переменного состава
- •6.2.1 Диаграмма плавкости двухкомпонентных систем, не образующих химических соединений и твердых растворов
- •6.2.2 Диаграммы плавкости систем, компоненты которых образуют химическое соединение
- •6.3 Термический анализ
- •6.4 Физико-химический анализ
- •7 Термодинамика и кинетика твердофазного
- •7.2 Основные типы реакций взаимодействия соединяемых материалов
- •I. Кристаллохимические реакции замещения катиона оксида.
- •III. Реакции взаимного растворения оксидов.
- •IV. Образование нового оксида при переменной валентности катиона.
- •V. Окисление металла в контакте с оксидами переменного состава.
- •VI. Реакции растворения оксида в металле.
- •VII. Реакции с частичным окислением свариваемого металла
- •7.3 Термодинамика и кинетика формирования соединений при слабом химическом взаимодействии материалов
3.2 Самопроизвольные процессы и изменение энтропии
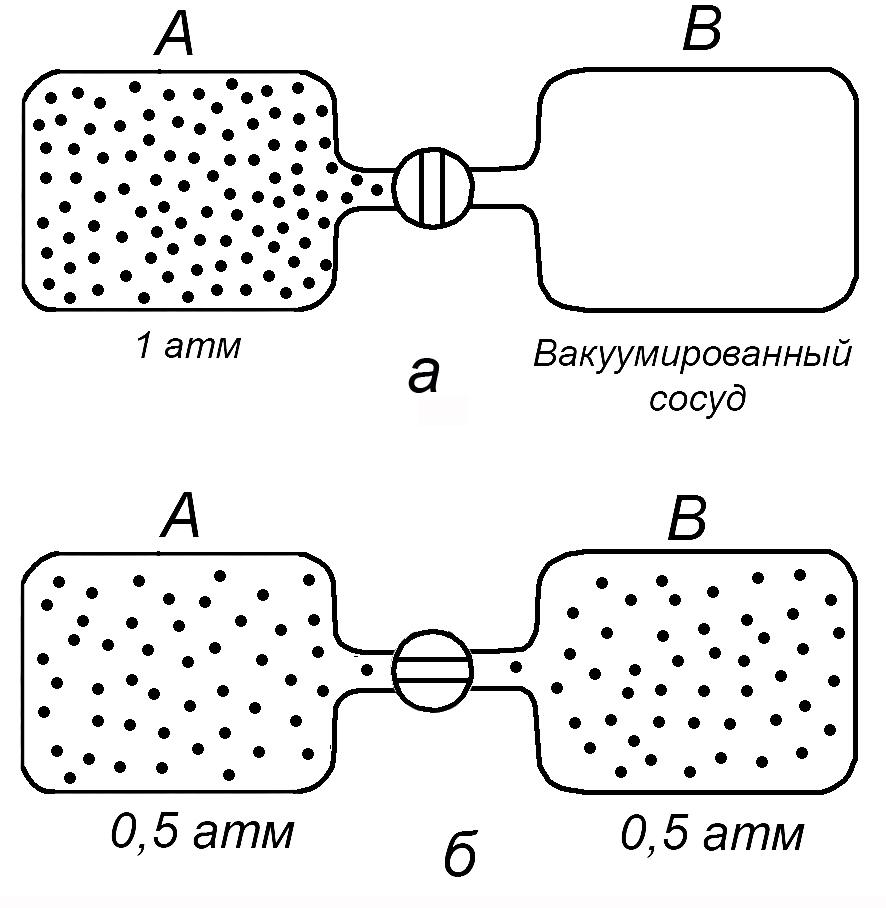
Нетрудно найти процессы, являющиеся самопроизвольными, несмотря на то, что они не относятся к экзотермическим. Рассмотрим, например, идеальный газ, заключенный в некотором сосуде (рис. 3.1). Допустим, что этот сосуд соединен трубкой с краном с другим сосудом объемом 1 л, из которого откачан воздух. Теперь представим себе, что мы открыли кран. Есть ли какие-нибудь сомнения в том, что должно произойти? Понятно, что газ должен расширяться во второй сосуд до тех пор, пока давление не распределится равномерно по обоим сосудам, т. е. станет равным 0,5 атм в каждом. В процессе расширения, т.е. в процессе увеличения объема, идеальный газ не получает и не отдает теплоту. Тем не менее, процесс является самопроизвольным. Обратный процесс, в котором газ, равномерно распределенный между двумя сосудами, внезапно полностью переместится в один из сосудов, а другой сосуд останется пустым, совершенно неправдоподобен. Однако и этот процесс протекал бы без выделения или поглощения теплоты. Очевидно, что процесс самопроизвольного расширения газа должен определяться еще каким-то важным фактором помимо выделения или поглощения теплоты.
В качестве второго примера рассмотрим плавление льда при комнатной температуре. Процесс, описываемый уравнением:
Н2О (тв.) → Н2О (ж.) (3.3)
при 27°С, как известно, происходит совершенно самопроизвольно. Однако это превращение представляет собой эндотермический процесс. Плавление льда при температуре выше 0°С служит примером самопроизвольного эндотермического процесса.
К такому же типу процессов относится, эндотермическое растворение многих солей в воде. Если поместить хлорид калия КС1 в воду при комнатной температуре и помешивать соль в воде, то можно почувствовать, что по мере ее растворения сосуд с раствором постепенно охлаждается. Следовательно, процесс, описываемый уравнением:
КСl (тв.) → Н2О → КСl (водн.) (3.4)
является эндотермическим и, несмотря на это самопроизвольным.
|
Все три описанных выше процесса имеют что-то общее, что объясняет причину их самопроизвольного протекания. В каждом случае состояние продуктов характеризуется большей хаотичностью, или неупорядоченностью, чем состояние реагентов. Обсудим каждый случай подробнее. Если газ заключен в сосуд объемом 1 л, как показано на рис. 3.1.а, то положение каждой молекулы газа можно определять относительно данного ограниченного объема. После того как газ расширится, нельзя с уверенностью |
Рис. 3.1. Расширение идеального газа в свободное пространство: а - в сосуде А находится идеальный газ под давлением 1 атм, из сосуда В откачан воздух; б - кран трубки, соединяющей сосуды, открыт. При расширении газ занимает оба сосуда, создавая в них давление 0,5 атм. |
сказать, какая из молекул газа в каждый момент времени находится в исходном объеме, а какая в другом сосуде. Поэтому приходится определять положение каждой молекулы в пространстве вдвое большего объема. Другими словами, поскольку молекулы газа теперь находятся в пространстве вдвое большего объема, их состояние является более хаотичным, чем когда они были заключены в исходном сосуде меньшего объема.
|
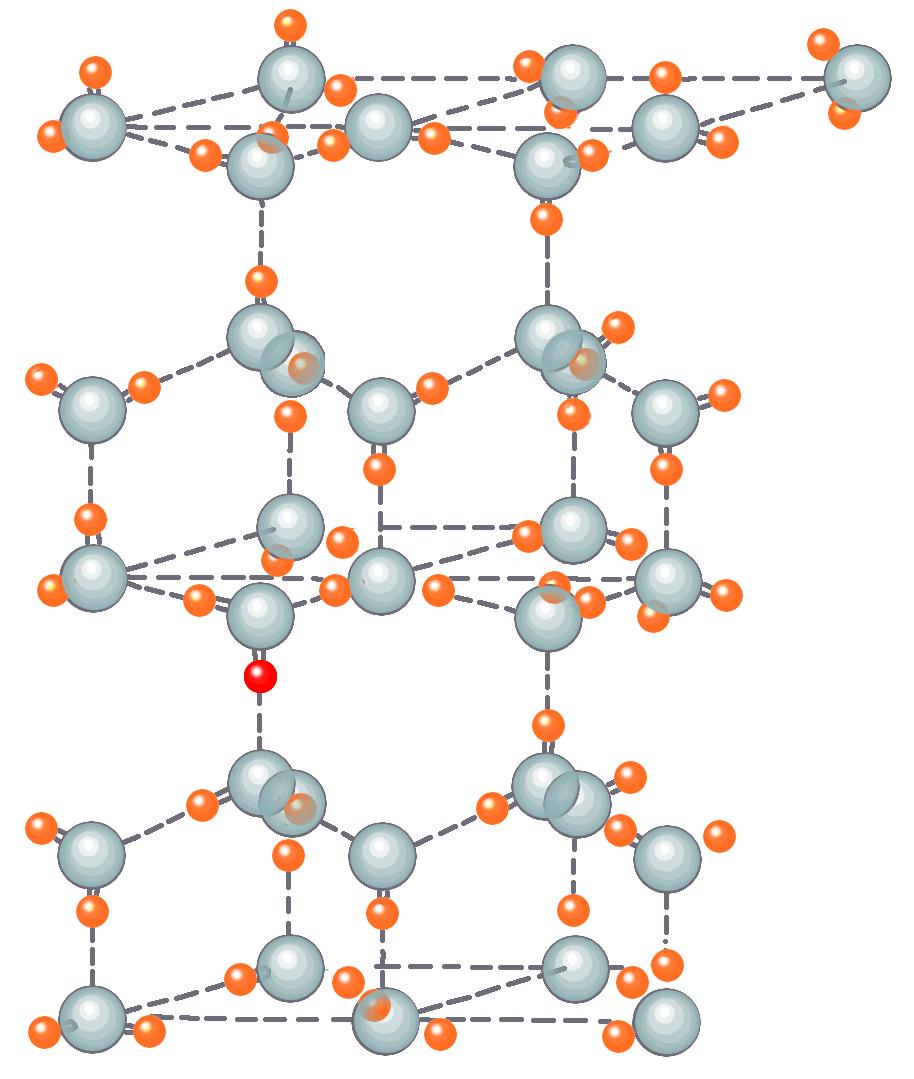
Рис. 3.2. Кристаллическая структура льда. |
Молекулы воды, образующие кристалл льда, прочно удерживаются в его кристаллической решетке. При плавлении льда молекулы воды получают возможность свободно перемещаться относительно друг друга и обмениваться местами. Следовательно, распределение индивидуальных молекул в жидкой воде характеризуется большей хаотичностью, чем в кристаллической. Высокоупорядоченная кристалли-ческая структура заменяется крайне неупорядоченной структурой жидкости. Аналогичная ситуация возникает при растворении КCl в воде, хотя здесь следует проявлять большую осторожность в рассуждениях. |
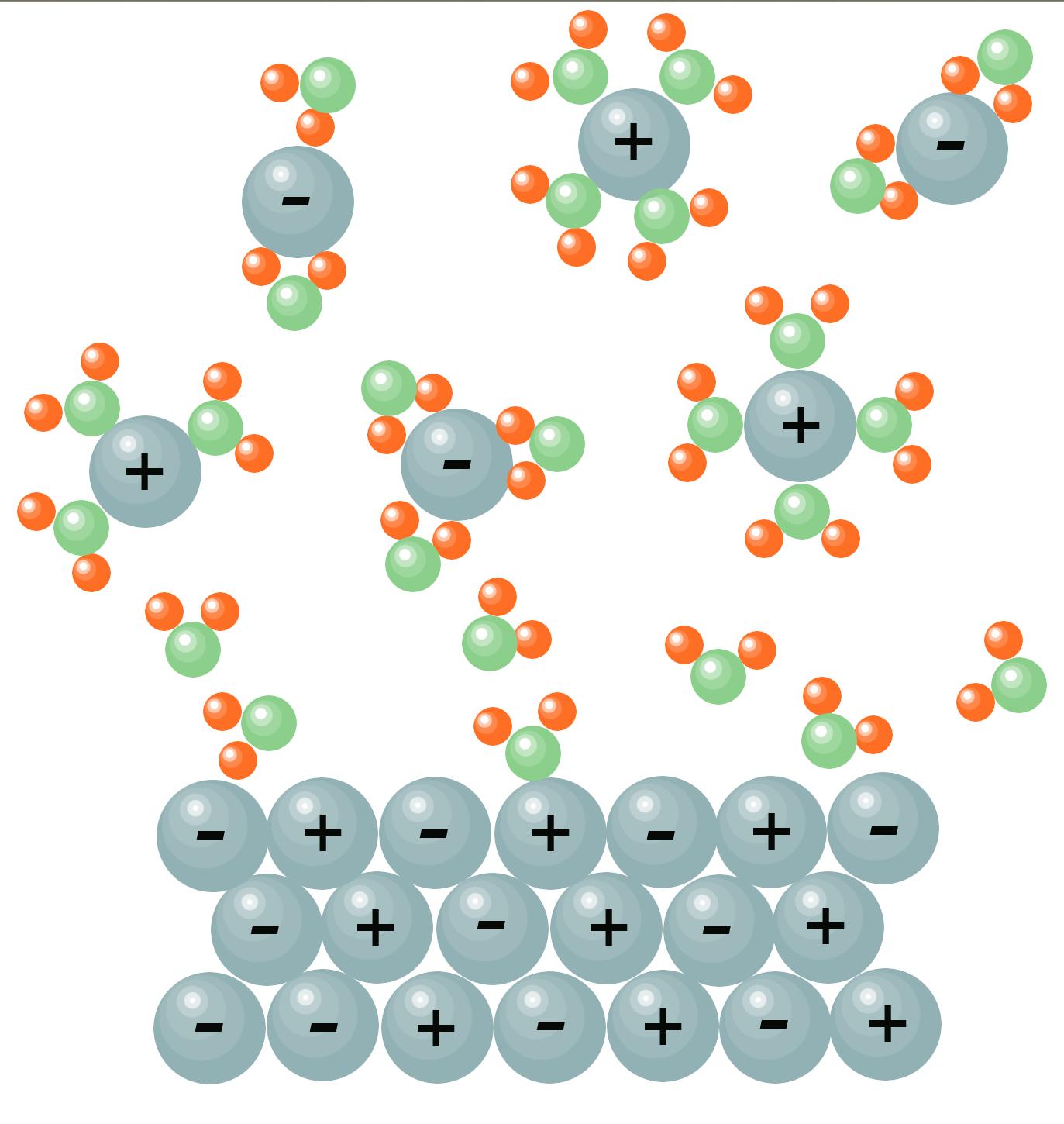
В твердом КCl ионы К+ и Cl- находятся в высокоупорядоченном кристаллическом состоянии. При растворении твердой соли ионы получают возможность свободно перемещаться в воде. Очевидно, они находятся в более хаотичном и неупорядоченном состоянии, чем прежде. Правда, в то же время молекулы воды связываются с ионами, образуя вокруг них гидрат, как показано на рис. 3.3.
|
Рис. 3.3. Изменения в степени упорядоченности ионов и молекул растворителя при растворении ионного твердого вещества в воде. |
|
Распределение ионов в пространстве становится более хаотичным, а распределение гидратных молекул воды вокруг ионов становится менее хаотичным.
Молекулы гидратной воды оказываются в более упорядоченном состоянии, чем прежде, поскольку их расположение ограничено ближайшим окружением ионов. Следовательно, растворение соли включает одновременно процессы упорядочения и разупорядочения.
Преобладающими оказываются процессы разупорядочения, поэтому результирующим эффектом является повышение беспорядка при растворении соли в воде.
УПРАЖНЕНИЕ 3.1
Для каждого из следующих случаев укажите, приводит ли процесс к повышению или понижению хаотичности, т.е. беспорядка, в системе:
a) 4Fe (тв.) + 3О2 (г.) → 2Fe2O3 (тв.)
б) Ag+(водн.) + Сl-(водн.) → AgCl (тв.)
в) Н2О (ж.) → Н2О (г.)
Решение: Процесс «а» приводит к уменьшению беспорядка, поскольку газ превращается в часть кристаллической решетки. Структурные единицы кристаллической решетки оксида намного более упорядочены и ограничены определенными положениями, чем молекулы газа. (Отметим, что эта реакция протекает самопроизвольно, несмотря на общее уменьшение хаотичности. Дело в том, что она является сильно экзотермичной. Результаты, к которым приводят одновременное изменение энтальпии и изменение хаотичности системы, обсуждаются в разд. 3.5).
Процесс «б» также характеризуется уменьшением хаотичности, поскольку ионы, свободно перемещавшиеся в объеме раствора, образуют твердое вещество, в кристаллической решетке которого они ограничены строго определенными положениями.
Процесс «в» протекает с повышением хаотичности, или беспорядка, поскольку молекулы воды в газовой фазе распределены в намного большем объеме, чем в жидкой фазе.
Как
показывают рассмотренные выше примеры,
самопроизвольное протекание процесса
связано с повышением хаотичности, или
неупорядоченности, системы. Степень
неупорядоченности выражается
термодинамической величиной, называемой
энтропией,
которая обозначается латинской буквой
![]() .
Чем
больше хаотичность системы, тем больше
ее энтропия. Подобно энтальпии, энтропия
является функцией состояния (см. разд.
1.3.). Изменение энтропии, сопровождающее
процесс
.
Чем
больше хаотичность системы, тем больше
ее энтропия. Подобно энтальпии, энтропия
является функцией состояния (см. разд.
1.3.). Изменение энтропии, сопровождающее
процесс
![]() ,
зависит только от исходного и конечного
состояний системы, но не от конкретного
пути, по которому происходит переход
из одного состояния в другое.
,
зависит только от исходного и конечного
состояний системы, но не от конкретного
пути, по которому происходит переход
из одного состояния в другое.
ВТОРОЙ ЗАКОН ТЕРМОДИНАМИКИ
С помощью введенного выше понятия энтропии мы можем по-иному обсудить второй закон термодинамики и его применения. Говоря, в разд. 3.1, о самопроизвольных процессах, мы упомянули, что второй закон предназначен для установления направления процессов; это связано с представлением, что процессы, протекающие самопроизвольно в одном направлении, в противоположном направлении не являются самопроизвольными. Такое представление применимо не только к химическим превращениям, но вообще к любым процессам.
Всем известно, что теплота самопроизвольно передается от горячих предметов к более холодным. Мы знаем также, что для передачи теплоты в обратном направлении, от холодных предметов к более горячим или от системы с некоторой температурой к окружающей среде с более высокой температурой, необходимо затрачивать энергию. Например, для того чтобы внутри холодильника поддерживалась более низкая температура, чем в кухне, где он стоит, требуется затрачивать электрическую энергию.
С этим связано и менее очевидное соображение, что теплоту нельзя полностью превратить в работу. Некоторая часть теплоты при этом всегда передается окружающей среде. Например, при работе паровой турбины тепловая энергия перегретого пара превращается в электрическую энергию; кинетическая энергия молекул пара превращается в кинетическую энергию движущихся лопастей турбины и, в конце концов, в электрическую энергию. Но не вся кинетическая энергия молекул пара превращается в кинетическую энергию турбины. Некоторая часть энергии теряется в окружающую среду в виде теплоты. Каждая электростанция вызывает тепловое загрязнение окружающей среды. Законы термодинамики говорят, что это неизбежно. В самом деле, одной из первых формулировок второго закона термодинамики было утверждение, что теплоту нельзя полностью превратить в полезную работу.
Существует множество формулировок второго закона. В химической литературе его обычно выражают с помощью представления об энтропии. Чтобы прийти к такой, формулировке, рассмотрим изолированную систему, т.е. систему, которая не обменивается с окружающей средой ни энергией, ни веществом. Если в такой изолированной системе происходит какой-либо самопроизвольный процесс, система всегда переходит в более неупорядоченное состояние. Например, при расширении газа в установке, изображенной на рис. 3.1., система не обменивается с окружающей средой ни теплотой, ни работой, ни веществом; следовательно, она является изолированной. Самопроизвольному расширению этой системы (газа) соответствует повышение энтропии.
В реальном мире редко приходится иметь дело с изолированными системами. Обычно мы имеем дело с системами, которые обмениваются со своим окружением энергией в форме теплоты или работы. Если в такой системе происходит самопроизвольный процесс, он может сопровождаться повышением или уменьшением энтропии. Однако второй закон термодинамики утверждает, что Вселенная в целом должна повышать свою энтропию при любом самопроизвольном процессе. В качестве примера рассмотрим окисление железа в Fe2O3 (тв.):
4Fe (тв.) + 3О2 (г.) → 2Fe2O3 (тв.) (3.5)
Как
было показано в упражнении 3.1, этот
химический процесс приводит к уменьшению
хаотичности, т.е.
![]() для него является отрицательной
величиной. Но при протекании этого
процесса в окружающей среде тоже
происходят определенные изменения.
Например, поскольку реакция образования
оксида экзотермична, выделяющаяся
теплота поглощается окружающей средой.
В действительности изменения, происходящие
в окружающей среде, вызывают повышение
ее энтропии, которое больше понижения
энтропии в самой системе. Для любого
самопроизвольного процесса сумма
изменений энтропии системы и окружения
(эта сумма есть изменение энтропии
Вселенной в результате данного процесса)
должна быть положительной:
для него является отрицательной
величиной. Но при протекании этого
процесса в окружающей среде тоже
происходят определенные изменения.
Например, поскольку реакция образования
оксида экзотермична, выделяющаяся
теплота поглощается окружающей средой.
В действительности изменения, происходящие
в окружающей среде, вызывают повышение
ее энтропии, которое больше понижения
энтропии в самой системе. Для любого
самопроизвольного процесса сумма
изменений энтропии системы и окружения
(эта сумма есть изменение энтропии
Вселенной в результате данного процесса)
должна быть положительной:
![]() (3.6)
(3.6)
Ни один процесс, приводящий к возрастанию упорядоченности (уменьшению энтропии) в системе, не может происходить без поступления энергии к системе от ее окружения. Более того, хаотичность, вносимая в окружение системы, всегда превосходит достигаемую в системе упорядоченность. Таким образом, наряду с сохранением энергии (первый закон термодинамики) в природе всегда происходит повышение энтропии (второй закон).