
- •ШЕСТИЧЛЕННЫЕ
- •Способы получения
- ••2). Синтезы пиридина на основе более простых реагентов:
- •Физические свойства
- ••Строение
- ••НЭП атома азота находится вне сопряженной системы и занимает гибридную sp2 –орбиталь, ориентированную
- ••Резонансные структуры, иллюстрирующие ароматическую делокализацию π-электронов в молекуле пиридина :
- ••В большей части этих структур атом азота имеет отрицательный заряд, что соответствует его
- ••пиридин
- •Химические свойства
- ••Пиридин более сильное основание, чем анилин.
- ••Пиридин легко образует соли с HBr, HCl, H2SO4 и др. кислотами.
- ••Однако основность пиридина значительно ниже, чем у жирных аминов Alk→NH2.
- ••Благодаря эл-ой паре N пиридин проявляет нуклеофильные в-ва. Так, пиридин легко алкилируется с
- ••Соли при нагревании перегруппировываются в гомологи пиридина.
- ••Нуклеофильные свойства пиридина подтверждаются и легкостью образования N-ацилпиридиниевых солей.
- ••П с SO3 образует комплекс С6H5N∙SO3, используемый для сульфирования ацидофобных соединений. Это мягкий
- •2. Электрофильное ароматическое замещение
- ••Это обусловлено двумя причинами:
- ••Пиридин по cв-вам напоминает нитробензол.
- •• Атака в положение 2:
- •• Атака в положение 3:
- •N пиридин
- •3. Реакции нуклеофильного замещения
- •• Классическим примером такой реакции является
- •NaNH2
- •4.Окисление
- •• SЕ-реакции у пиридин-N-оксида
- •Обработкой продукта р-ции PCl3 удаляют кислород.
- •5.Восстановление
- •Производные пиридина
- ••2- и 4 -гидрокси- и аминопиридины резко отличаются от 3-производных по cв-вам.
- ••Это можно объяснить таутомерным превращением.
- ••Анологично и у аминопроизводных.
- ••α- и γ-аминопиридины не диазотируютя,
- •• Пиридинкарбоновые кислоты:
- ••Никотиновая к-та – широко распространена в природе – сод-ся в печени, экстракте дрожжей,
- ••Никотин 3-[2-(N-метилпирролидил)]-пиридин содержится в листьях и корнях табака. Это

• SЕ-реакции у пиридин-N-оксида
идут легче, чем у П, преимущественно в положения
2 и 4
NO2
|
HNO3, H2SO4 |
|
N |
90 oC |
N |
O |
|
O |
пиридин- |
4-нитропиридин- |
|
N-оксид |
N-оксид (90 %) |
|
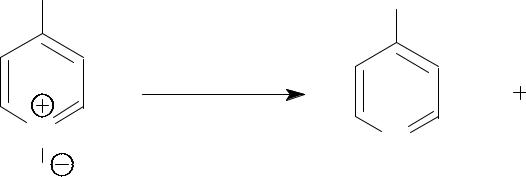
Обработкой продукта р-ции PCl3 удаляют кислород.
NO2 |
NO |
|
2 |
PCl3, to |
|
N |
POCl3 |
N |
|
O |
4-нитропиридин |
4-нитропиридин- |
|
N-оксид

5.Восстановление
•Пиридин восстанавливается легче, чем бензол. Восстановление проходит гладко не только как гидрирование в присутствии Pt-катализатора, но и при действии натрия
вабсолютном спирте.
H2
Pt 
N |
|
Na |
NH |
|
|
пиперидин |
|||
пиридин |
C2H5OH |
|||
|
||||
Производные пиридина
•2- и 4-гидроксипиридины легко получаются при обработке
2- и 4-аминопиридинов нитритом натрия в присутствии минеральных кислот
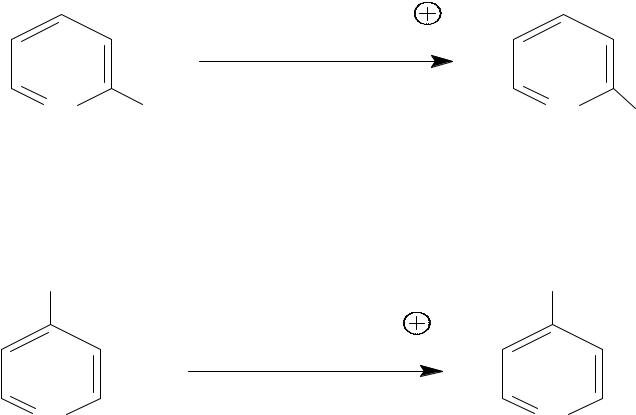
|
NaNO2 |
, H |
|
|
N |
H2O |
N |
OH |
|
NH2 |
|
|||
2-ам ин о п иридин |
|
|
|
|
|
2-гидро ксип иридин |
|||
NH2 |
|
|
OH |
|
|
NaNO2 , H |
|
|
|
N |
H2O |
|
N |
|
4-ам ин о п иридин
4-гидро ксип иридин
•2- и 4 -гидрокси- и аминопиридины резко отличаются от 3-производных по cв-вам.
•3-гидроксипроизводные подобно
фенолам дают с FeCl3 окрашивание, обладают слабокислыми cв-вами.
•2- и 4-гидроксипроизводные этих св-в не обнаруживают.

•Это можно объяснить таутомерным превращением.
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
|
OH |
|
|
|
N |
|
O |
|||
|
|
|
|
|
|||||||||
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|||||||
2-гидро кси- |
|
|
|
H |
|
|
|||||||
2-п иридо н |
|||||||||||||
п иридин |
|
|
|
|
|
|
|
|
|||||
Положение таутомерного равновесия сильно зависит от природы радикалов, входящих в пиридиновое кольцо.
•Анологично и у аминопроизводных.
β-аминопиридины подобно первичным ароматическим аминам диазотируются – образующиеся соли диазония вступают во все превращения, характерные для арилдиазониев;
•если две NH2-гр. в обоих β-положениях, соль с кислотами образуется по обеим гр.

•α- и γ-аминопиридины не диазотируютя,
соли дают только по одной NH2-гр., если их две.
•α- и γ -Аминопиридины также способны к таутомерным превращениям.
|
|
|
|
|
|
|
|
|
|
|
N |
|
NH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
N |
|
NH2 |
|
|
|
|
|||||||
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
||||||
àì èí î -ô î ðì à |
|
|
|
|
H |
|
|
|||||||
|
èì èí î -ô î ðì à |
|||||||||||||
|
|
|
|
|
|
|
|
|||||||
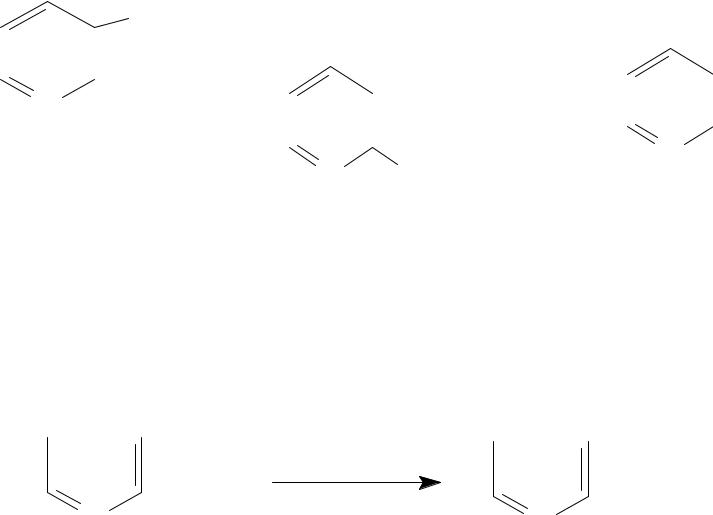
• Пиридинкарбоновые кислоты:
|
|
|
|
COOH |
|
COOH |
|||||||
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
N |
|
||||
í èêî òèí î âàÿ |
|
|
|
|
|
|
|||||||
|
|
|
|
||||||||||
|
N COOH |
||||||||||||
|
|
|
|
|
|
èçî í èêî òèí î âàÿ |
|||||||
|
|
|
|
|
ï èêî ëèí î âàÿ |
|
|
|
|
|
|||
Получают окислением гомологов пиридина (пиколинов):
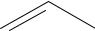
 CH3 KMnO4
CH3 KMnO4 
 COOH
COOH
N |
H2SO4 |
N |
