
Литература / учебное пособие
.pdf
чевую роль в ряде жизненно важных процессов. К их числу прежде всего следует отнести гликолиз, который начинается с реакции фосфорилирования глюкозы с помощию аденозинтрифосфоной кислоты в присутствии фермента глюкокиназы.
Моносахаридам присущи реакции восстановления, в ходе которых образуются многоатомные спирты, называемые альдитами:
|
C |
O |
|
|
|
|
|
CH2OH |
|
|||
|
|
H |
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
||||||
H |
|
|
OH |
|
|
H |
|
|
OH |
|
||
H |
|
|
|
H |
O + H2, Ni |
H |
|
|
|
H |
O |
|
|
|
|
|
|
|
|||||||
H |
|
|
OH |
|
|
H |
|
|
OH |
|
||
|
|
|
|
|
||||||||
H |
|
|
OH |
|
|
H |
|
|
OH |
|
||
|
|
|
|
H2OH |
|
|
|
|
|
|
||
|
C |
|
|
CH2OH |
|
|||||||
D |
|
|
-глюкоза |
|
|
|
|
|
D-сорбит |
|||
Некоторые из них известны в качестве заменителя сахара (ксилит, сорбит). Окисление моносахаридов является важной реакцией в химии углеводов.
Его используют для получения ряда соединений в структурных исследованиях и биохимических анализах. В зависимости от условий окисления моносахаридов образуются различные продукты. В щелочной среде окисление сопровождается разрушением углеродной цепи молекулы (реакция ”серебряного зеркала”). Окисление в нейтральной среде позволяет сохранить углеродный скелет. Под действием мягких окислителей окисляется только карбонильная группа. С помощью сильного окислителя концевые группы в случае альдоз одновременно окисляются в карбоксильные группы:
|
|
|
|
|
|
|
|
|
|
|
COOH |
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
H |
|
|
OH |
глюконовая |
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
C |
O |
|
[O], Br2 + H2O H |
|
|
H |
|
|
O |
|
||||||||
|
|
H |
|
|
|
|
|
H |
|
|
OH |
|
|
кислота |
|||||
|
H |
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
H |
|
|
OH |
|
|
|
|
|
|||
H |
|
|
|
H |
O |
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
CH2OH |
|
|
|
|
|
||||||
|
H |
|
|
OH |
|
|
|
|
|
|
COOH |
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
H |
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
[O], HNO3 (разб.) |
|
|
|
H |
|
|
|
OH |
|
||||
|
|
|
|
H2OH |
|
|
|
|
|
|
|
|
|
|
|||||
|
C |
|
|
|
|
|
|
H |
|
|
|
H |
O |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
глюкаровая |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
D-глюкоза |
|
|
|
|
|
|
|
|
|
H |
|
|
|
OH |
кислота |
||||
|
|
|
|
|
|
|
|
|
H |
|
|
|
OH |
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
COOH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
32

|
Аналогично альдегидам и кетонам моносахариды вступают в реакции |
нук |
леофильного присоединения с гидроксиламином, фенилгидразином, а также |
ссинильной кислотой.
4.3. Олигосахариды
Олигосахариды классифицируют:
а ) в зависимости от числа моносахаридных фрагментов, входящих в олигосахарид (дисахариды, трисахариды, тетрасахариды и т. д.);
б) по составу моносахаридных остатков (гомоолигосахариды, гетероолигосаха-
рид ы);
в) в зависимости от порядка соединения мономеров (линейные, разветвленные);
г) на восстанавливающие и невосстанавливающие.
Из олигосахаридов в природе наиболее широко распространены дисаха-
рид ы.
Увосстанавливающих дисахаридов связь между моносахаридными ос-
татками осуществляется за счет спиртового и полуацетального гидроксилов. П ри этом один из моносахаридных остатков сохраняет свободный полуаце-
тальный гидроксил, который определяет восстанавливающие свойства и реакции , свойственные моносахаридам.
Уневосстанавливающих дисахаридов гликозидная связь образована за
счет полуацетальных гидроксилов обоих моносахаридов. Они не содержат сво-
бодного полуацетального гидроксила и не вступают в реакции, характерные для
карбонильной группы.
Квосстанавливающим дисахаридам относятся мальтоза, целлобиоза, лак-
тоза и др.
Мальтоза (солодовый сахар) является продуктом распада крахмала под
действием фермента β-амилазы, выделяемого слюнной железой. В мальтозе ос-
татки двух молекул D-глюкопиранозы связаны α(1→4)-гликозидной связью.
|
6CH2OH |
|
|
|
|
|
|
|
6CH2OH |
|
|
|
||||
H 5 |
|
|
O |
H |
|
H 5 |
|
|
O OH |
|||||||
|
|
|||||||||||||||
4 |
H |
|
|
|
1 |
|
4 |
H |
|
|
1 |
|||||
|
|
H |
|
|
|
|
|
O |
|
|
H |
|
|
|
||
|
H 3 |
|
|
2 |
|
|
|
H 3 |
|
|
|
|||||
|
|
|
H |
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|||||||||
|
O |
|
|
|
|
OH |
||||||||||
мальтоза (a-D-глюкопиранозил-(1 Æ 4)-b-D-глюкопираноза)
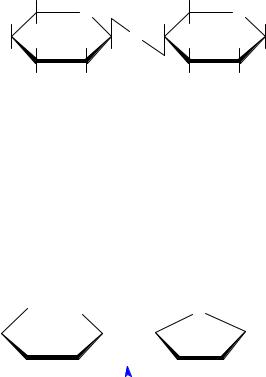
Целлобиоза образуется при неполном гидролизе полисахарида целлюло-
з |
ы. Она также построена из двух молекул глюкозы, но отличается |
т |
ем, что в одной из молекул, образующих димер, в реакцию вступ |
т |
альный гидроксил β-пиранозной формы. Таким образом, в целлоб |
д |
вух молекул D- глюкопиранозы связаны β(1→4)-гликозидной связ |
33
|
6CH2OH |
|
6CH2OH |
|
|
H |
5 |
O |
H |
5 |
O OH |
4 |
H |
1 O |
4 |
H |
|
|
H |
|
|
H |
|
|
H3 |
2 |
|
3 |
2 |
|
OH |
|
H |
OH |
|
целлобиоза (b-D-глюкопиранозил-(1 Æ 4)-b-D-глюкопираноза)
Ворганизме человека мальтоза расщепляется ферментом α-глюкозидазой
( |
мальтазой), а целлобиоза - β-глюкозидазой, который в организме ч |
с |
утствует. |
Наиболее распространенным невосстанавливающим дисахаридом являет-
с |
я |
сахароза. |
Она |
построена |
из остатков D-глюкопиранозы и |
|||||||||||||||
ф |
уранозы: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
CH2OH |
O |
|
|
|
|
|
|
C |
O |
|
H2 |
||||||
|
H |
|
|
|
H HO |
|
|
|||||||||||||
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
||||||||||||||
|
|
|
HH |
|
|
|
1 |
O |
2 |
|
|
|
|
|
|
|
H2OH |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
O |
|
H |
|
|
|
O |
HH |
|
|
|
||||||
|
|
|
( |
|
|
|
|
|
|
|
|
|
|
|
1®2)-гликозидная связь |
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
са |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
хароза (a-D-глюкопиранозил |
|
|
В |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
отличие от больши |
|
пол |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
уацетального ги |
м |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
и свойствами. |
4. |
4. Полисахариды |
П |
олисахариды предст |
х |
аридов, котор |
з |
ом, по химич |
В |
полисахарид |
( |
1→4)- и (1→ |
а |
льного проис |
с |
вязи. |
Г |
ликозидная природ |
г |
идролизу в ки |
х |
аридов и их п |
ч |
исле дисахари |
ч |
ивостью и не |
П |
олисахариды различ |
ным |
и особенностями |
34
носахарид, входящий в состав полимерной молекулы, может находиться в пиранозной или фуранозной форме.
С точки зрения общих принципов строения, полисахариды делят на гомополисахариды, которые состоят из остатков одного моносахарида и гетерополисахариды, которые состоят их остатков различных моносахаридов. К гомополисахаридам относятся многие полисахариды растительного (крахмал, целлюлоза) и животного происхождения (гликоген, хитин). Гетерополисахариды изучены менее подробно. Однако известно, что они играют важную роль в живых организмах и функционируют при этом в комплексах с белками.
Крахмал (резервный гомополисахарид растений) представляет собой белое аморфное вещество, нерастворимое в холодной воде. При быстром нагревании крахмала за счет содержания в нем влаги происходит гидролитическое расщепление полимерной цепи на более мелкие осколки, называемые декстринами. Декстрины растворяются в воде лучше, чем крахмал.
Крахмал представляет собой смесь двух полимеров, построенных из D-глюкопиранозных остатков – амилозы (10-20%) и амилопектина (80-90%).
В амилозе D-глюкопиранозные остатки связаны α-(1→4)-гликозидными связями, т.е. дисахаридным фрагментом амилозы является мальтоза. Цепь амилозы неразветвленная. Она включает 200-1000 глюкозидных остатков. Макромолекула амилозы свернута в спираль. При этом на каждый виток спирали приходится шесть моносахаридных звеньев.
CH2OH |
O |
|
|
CH2OH |
O H |
CH2OH |
O |
|
|
CH2OH |
O H |
H |
H |
H |
HH |
H |
H |
H |
HH |
||||
HH |
|
1 |
4 |
|
HH |
|
|
O |
H |
||
|
|
O |
|
|
|
O |
|
|
|
||
H |
O |
H |
|
H |
O H |
H |
O |
|
H |
H |
OH |
a(1®4)-гликозидная связь
амилоза
Амилопектин отличается от амилозы высокоразветвленным строением. В линейных участках этого полисахарида D-глюкопиранозные остатки связаны α-(1→4)-гликозидными связями, а в точках разветвления имеются дополнительные α-(1→6)-гликозидные связи. Между точками разветвления располагаются 20-25 остатков глюкозы.
Гликоген (резервный гомополисахарид животных организмов) является структурным и функциональным аналогом крахмала. По строению подобен амилопектину, но отличается от него большей разветвленностью и более жесткой упаковкой молекулы. Сильное разветвление способствует выполнению гликогеном энергетической функции, поскольку при наличии большого числа концевых остатков обеспечивается быстрое отщепление нужного количества глюкозы.
35
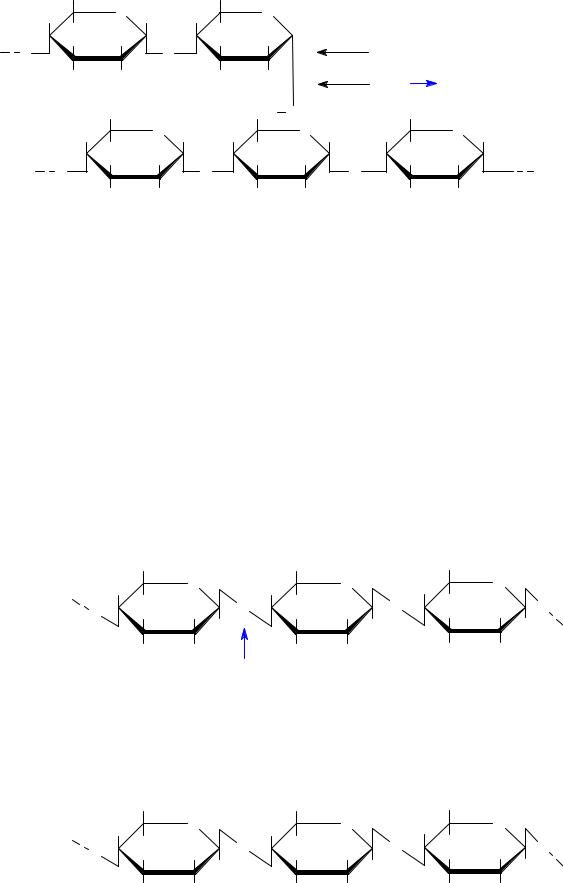
CH2OH |
O H |
|
|
CH2OH |
O |
|
|
|
|
||
H |
|
|
H |
H |
|
|
|
|
|
||
H |
|
|
|
|
H |
|
|
|
|
|
|
H |
|
|
O |
|
|
|
|
разветвление |
|||
O |
|
|
|
|
|
|
|
||||
H |
|
O |
H |
|
H |
|
OH |
|
a(1 |
6)-гликозидная связь |
|
|
CH2OH |
|
|
|
CH2 O |
|
CH2OH |
|
|||
H |
H |
|
O |
H |
|
H |
O |
H |
H |
O |
H |
|
H |
|
|
|
H |
|
|
H |
|
|
|
|
|
|
O |
|
H |
O |
H |
|
|
||
|
|
|
|
|
|
|
|
|
|
||
|
H |
|
O |
H |
|
H |
O |
H |
H |
O |
H |
|
|
|
|
|
|
|
а |
|
|
|
мило |
Ц
ный
к
з
це
г
м
це
у
рим
д
ный
не
|
CH2OH |
|
CH2OH |
|
|
CH2OH |
O |
|
|
H |
O |
H |
|
O |
|
H |
|
O |
H |
H |
O |
H |
|
O |
H |
O |
|
|
H |
|
|
H |
|
||
|
H |
OH |
|
H |
OH |
|
H |
OH |
b(1®4)-гликозидная связь
целлюлоза
Хитин является структурным гомополисахаридом наружного скелета членистоногих и некоторых других беспозвоночных животных, а также клеточных мембран грибов.
|
CH2OH |
|
|
CH2OH |
CH2OH |
O |
||
|
H |
O |
H |
|
|
O |
H |
|
O |
H |
O |
|
H |
H |
O |
H |
O |
H |
|
|
|
|
H |
|
||
|
H |
NHCOCH3 |
|
H |
|
NHCOCH3 |
H |
NHCOCH3 |
х
36

Хитин построен из остатков N-ацетил D-глюкозамина, связанных между
собой α-(1→4)-гликозидными связями. Макромолекула хитина не имеет раз-
ветвлений, а его пространственная упаковка подобна целлюлозе.
|
5. НУКЛЕОТИДЫ И НУКЛЕИНОВЫЕ КИСЛОТЫ |
|
Нуклеиновые кислоты впервые были выделены во второй половине XIX в. |
из |
клеток различных органов (печени, селезенки, щитовидной железы и др.). |
Название этих соединений (от лат. nucleus - ядро) отражает их высокую кон-
це |
нтрацию в ядрах растительных и животных клеток. |
|
Нуклеиновые кислоты играют ключевую роль в передаче наследственных |
приз |
наков (генетической информации) и управлении процессом биоситеза белка. |
|
Нуклеиновые кислоты представляют собой соединения, молекулярная |
масса которых варьирует в пределах от 25 тыс. до 1 млн и более.
|
|
|
|
|
|
|
|
|
|
|
|
|
|
5.1. Нуклеозиды и нуклеотиды |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
Нуклеозиды являются простейшими структурными компонентами нук- |
|||||||||||||||||||||||||||||||||||||||||||||||||
ле |
иновых кислот. Их молекулы состоят из азотистого основания (аденин, гуа- |
|||||||||||||||||||||||||||||||||||||||||||||||||
нин , тимин, урацил, цитозин) и углевода (рибозы или дезоксирибозы). |
||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
NH2 |
7 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
7 |
|
|
|
|||||||||||||
|
|
|
|
|
|
|
6 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|
6 |
|
|
|
|
5 |
|
|
|
|||||||||||||
|
|
|
1 |
|
|
|
|
5 |
N |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
|
|
||||||||||||||||||||||
|
|
|
N |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
HN |
|
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
8 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
8 |
|
||||||||||
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
NH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
N 4 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H2N |
N 4 NH |
|
|
||||||||||||||||||||||||||
|
|
|
|
|
|
|
3 |
|
|
9 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3 |
|
|
9 |
|
|
|
|
|
||||||||||
|
|
|
|
|
|
аденин (А) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
гуанин (Г) |
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
NH2 |
|
|
|
|
|
|
|
|
H |
|
|
O |
|
|
|
|
|
|
|
|
H |
|
|
O |
CH |
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
4 |
|
|
|
|
|
|
|
|
|
3 |
|
|
|
|
4 |
|
|
||||||||
|
3 |
|
4 |
|
|
|
|
|
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
|
|
|
|
3 |
|||||||||||||||||||||||
|
N |
|
|
|
|
|
|
5 |
|
|
|
|
|
|
|
|
|
N |
|
|
|
|
|
|
5 |
|
|
|
|
|
|
|
|
|
|
|
N |
|
|
|
|
|
|
5 |
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
6 |
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
6 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
6 |
|
||||||
|
O N1 |
|
|
|
|
|
|
|
|
|
|
O N 1 |
|
|
|
|
|
|
O N1 |
|
||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|||||||||||||
|
цитозин (Ц) |
|
|
|
|
|
|
|
урацил (У) |
|
|
|
|
|
тимин (Т) |
|
|
|||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
1' |
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C |
|
H |
|
|
|
|
|
|
HO 5'C O OHH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H2' |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H3' |
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
4 |
|
|
1' |
|
|
|
|
|
|
|
|
|
|
|
|
|
' |
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H4' |
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
3' |
2' |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
5' |
|
CH2OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
р |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ибоза |
||
37
1' |
|
|
O |
|
|
|
|
|
|
|
|
|
||
|
C |
|
H |
5' |
|
|
|
|
|
|||||
|
H2' |
|
|
|
|
|
||||||||
|
|
|
|
H |
|
|
HO C O |
OHH2 |
|
|||||
|
H3' |
|
|
|
OH |
|
|
|
4 |
|
3' |
|
1' |
' |
|
|
|
|
|||||||||||
|
H4' |
|
|
|
OH |
|
|
|
2'H |
|
||||
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
OH |
|
||||||||
|
5' |
|
CH2OH |
д |
|
|
|
|||||||
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
||||||
А
з
1
в
б
|
|
|
|
|
азотистое основание |
|
||
|
|
5' |
O |
BH2 |
|
|
|
|
|
|
HO C |
N-гликозидная связь |
|
||||
|
|
4 |
|
1' |
|
|||
|
|
|
|
' |
|
|
||
|
|
|
3' |
2' |
|
|
|
|
|
|
|
OH |
R |
|
|
|
|
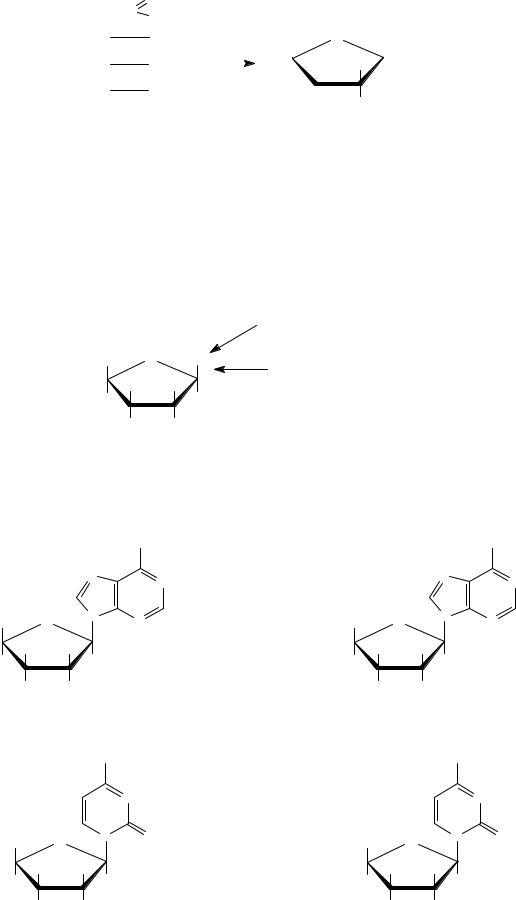
R = OH - рибонуклеозид |
|
|
|
|
||||
R = H - дезоксирибонуклеозид |
|
|
|
|||||
|
|
|
|
общая формула нуклеозидов |
|
|
||
|
|
|
NH2 |
|
|
|
NH2 |
|
|
|
N |
|
N |
|
|
N |
N |
HO C O |
|
N |
N |
|
|
HO C O |
N |
N |
|
H2 |
|
|
H2 |
||||
OH |
OH |
|
|
|
OH |
H |
|
|
аденозин |
|
|
|
дезоксиаденозин |
|
|||
|
|
NH2 |
|
|
|
NH2 |
|
|
|
|
|
N |
|
|
|
N |
|
H |
O |
N |
O |
|
O |
H |
N |
O |
C |
H2 |
|
|
|
CH2 |
|
|
|
OH |
|
OH |
|
|
|
OH |
H |
|
цитидин |
|
|
|
дезоксицитидин |
|
|||
езокс
OO
38

Нуклеозиды достаточно устойчивы к гидролизу в слабощелочной среде.
Вкислой среде они подвергаются гидролизу. При этом пуриновые нуклеозиды
гидролизуются легче, чем пиримидиновые.
Вотличие от нуклеозидов нуклеотиды при гидролизе распадаются не
только на азотистое основание и углевод, но и на фосфорную кислоту. Поэто-
му, нуклеотидами называют фосфаты нуклеозидов. Реакция этерификации ме-
жд |
у фосфорной кислотой и нуклеозидом обычно осуществляется при С-5 или |
С-3 атоме в остатке рибозы (рибонуклеотиды) или дезоксирибозы (дезоксири-
бонуклеотиды):
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NH2 |
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NH2 |
|
|
|
|
N |
|
|
N |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
|
|
N |
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
|
|
|
|||||||||
|
|
O |
|
|
|
|
|
|
|
|
|
HO C |
O |
N |
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
H2 |
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
C O |
|
N |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
N |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
O |
|
|
P HO |
|
|
|
H2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
OH |
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
OH |
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
P |
|
|
OH |
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
аденозин-5’-фосфат |
|
|
аденозин-3’-фосфат |
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
5.2. Первичная структура нуклеиновых кислот |
|
|
|
||||||||||||||||||
|
|
|
|
По своей химической структуре нуклеиновые кислоты являются полиме- |
|||||||||||||||||||||||||||
ра |
|
|
|
|
|
|
|
|
ми, мономерными звеньями которых служат нуклеотиды. В полинуклеотид |
||||||||||||||||||||||
ны |
|
|
|
|
|
|
|
х цепях нуклеотидные звенья связаны через фосфатную группу, которая об- |
|||||||||||||||||||||||
ра |
|
|
|
|
|
|
|
|
зует две сложноэфирные связи с С-3’ предыдущего и с С-5’ последующег |
||||||||||||||||||||||
нук |
|
|
|
|
|
|
леотидных звеньев. В основе цепи лежат чередующиеся углеводные и фос- |
||||||||||||||||||||||||
фатные остатки, а азотистые основания являются “боковыми” фрагментам
прис |
оединенными к углеводным остаткам. |
|
Так возникает одноцепочная молекула нуклеиновой кислоты. При этом |
пос |
тоянная и строго специфичная последовательность нуклеотидов, состав- |
ля |
ющих полинуклеотидную цепь, называется первичной структурой нуклеино |
вых кислот.
Различают рибонуклеиновую (РНК) и дезоксирибонуклеиновую кислоты
( ДНК). В их химическом составе есть некоторые различия (таблица 4). ДНК в основном содержится в ядрах клеток, а РНК находится в рибо-
с омах и в протоплазме клеток. При этом молекулы РНК различаются по
функциям (транспортная, матричная, рибосомная).
39

O
CH3
HN
O |
N |
|
C O |
H2 |
NH2 |
|
H N
N
OH(OH) O
 N
N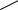
PHO C |
OO |
|
H2 |
|
|
NH2 |
O |
|
H |
|
|
N |
N |
|
|
|
|
|
||
|
O |
H(OH) |
|
N |
N |
|
|
|
|
|
|||
OH |
P O |
|
C |
O |
H2 |
|
|
O |
|
|
|
|
|
|
|
|
O |
|
H(OH) |
|
|
|
H |
P |
|
O |
|
|
|
|
O |
|
|
|
Фрагмент цепи молекулы ДНК (РНК)
|
|
Таблица 4 |
С |
ходство и различие в химическом составе нуклеинов |
|
ДНК |
|
РНК |
|
Азотистое основание |
|
А |
денин |
Аденин |
Г |
уанин |
Гуанин |
Ц |
итозин |
Цитозин |
Т |
имин |
Урацил |
|
Углеводный компонент |
|
Д |
езоксирибоза |
Рибоза |
5.3. Вторичная структура ДНК |
||
У |
животных и человека молекула ДНК в отличие |
|
с |
ложную пространственную организацию по |
|
це |
почную правозакрученную спираль, состоящ |
|
д |
ругу |
антипараллельных полинуклеотидных |
с |
труктуре ДНК. В ней пуриновые и пирим |
|
40
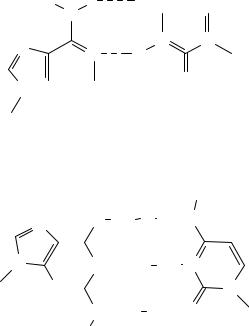
внутрь двойной спирали, а углеводно–фосфатные группы расположены снаружи спирали. Азотистые основания аденин и тимин, гуанин и цитозин, принадлежащие двум цепям, соединяются за счёт водородных связей и образуют комплементарные пары оснований:
CH3
HN H O

N N H N N |
в цепь |
N N
N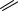 O
O
тимин
в цепь
аденин
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
N |
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
H |
|
|
N |
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
N |
|
|
|
|
|
N |
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
N |
N |
|||
N |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
в цепь |
|
|
|
N |
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
O |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
в цепь |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
гуанин |
|
|
|
|
|
|
|
|
|
цитозин |
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
О |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
снова |
к |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ф |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
5. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
4. Третичная структур |
У |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
всех |
в |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
прок |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ар |
д |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
м |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
проце |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
сса |
в |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
с |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
б |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
с
т
Д
41
