
- •Различают 4 вида субстратной специфичности ферментов:
- •Применение ферментов в качестве лекарственных препаратов
- •Окислительное декарбоксилирование пировиноградной кислоты: суммарное уравнение, строение и регуляция пируватдегидрогеназного комплексeа, связь с цпэ, биологическое значение.
- •Цикл трикарбоновых кислот (цитратный цикл): последовательность реакций, связь с цпэ, регуляция, биологическая роль.
- •Энергетическая
- •Теория Митчелла. Условия синтеза атф. Коэффициент фосфорилирования р/о.
- •Анаэробный гликолиз: схема процесса, энергетический эффект, и биологическое значение.
- •Лактатный цикл. Биологическое значение.
- •Глюконеогенез из аминокислот и глицерина. (схема процесса). Глюкозо- аланиновый цикл. Биологическое значение.
- •Синтез пуриновых нуклеотидов: схема, ферменты, регуляция, запасные пути синтеза.
- •Нарушения обмена пуриновых нуклеотидов: гиперурикемия, синтдром Леша-Нихана. Биохимические основы лечения подагры.
- •Биосинтез пиримидиновых нуклеодитов: схема, ферменты, регуляция, нарушения.
- •Нарушение обмена пиримидиновых нуклеотидов
- •Наследственная форма
- •Приобретенная форма
- •Распад пиримидиновых нуклеотидов: схема, ферменты.
- •Аденилатциклазная система передачи сигналов в клетки, роль g-белков в механизме трансдукции сигнала, вторичные посредники.
- •Либерины, статины, тропные гормоны гипофиза.
- •Адреналин: строение, синтез, регуляция секреции, ткани-мишени, механизм передачи сигнала, влияние на метаболизм в тканях-мишенях.
- •Мишени и эффекты
- •Ну или проще
- •80. Обмен железа: всасывание, транспорт, депонирование, регуляция, Роль железа в организме. Нарушения обмена железа в организме человека.
- •Существуют три способа перемещения железа из просвета кишечника в энтероциты:
- •Регуляция
- •Роль железа в организме:
- •Избыток железа
- •Железодефицит
- •Противосвертывающие системы крови: антитромбиновая и фибринолитическая.
- •Функции протеина s (ps):
- •Механизмы обезвреживания токсических веществ в печени: микросомальное окисление, реакции конъюгации
- •Nadph-зависимая монооксигеназная система
- •Nadh-зависимая монооксигеназная система
- •Распад гема, образование и обезвреживание билирубина. «Прямой» и
- •Биохимические изменения при нарушении обмена билирубина
- •Референтные величины концентрации общего билирубина в
- •Гемолитическая (надпеченочная) желтуха
- •Паренхиматозная (печёночная) желтуха.
- •Лабораторная диагностика
- •Механическая или обтурационная (подпеченочная) желтух.
- •Диагностическое значение определения билирубина и других желчных пигментов в крови и моче.
- •Эластин.
- •Свойства:
- •Возвращается в первоначальное состояние после снятия нагрузки.
- •Структурные и регуляторные белки мышц и их роль в мышечном сокращении
- •Функции субъединиц тропонина
- •Толстые нити образованы белком миозином
- •– Й этап.
- •На этой стадии атф не расщепляется, т.Е. Служит не источником энергии, а аллостерически изменяет конформацию миозиновой головки и тем самым ослабляет связь миозина с актином
- •Мышечное расслабление
- •Сокращение гладких мышц
- •Стадия – стадия начальных изменений
- •Стадия – стадия поздних изменений
- •Усилением:
- •Ослаблением:
Механизмы обезвреживания токсических веществ в печени: микросомальное окисление, реакции конъюгации
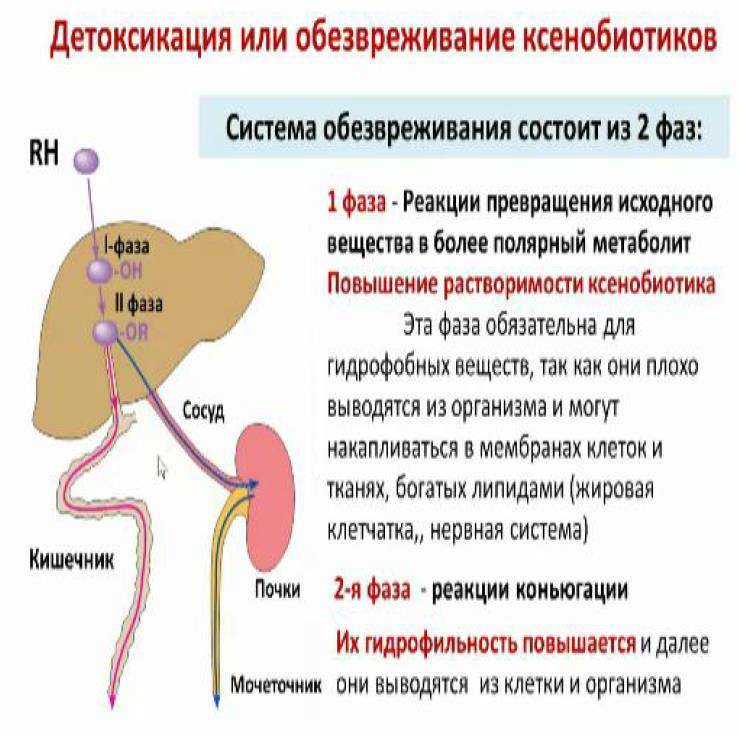
Большинство ксенобиотиков обезвреживаются путём гидроксилирования в результате микросомального окисления:
 RH ROH
RH ROH
В мембранах эндоплазматического ретикулума (ЭР) практически всех тканей локализована система микросомального (монооксигеназного) окисления), отвечающая за течение первой фазы обезвреживания.
Микросомальная система включает несколько белков, составляющих электронтранспортные цепи (ЦПЭ). В ЭР существуют две такие цепи:
первая NADPH-зависимая
вторая NADH-зависимая
Nadph-зависимая монооксигеназная система
Состоит из двух ферментов - NADPH-Р450 редуктазы и цитохрома Р450;
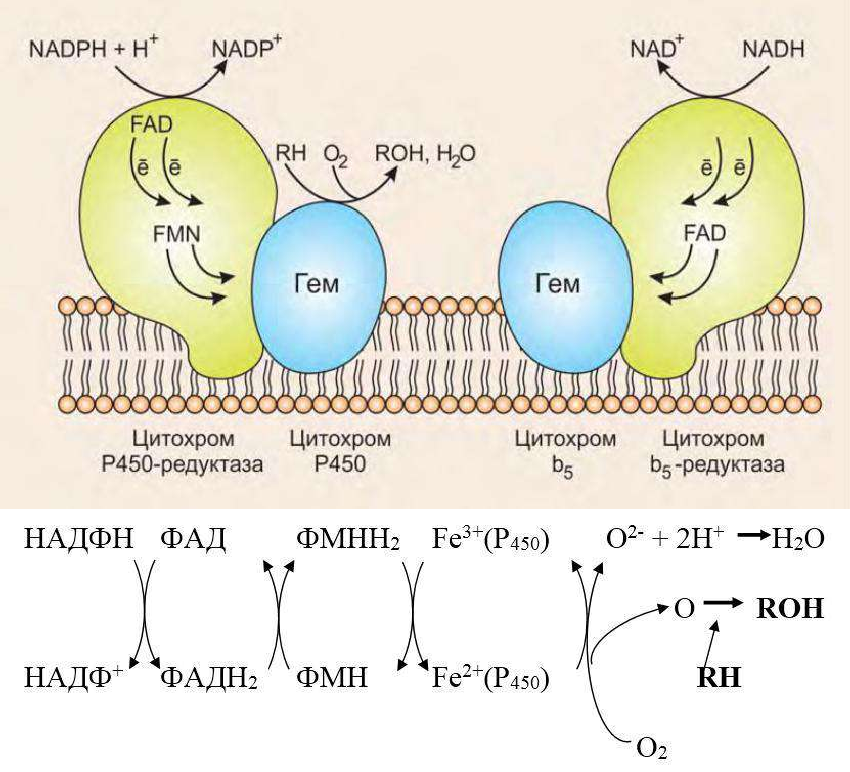
Цитохром Р450 передает 2ё на 1 атом молекулы О2, который превращается в О2-
При взаимодействии О2- с 2 протонами образуется вода (О2-+ 2Н+→ Н2О). Второй атом кислорода включается в гидроксильную группу вещества RH, образуя R-OH.
Nadh-зависимая монооксигеназная система
Включает фермент NADH-цитохром-b5редуктазу, цитохром b5 и фермент - стеароил-КоА-десатуразу.
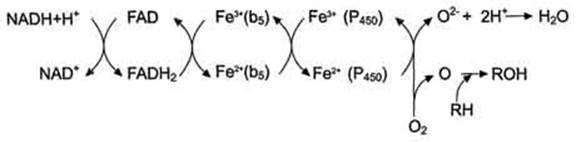
Окисление NADH происходит цитохром-b5-редуктазой, а далее электроны идут на цитохром b5, который далее передаёт электроны на ферменты (цитохром Р450, стеароил-КоА-десатуразу). Стеароил-КоА-десатураза
передает электроны на 1 атом кислорода, образуя воду при участии протонов. Второй атом кислорода включается в стеариновую кислоту.
Суммарное уравнение реакции гидроксилирования вещества RH ферментами микросомального окисления:
RH + O2 + NADPH + H+ → ROH + H2O + NADP+.

2-ая фаза – реакции конъюгации
Гидроксилирование позволяет перейти процессу обезвреживания ко второй фазе – реакции конъюгации, в ходе которой к созданной функциональной группе будут присоединяться другие молекулы эндогенного происхождения
– глюкуроновая кислота, глицин, глутатион, серная кислота и др. Образованный конъюгат удаляется из организма

Распад гема, образование и обезвреживание билирубина. «Прямой» и
«непрямой» билирубин.
Эритроциты живут 90-120 дней, после чего разрушаются. В крови высвобождаемый гемоглобин образует комплекс с белком-переносчиком гаптоглобином и переносится в клетки ретикуло-эндотелиальной системы (РЭС): селезенки, костного мозга, печени, где происходит его катаболизм.

реакция протекает при участии НАФДН-зависимого комплекса – гемоксигеназы, локализован этот комплекс в мембране эндоплазматического ретикулума рядом с цепью микросомального окисления.
Гем индуцирует транскрипцию гена гемоксигеназы, абсолютно специфичной по отношению к гему.
Билирубин – основной желчный пигмент–красно-желтого цвета. Билирубин образуется не только при распаде гемоглобина, но также при катаболизме других гемсодержащих белков, таких как цитохромы и
миоглобин. Билирубин- конечный продукт распада всех гемсодержащих белков.
Дальнейший метаболизм билирубина происходит в печени. Билирубин, образованный в клетках РЭС (селезёнки и костного мозга), плохо растворим в воде, по крови транспортируется в комплексе с белком плазмы крови альбумином. Эту форму билирубина называют неконъюгированным или непрямым билирубином
В дальнейшем метаболизм билирубина складывается из трёх процессов:
поглощение паренхимальными клетками печени;
конъюгация билирубина в гладком эндоплазматическом ретикулуме гепатоцитов;
секреция из эндоплазматического ретикулума в жёлчь.

В результате реакций конъюгации образуется хорошо растворимый в воде прямой или конъюгированный, билирубин.
 Прямой
билирубин – это нормальный компонент
желчи, попадающий в
кровь в
незначительном
количестве. Он
может проходить
через почечный
барьер, но в крови в норме его мало,
поэтому в моче обычными
лабораторными методами он
не определяется.
Прямой
билирубин – это нормальный компонент
желчи, попадающий в
кровь в
незначительном
количестве. Он
может проходить
через почечный
барьер, но в крови в норме его мало,
поэтому в моче обычными
лабораторными методами он
не определяется.
