
Приложение 5.Электрохимические методы анализа
.pdfПри содержании меди в пробе 0,02 - 0,5 мг/л пробу концентрируют в 50 раз. В фарфоровой или стеклянной чашке выпаривают досуха 250 мл пробы с 1 мл концентрированной НС1. Полученный сухой остаток смачивают концентрированно НС1 и вновь выпаривают. Затем в чашку наливают 5,0 мл раствора, приготовленного непосредственно перед его использованием смешением 10 частей индифферентного электролита, 1 части раствора желатины, 39 частей дистиллированной воды с добавкой твердого сульфита натрия (при работе в режиме ДИП желатину исключают, а для составления смешанного раствора берут 40 частей дистиллированной воды). Содержимое чашки перемешивают до растворения сухого остатка, раствор переливают а сухую полярографическую ячейку и регистрируют кривую от -0,2 до -0,8 В относительно потенциала ртутного дна в том же режиме, в котором регистрировались полярограммы градуировочных растворов.
Концентрацию меди в полярографируемом растворе (С, мг/л) находят по градуировочному графику. Концентрацию меди в пробе (Х, мг/л) с учетом пробоподготовки находят по формуле:
X = |
C VП |
, |
(14.1) |
|
|||
|
V |
|
|
где VП - объем раствора, подготовленного для полярографирования, т.е. 25 или 5 мл в зависимости от ожидаемого содержания меди в пробе; V - объем пробы, взятый для определения.
6. Определить концентрацию меди в пробе методом добавок.
Для анализа отмерить два одинаковых объема пробы. К одной пробе прибавить стандартный раствор с определенной концентрацией меди (необходимо добавлять такое количество стандартного раствора, чтобы высота волны или пика возросла в 1,5 - 2 раза). Обе пробы обработать параллельно одинаковым способом (окончательные объемы растворов, подготовленных для полярографирования, должны быть одинаковыми). Записать вольтамперные кривые сначала в растворе без добавки, а затем с добавкой по три раза в том же режиме, в котором производилось определение меди по графику. Содержание меди в мг/л (Х) вычислить по формуле метода добавок:
X = h (VСТ C) CТ , (14.2) H −h V
где h - высота волны (или пика) пробы без добавки, мм; Н - то же для пробы с добавкой, мм;
V - объем пробы, взятый для определения, без добавки стандартного раствора, мл;
VСТ - объем добавки стандартного раствора, мл;
ССТ - концентрация добавленного стандартного раствора, мг/л. Можно использовать и графический вариант метода добавок.
71
Для этого приготовить три одинаковых объема пробы. В одну из них ввести небольшую по объему добавку стандартного раствора меди, а в другую - вдвое большую добавку того же раствора (объем добавок не должен превышать 1% от объема пробы, тогда разбавление можно не учитывать). Все три пробы обработать параллельно одинаковым способом (окончательные объемы растворов, подготовленных для полярографирования, должны быть одинаковыми).
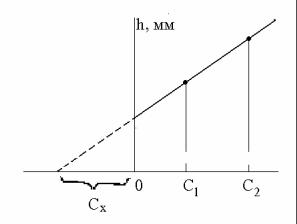
Записать вольтамперные кривые сначала в растворе без добавки, а затем - в растворах с меньшей и большей добавками по три раза в том же режиме, в котором производилось определение меди по графику. Для нахождения неизвестной концентрации меди поступают так, как показано на ри-
сунке 14.1.
Вправо от начала координат откладывают концентрации (в выбранных единицах масштаба), создаваемые в объеме пробы добавками стандартного раствора определяемого вещества. По оси ординат откладывают высоты волн или пиков (мм). Экстраполяция полученной прямой до пересечения с осью абсцисс дает отрезок, расположенный влево от условного нуля координат, величина которого в выбранном масштабе соответствует искомой концентрации Х.
7. Определить природу и концентрацию металлов, присутствующих в пробе совместно с медью. Совместно с медью на фоне аммиачного буфера на полярограмме могут появляться волны восстановления кадмия, никеля и цинка. Пробу готовят для полярографирования так, как описано выше (пункт 6). В выбранном режиме полярографируют пробу от -0,2 В до потенциала разряда фона. Для этого задают начальное значение потенциала - 0,2 В и увеличивают амплитуду развертки потенциала до 2 В.
Если концентрации всех элементов примерно одинаковы или концентрации элементов, восстанавливающихся при более отрицательных потенциалах, выше, чем концентрации элементов, восстанавливающихся при боле положительных потенциалах, полярографические волны отдельных элементов записывают с рационально выбранными чувствительностями так, чтобы была использована вся ширина диаграммной бумаги. Если же концентрации элементов с более положительным потенциалом полуволн
72
значительно выше концентраций остальных элементов, необходима более сложная пробоподготовка.
Определить характеристики всех волн (пиков) восстановления, наблюдаемых на полярограмме, записанной для пробы природной воды. Сравнить их с табличными значениями для отнесения наблюдаемых волн конкретному металлу. Определить высоты волн (пиков) каждого металла.
Проверить методом добавок правильность идентификации металлов, присутствующих в растворе. Для этого внести в ячейку 0,3 - 0,5 мл стандартного раствора одного из предполагаемых металлов и зарегистрировать полярограмму. Если число волн (пиков) на полярограмме и величины Е1/2 остаются неизменными, а высота одной из волн (пиков) возросла, следовательно эта волна (пик) соответствует восстановлению добавленного металла. Если на полярограмме еще остались неидентифицированные волны (пики), добавить стандартный раствор другого возможного металладеполяризатора и вновь записать полярограмму, и т.д. вплоть до идентификации всех волн (пиков), наблюдаемых на полярограмме.
При необходимости определить концентрацию металлов, присутствующих в пробе совместно с медью, построив для каждого из них градуировочный график или воспользовавшись методом добавок.
Работа 15. Определение свинца и цинка в питьевой воде
(составлено по ГОСТ 18293-72 Вода питьевая. Определение содержания свинца и цинка в одной пробе [полярографический метод])
Цель работы. Определить содержание свинца и цинка из одной пробы питьевой воды с использованием различных количественных методов, сравнить полученные результаты.
Введение. Естественными источниками поступления свинца и цинка в водную среду являются процессы выщелачивания горных пород, минералов и почв в районе рудных месторождений. Содержание цинка в поверхностных водах колеблется от единиц до сотен микрограммов в литре. Содержание свинца в незагрязненных речных и озерных водах обычно меньше 10 мкг/л. В районах месторождений полиметаллических руд содержание свинца в поверхностных водах может быть повышено до нескольких десятков микрограммов в литре.
Антропогенное загрязнение водных объектов соединениями свинца и цинка обусловлено их выносом со сточными водами. Для свинца - это, в первую очередь, сточные воды рудообогатительных фабрик, шахт, некоторых металлургических и химических предприятий, а для цинка - сточные воды предприятий горнодобывающей промышленности, гальванических цехов, производств минеральных красок и т.д. В питьевую воду свинец
73
может попадать кроме того из свинцовых труб или свинцовых деталей водопровода, а цинк в результате вымывания из оцинкованных водопроводных труб.
Свинец оказывает токсическое воздействие на гидробионты и человека. Описаны случаи острого и хронического отравления человека при попадании в желудок с водой и пищей достаточно больших количеств свинца. Свинцовое отравление связано с весьма разнообразными клиническими проявлениями. Так свинец обладает способностью поражать центральную и периферическую нервную систему, о чем свидетельствуют изменения поведения, депрессия, снижение памяти, нарушения движений, расстройства письма и речи. Действие свинца на кроветворение связано с вмешательством его в ферментативные процессы, обеспечивающие синтез предшественников гема. Имеются наблюдения, свидетельствующие о воздействии свинца на синтез белка, генетический аппарат клетки, а также об эмбриотоксическом и тератогенном действии свинца на человека. Поэтому содержание свинца нормируется как в поверхностных водах, так и в питьевой воде. ПДК растворённых форм свинца в воде водных объектов хозяй- ственно-питьевого и культурно-бытового назначения составляет 0,03 мг/л, рыбохозяйственных водоёмов - 0,1 мг/л, в питьевой воде - 0,01 мг/л.
Соединения цинка в повышенных концентрациях оказывают токсическое воздействие на гидробионты. Особенно сильно повреждаются жабры рыб. Сначала наблюдается фаза возбуждения и учащения дыхания, по мере разрушения респираторного эпителия наступают асфиксия и смерть. Значение ПДК для растворенных форм цинка для рыбохозяйственных водоемов составляет 0,01 мг/л, а для водных объектов хозяйственнопитьевого и культурно-бытового водопользования 1,0 мг/л (ЛПВ общесанитарный).
Воздействие цинка на человека связано с конкурентными отношениями цинка с рядом других металлов. Избыточное поступление цинка в организм сопровождается падением содержания кальция в крови и костях, одновременно нарушается усвоение фосфора, в результате развивается остеопороз. Цинк может представлять также онкогенную и мутагенную опасность для человека. ПДК растворимых форм цинка в питьевой воде, лимитированное по органолептическому признаку вредности, составляет 3,0 мг/л.
Сущность метода. Метод основан на восстановлении ионов свинца и цинка на ртутном капельном электроде. Продуктом восстановления является амальгама этих металлов. В среде 0,1 М раствора хлорной кислоты потенциалы полуволн восстановления ионов этих металлов различаются более, чем на 0,5 В, составляя -0,55 В для свинца и -1,13 В для цинка по отношению к насыщенному каломельному электроду. Предельный диффу-
74
зионный ток определяется уравнением Ильковича (ур. 13.1), поэтому концентрацию ионов металлов можно определить любым количественным методом: методом градуировочного графика, методом стандартных растворов и методом добавок.
Определению свинца мешает олово (Sn2+) в концентрации, превышающей в 1000 раз содержание свинца в исследуемой воде. Определению цинка мешает никель в концентрации, превышающей в 10 раз содержание цинка в пробе. Обычно такие концентрации олова и никеля в питьевой воде не встречаются.
Реактивы. 1. Индифферентный электролит, фон: 1 моль/л раствор хлор-
ной кислоты HClO4;
2. Стандартный раствор свинца, концентрации 1 мг Pb2+ в 1 мл. 1,600 г Pb(NO3)2 растворяют в бидистиллированной воде, содержа-
щей 1 мл концентрированной HNO3 в мерной колбе на 1 л.
Из него готовится рабочий стандартный раствор свинца с концен-
трацией 0,01 мг/мл.
3. Стандартный раствор цинка, концентрации 1 мг Zn2+ в 1 мл. 1,000 г металлического цинка растворяют в 7 мл HCl (1:1), раствор
переносят в мерную колбу вместимостью 1 л и доводят бидистиллированной водой до метки.
Из него готовится рабочий стандартный раствор цинка с концен-
трацией 0,1 мг/мл.
Ход работы
1. Познакомиться с устройством полярографа. См. раздел "Сущность метода" в работе 13.
2. Определить характеристики р.к.э. См. пункт 2 в разделе "Ход работы" работы 14.
3. Подготовить прибор к работе, выполнив пункт 2 раздела "Ход работы" работы 13.
4. Минерализация пробы и градуировочных растворов. Для определения отбирают 100 мл исследуемой воды, подкисленной при отборе пробы (если исследуемая вода не была подкислена, ее подкисляют 0,5 мл концентрированной HCl), помещают в химический стакан и выпаривают на водяной бане. Сухой остаток минерализуют на песчаной бане. Для этого к сухому остатку добавляют 0,5 мл концентрирован-ной серной кислоты и по каплям 2 мл концентрированной азотной кислоты и выпаривают досуха. Затем добавляют 0,5 мл перекиси водорода и 1 мл концентрированной соляной кислоты и вновь выпаривают на водяной бане. Для удаления остаточного количества кислоты сухой остаток дважды обрабатывают бидистиллиро-
75
ванной водой (порциями примерно по 10 мл) с последующим выпариванием до сухого остатка.
После такой обработки остаток количественно растворяют в 10 мл 0,1 М раствора хлорной кислоты (фона) и полярографируют.
Для построения градуировочного графика в мерных колбах емкостью 100 мл готовят серию стандартных растворов, содержащих одновременно свинец и цинк:
0,0; 1,0; 2,0; 4,0; 6,0; 8,0; 10 мкг свинца и 0,0; 10; 20; 40; 60; 80; 100 мкг цинка.
Полученные градуировочные растворы обрабатывают так же, как исследуемую пробу, получают в итоге по 10 мл градуировочных растворов, которые затем полярографируют.
При определении концентрации металлов методом добавок, добавку вносят в пробу перед минерализацией, а затем проводят через все стадии пробоподготовки параллельно пробу без добавки и пробу с добавкой.
Следует отметить, что в процессе минерализации происходит концентрирование проб и градуировочных растворов в 10 раз.
5. Построение градуировочного графика. При отработке методики на модельных растворах стадию минерализации можно исключить. Тогда для получения в градуировочных растворах тех же концентраций, что и после минерализации, градуировочные растворы необходимо готовить следующим образом. В мерные колбы на 25 мл налить рабочий стандартный раствор свинца с концентрацией 0,01 мг/мл и раствор цинка с концентрацией 0,1 мг/мл в количествах, указанных в таблице. В каждую колбу добавить по 2,5 мл концентрированного раствора фона (1 моль/л HClO4) и довести до метки бидистиллированной водой. Получится стандартная шкала с концентрациями свинца и цинка, указанными в таблице:
№ градуировочного раствора |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
Количества растворов свинца, |
|
|
|
|
|
|
|
0,01 мг/мл (цинка, 0,1 мг/мл) для |
|
|
|
|
|
|
|
приготовления градуиро-вочных |
0 |
0,25 |
0,5 |
1,0 |
1,5 |
2,0 |
2,5 |
растворов, мл |
|
|
|
|
|
|
|
(в колбах на 25 мл) |
|
|
|
|
|
|
|
Концентрация свинца в граду- |
0,0 |
0,1 |
0,2 |
0,4 |
0,6 |
0,8 |
1,0 |
ировочных растворах, мкг/мл |
|
|
|
|
|
|
|
Концентрация цинка в граду- |
0,0 |
1,0 |
2,0 |
4,0 |
6,0 |
8,0 |
10 |
ировочных растворах, мкг/мл |
|
|
|
|
|
|
|
Записать вольтамперные кривые градуировочных растворов, начиная с наиболее разбавленных, в режиме дифференциально-импульсной полярографии (ДИП). Для этого часть раствора залить в полярографическую ячейку, подключить электроды: РАБ - р.к.э., ВСП -платиновая пластинка и
76
СРАВН - насыщенный хлорсеребряный электрод. Включить трехэлектродный режим дифференциально-импульсной полярографии[ПП]. Установить начальное напряжение -0,2 В, амплитуду развертки 1,5 В, направление развертки потенциала - отрицательное, скорость развертки - 0,5х10 мВ/с, установить амплитуду переменного напряжения в интервале 5 - 10 мВ. Установить режим работы с принудительным отрывом капли - принудительный, режим регистрации полярограмм - таст. Включить синхронизацию (1 - 3), а также время задержки 1,0 - 1,5 с (это время составляет 2/3 от принудительного периода капания).
Для удаления растворенного кислорода в течение 10 минут продуть раствор инертным газом (в ходе записи вольтамперных кривых инертный газ продувать над раствором), и записать вольтамперную кривую, включив последовательно датчик, принудительный отрыв капли кнопкой СЧЕТ и развертку потенциала кнопкой ПУСК. По окончании записи вернуться к исходному потенциалу, нажав кнопку СБРОС, остановить принудительный отрыв капель кнопкой УСТАНОВКА НУЛЯ и отключить датчик. Если высота пиков на вольтамперной кривой мала (менее 25 мм), чувствительность прибора увеличить (уменьшить ДТ), если велика - уменьшить.
Запись каждой кривой при выбранном ДТ произвести три раза.
Из результатов трех параллельных измерений определить средние характеристики пиков восстановления свинца и цинка (потенциал пиков ЕП и их высоту hП). Если запись вольтамперных кривых различных градуировочных растворов производилась при разных ДТ, привести высоты пиков к одному ДТ. Построить две градуировочные зависимости, нанося высоты пиков свинца и цинка на ось ординат, а соответствующие концентрации в мкг/мл -на ось абсцисс.
6. Определить концентрацию свинца и цинка в модельном растворе по градуировочному графику. 20 мл раствора, содержащего свинец в концентрации ≥ 0,1 мкг/мл и цинк в концентрации ≥ 1 мкг/мл, налить в мерную колбу на 25 мл. Добавить 2,5 мл 1 М раствора хлорной кислоты (фон) и довести до метки бидистиллированной водой.
Часть раствора залить в ячейку для полярографирования, продуть инертным газом и трижды записать вольтамперную кривую в тех же условиях, в которых производилось полярографирование градуировочных растворов. Если пики свинца и цинка несоизмеримы по высоте, то, подобрав ДТ для свинца, записать вначале его пик. Затем остановить развертку потенциала кнопкой СТОП, изменить ДТ и, отжав кнопку СТОП, продолжить запись вплоть до полного прорисовывания пика цинка.
Из результатов трех параллельных измерений определить средние характеристики пиков восстановления свинца и цинка (потенциал пиков ЕП и их высоту hП). Высоты пиков привести к той же чувствительности (ДТ),
77
для которой построены градуировочные графики.
Концентрацию свинца (цинка) в полярографируемом растворе (С, мкг/мл) находят по градуировочному графику. Концентрацию в пробе (Х, мг/л) с учетом пробоподготовки находят по формуле:
X = |
C VП |
, |
(15.1) |
|
|||
|
V |
|
|
где VП - объем раствора, подготовленного для полярографирования, т.е. в данном случае 25 мл;
V -объем пробы, взятый для определения (в данном случае 20 мл). 7. Определить концентрацию свинца и цинка методом стандартных растворов. Из имеющихся вольтамперных кривых градуировочных растворов выбрать для каждого металла по две, имеющие наиболее близкие высоты пиков к высоте пика данного металла в модельном растворе (при одном ДТ). Градуировочные растворы, из которых записывались эти вольтамперные кривые, могут служить стандартами для определения концентрации в пробе методом стандартных растворов. Концентрацию ионов свинца (цинка) в модельном растворе (Х, мг/л) с учетом двух стандартных растворов
можно рассчитать по формуле: |
|
|
|||||||
|
|
|
|
′ |
′′ |
|
|
|
|
X = CСТ |
|
hX V V |
|
|
|
, |
(15.2) |
||
|
′ |
′′ |
|
′′ ′ |
) |
|
|||
|
10(h V |
|
+h V |
|
|
|
|||
где ССТ - концентрация рабочего стандартного раствора соли металла, использованного для приготовления градуировочных растворов, мг/л; V′ и V′′ - объемы рабочего стандартного раствора металла, взятые (см. таблицу) для приготовления градуировочных растворов, используе-
мых в качестве стандартов, мл;
hX - высота пика в модельном растворе, мм;
h′ и h′′ - высоты пиков в первом и втором стандартных растворах при том же ДТ, мм.
Проверьте правильность формулы (15.2), выведя ее из уравнения линейной зависимости высоты пика восстановления от концентрации металла.
8. Определить концентрацию свинца и цинка в модельном растворе методом добавок. В две мерные колбы емкостью 25 мл поместите по 20 мл модельного раствора. К одной пробе прибавьте некоторое количество рабочего стандартного раствора свинца и цинка (необходимо добавлять такое количество стандартных растворов, чтобы высоты пиков возросли в 1,5 - 2 раза). Затем в оба раствора добавьте по 2,5 мл 1 М раствора HClO4 и доведите бидистиллированной водой до метки. Запишите вольтамперные кривые сначала в растворе без добавки, а затем с добавками по три раза в режиме ДИП, предварительно продув растворы инертным газом для удаления растворенного кислорода. Содержание свинца (цинка) в мг/л (Х) вы-
78
числите по формуле метода добавок (ур. 14.2).
Сопоставьте концентрации свинца и цинка, определенные тремя различными количественными методами.
Работа 16. Определение хрома(VI) в природных водах методом переменнотоковой полярографии
(составлено по РД 118.02.16-88 Методика выполнения измерений содержания хрома (VI) в природных водах)
Цель работы. Определить содержание хрома (VI) в пробе природной воды методом градуировочного графика в режиме переменнотоковой полярографии. Произвести контроль точности и воспроизводимости измерения. Введение. В поверхностных водах содержание хрома, как правило, не превышает 10 мкг/л, однако в сильно загрязненных водных объектах его концентрация может достигать сотен микрограммов в литре. В водную среду хром попадает при выщелачивании из горных пород и минералов, из почв в районах рудных месторождений. Основным источником антропогенного поступления хрома в водные объекты являются сточные воды гальванических цехов, текстильных и кожевенных предприятий, а также химических производств.
Соединения хрома присутствуют в водах в растворённом и взвешенном состояниях, соотношения между которыми обусловлены химическим составом вод, температурой, рН, Еh и другими факторами. Во взвеси доминирующее положение занимает сорбированная форма. В растворе хром может присутствовать в двух степенях окисления: Cr(III) и Cr(VI).
Cr(III) устойчив в растворе и в реальных условиях существования водных объектов далее не окисляется. Cr(VI), существующий в виде хромат- или дихромат-ионов, относительно устойчив только в аэробных условиях, при дефиците кислорода и в присутствии восстановителей он быстро восстанавливается до Cr(III).
Соединения хрома, особенно Сr(VI) токсичны и обладают канцерогенным действием. ПДК хрома(VI) для рыбохозяйственных водоемов составляет 0,02 мг/л, для водных объектов хозяйственно-питьевого и куль- турно-бытового водопользования - 0,05 мг/л.
Сущность метода. Содержание хрома (VI) в природных водах в диапазоне концентраций 0,2 - 5,0 мг/л может быть определено методом переменнотоковой полярографии. Определение основано на способности хрома (VI) восстанавливаться на ртутном капельном электроде на фоне 0,1 М NH4Cl + 0,1 M NH3. При этом образуется три пика восстановления (ЕП′ = - 0,28 В, ЕП′′ = - 1,45 В, ЕП′′′ = - 1,60 В). Для аналитических целей используется пик с потенциалом ЕП = - 0,28 В. В этом случае определению мешает медь (II) при соизмеримых концентрациях.
79
Более низкие концентрации хрома непосредственно по пику его восстановления не определяются. Поэтому для измерения содержаний хрома (VI) в диапазоне концентраций 0,01 - 0,2 мг/л используются каталитические токи. Метод основан на способности хрома (VI) на аммиачнохлоридном буферном растворе (рН 10,2) в присутствии нитрита образовывать на ртутном капельном электроде каталитический пик (ЕП = - 1,6 В), который и используется для аналитических целей. Определению мешает хром (III).
Реактивы. 1. Аммиачно-хлоридный буферный раствор 0,5 М (фон 1). Рас-
творяют 26,75 г NH4Cl в 38 мл концентрированного раствора аммиака и доводят объем дистиллированной водой до 1 л.
2.Аммиачно-хлоридный буферный раствор 0,1 М с рН 10,2 (фон 2).
Из фона 1 готовят аммиачно-хлоридный буферный раствор с концентрацией 0,1 М и доводят рН до 10,2 концентрированным аммиаком.
3.Раствор нитрита натрия 1М. Растворяют 68,995 г NaNO2 в дис-
тиллированной воде в мерной колбе на 1 л.
4.Стандартный раствор хрома (VI), концентрации 1 мг/мл. Рас-
творяют 3,7344 г K2Cr2O7 в дистиллированной воде и доводят объем до 1 л. Из него непосредственно перед определением готовят рабочие рас-
твор хрома (VI) концентрации 100 мг/л и 10 мг/л.
Ход работы
1. Познакомиться с устройством полярографа. См. раздел "Сущность метода" в работе 13.
2. Определить характеристики р.к.э. См. пункт 2 в разделе "Ход работы" работы 14.
3. Подготовить прибор к работе, выполнив пункт 2 раздела "Ход работы" работы 13.
4. Построить градуировочный график и определить по нему концентрацию хрома (VI) в пробе в диапазоне 0,01 - 0,2 мг/л. Для построения градуировочного графика в мерные колбы вместимостью 25 мл помещают по 10 мл фонового раствора № 2 , т.е. 0,1 М NH4Cl + NH3 (рН 10,2), по 0,25 мл 1 М
раствора NaNO2 и по 0; 0,025; 0,05; 0,075; 0,1; 0,15; 0,20; 0,40 мл рабо-
чего раствора хрома (VI) с концентрацией 10 мг/л. При этом концентрации хрома (VI) в приготовленных растворах будут равны соответственно 0; 0,01; 0,02; 0,03; 0,04; 0,06; 0,08; 0,16 мг/л. Доводят объем до метки ам-
миачно-хлоридным буферным раствором (фон 2) и перемешивают.
Часть раствора переносят в ячейку для полярографирования, продувают его инертным газом для удаления растворенного кислорода и снимают переменнотоковую полярограмму.
Для этого подключают электроды: РАБ - р.к.э. и ВСП - ртуть на дне
80
