
- •1.Охарактеризуйте обмен веществ и энергии как сопряженную систему катаболических и анаболических процессов
- •2.Макроэргические вещества и радикалы. Строение и функции атф в организме.
- •4)Дыхательная цепь и комплексы с переносом заряда.
- •5)Структура и функции конкретных компонентов дыхательной цепи.
- •6.Функции атф-синтетазы и молекулярного кислорода в клеточном дыхании.
- •7. )Механизм синтеза атф путем окислительного фосфорилирования
- •8. ) Механизм и биологическое значение разобщения окислительного фосфорилирования.
- •9.Цикл лимонной кислоты – центральный процесс энергетического обмена
- •10.) Регулирование скорости цикла лимонной кислоты.
- •11.Пути образования активного ацетила.
- •12.Пути потребления активного ацетила.
- •13) Назначение и пути потребления кетоновых тел
- •14.Пути образования и превращения пвк
- •15.Синтез жира из углеводов.
- •16.Особенности превращений углеводов в пищеварительном тракте и в ходе метаболизма в организме жвачных.
- •17.Биохимические механизмы поддержания нормального уровня глюкозы в крови при голодании.
- •18.Биологическое значение пентозного пути окисления углеводов.
- •19.Нарушение углеводного обмена.
- •1. Нарушение всасывания углеводов в жкт
- •2. Состояния, при которых нарушен процесс синтеза или расщепления гликогена
- •3. Состояния, вызывающие нарушения промежуточного обмена углеводов
- •4. Гипергликемия
- •20. Пути образования и превращений фосфатидной кислоты.
- •21.Спонтанное свободнорадикальное окисление ненасыщенных соединений и пути его предотвращения. Антиоксиданты
- •22.Строение и функции клеточных мембран, их участие в метаболизме.
- •23. Транспорт липидов в организме.
- •24.Метаболизм липидов и холестерина.
- •25. Строение, синтез и биологическое значение холестерола.
- •26. Биологически активные производные холестерина.
- •27. Нарушение липидного обмена.
- •28. Биохимические механизмы образования и утилизации аммиака в организме.
- •29. Участие трансаминаз в метаболизме.
- •30) Биохимическая роль нуклеотидов в метаболизме.
- •31. Отличия и сходства строения днк и рнк.
- •32. Отличия и сходства механизмов синтез днк и рнк.
- •33. Субстраты, ферменты и механизм синтеза и репарации днк.
- •36. ) Конечные продукты пуринового обмена у разных видов животных.
- •37.) Особенности азотистого обменау разных видов животных.
8. ) Механизм и биологическое значение разобщения окислительного фосфорилирования.
Присутствие во внутренней митохондриальной мембране агентов (ионофоров), увеличивающих их проницаемость для Н+, разобщает окислительное фосфорилирование от процесса транспорта электронов, поскольку при этом нарушается генерирование электро-химического потенциала и, следовательно, синтез АТФ. ДНФ является липофильной слабой кислотой, поэтому легко проходит через мембрану (снаружи внутрь митохондрии), ослабляя естественный ток протонов, идущий в противоположном направлении.
Путь транспорта электронов, не связанный с синтезом АТФ, называется свободным, нефосфорилирующим, окислением. При свободном окислении энергия не аккумулируется, а высвобождается в виде тепла. Это имеет физиологическое значение при охлаждении организма.
Частичное разобщение окисления и фосфорилирования наблюдается при многих заболеваниях, так как митохондрии являются наиболее чувствительными клеточными органеллами к действию различных повреждающих факторов. Нарушение их структуры, приводящее к частичному или полному распаду внутренней митохондриальной мембраны, неизбежно будет способствовать обратному току протонов и нарушать энергопродукцию. Поэтому особое значение приобретает стабилизация митохондриальных мембран биоантиоксидантами (витаминами Е, А и аскорбатом) при любой патологии.
В ряде случаев некоторые пункты фосфорилирования могут «выключатся» - такое состояние называется разобщением окислительного фосфорилирования - и в этом случае P/O снижается: для НАД-зависимых субстратов - ниже 3; для ФАД-зависимых субстратов - ниже 2-ух.
И исходя из 1-го закона термодинамики в разобщенных митохондриях увеличивается теплообразование. (Это происходит за счет того, что та энергия электронов, которая должна была быть использована для синтеза АТФ в «выключенном» пункте фосфорилирования, рассеивается в виде тепла).
Процесс разобщения окислительного фосфорилирования лежит в основе лихорадки, вызванной бактериями, вирусами и другими агентами.
Разобщение резко усиливается при охлаждении организма.
Работа митохондрий при «выключенных» всех пунктах фосфорилирования называется сопряженной, в противном, выше описанном случае, разобщенной и дыхание при этом называется свободным.
В качестве разобщителей окислительного фосфорилирования выступают слабые гидрофобные кислоты (ЖК), тиреоидные гормоны, лекарства(дикумарин, динитрофенол).
ДЦ имеет механизмы шунтирования: сброс электронов и протонов по протяжению с НАД на цитохромы, или с НАД на межмембранные дегидрогеназы, на наружную мембрану и гладкую ЭПС (микросомальную цепь).
Такой перенос характерен для печени. При воздействии какого-либо блокатора, возникает блок в 1-ом комплексе ДЦ, происходит накопление НАД.Н2 и становится реальной угроза гипоксии, печень может погибнуть. Чтобы этого не произошло происходит сброс НАД.Н2 с митохондрий ДЦ на микросомальную ДЦ через цитохром b5.
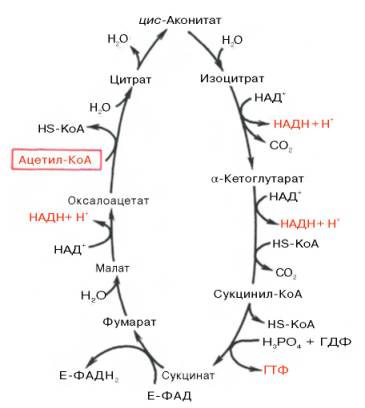
9.Цикл лимонной кислоты – центральный процесс энергетического обмена
Цикл Кребса - общий конечный путь окисления ацетильных групп (в виде ацетил-КоА), в которые превращается в процессе катаболизма большая часть органических молекул, играющих роль "клеточного топлива": углеводов, жирных кислот и аминокислот.
Образовавшийся в результате окислительного декарбоксилирования пирувата в митохондриях ацетил-КоА вступает в цикл Кребса. Данный цикл происходит в МАТРИКСЕ МИТОХОНДРИЙ и состоит из восьми последовательных реакций.
Начинается цикл с присоединения ацетил-КоА к оксалоацетату и образования лимонной кислоты (цитрата). Затем лимонная кислота путем ряда дегидрирований (отнятие водорода) и двух декарбоксилирований (отщепление CO2) теряет два углеродных атома и снова в цикле Кребса превращается в оксалоацетат, т.е. в результате полного оборота цикла одна молекула ацетил-КоА сгорает до СО2 и Н2О, а молекула оксалоацетата регенерируется.
 ЩУКа
съела ацетат, получается цитрат
через
цисаконитат будет он изоцитрат
водороды
отдав НАД, он теряет СО2
этому
безмерно рад альфа-кетоглутарат
окисление
грядет — НАД похитил водород
ТДФ,
коэнзимА забирают СО2
а
энергия едва в сукциниле появилась
сразу
АТФ родилась и остался сукцинат
вот
добрался он до ФАДа — водороды тому
надо
фумарат
воды напился, и в малат он превратился
тут
к малату НАД пришел, водороды приобрел
ЩУКа
снова объявилась и тихонько затаилась.
ЩУКа
съела ацетат, получается цитрат
через
цисаконитат будет он изоцитрат
водороды
отдав НАД, он теряет СО2
этому
безмерно рад альфа-кетоглутарат
окисление
грядет — НАД похитил водород
ТДФ,
коэнзимА забирают СО2
а
энергия едва в сукциниле появилась
сразу
АТФ родилась и остался сукцинат
вот
добрался он до ФАДа — водороды тому
надо
фумарат
воды напился, и в малат он превратился
тут
к малату НАД пришел, водороды приобрел
ЩУКа
снова объявилась и тихонько затаилась.
Первая реакция катализируется ферментом цитрат-синтазой, при этом ацетильная группа ацетил-КоА конденсируется с оксалоацетатом, в результате чего образуется лимонная кислота.
В результате второй реакции образовавшаяся лимонная кислота подвергается дегидратированию с образованием цис-аконитовой кислоты, которая, присоединяя молекулу воды, переходит в изолимонную кислоту (изоцитрат). Катализирует эти обратимые реакции гидратации–дегидратации фермент аконитатгидратаза (аконитаза). В результате происходит взаимоперемещение Н и ОН в молекуле цитрата.
Третья реакция, по-видимому, лимитирует скорость цикла Кребса. Изолимонная кислота дегидрируется в присутствии НАД-зависимой изоцитратдегидрогеназы.
В ходе изоцитратдегидрогеназной реакции изолимонная кислота одновременно декарбоксилируется. НАД-зависимая изоцитратдегидрогеназа является аллостерическим ферментом, которому в качестве специфического активатора необходим АДФ. Кроме того, фермент для проявления своей активности нуждается в ионах Mg2+ или Мn2+.
Во время четвертой реакции происходит окислительное декарбоксилирование α-кетоглутаровой кислоты с образованием высокоэнергетического соединения сукцинил-КоА. Механизм этой реакции сходен с таковым реакции окислительного декарбоксилирования пирувата до ацетил-КоА, α-кетоглутаратдегидрогеназный комплекс напоминает по своей структуре пируватдегидрогеназный комплекс. Как в одном, так и в другом случае в реакции принимают участие 5 коферментов: ТПФ, амид липоевой кислоты, HS-KoA, ФАД и НАД+.
Пятая реакция катализируется ферментом сукцинил-КоА-синтетазой. В ходе этой реакции сукцинил-КоА при участии ГТФ и неорганического фосфата превращается в янтарную кислоту (сукцинат). Одновременно происходит образование высокоэргической фосфатной связи ГТФ за счет высокоэргической тиоэфирной связи сукцинил-КоА.
В результате шестой реакции сукцинат дегидрируется в фумаровую кислоту. Окисление сукцината катализируется сукцинатдегидрогеназой, в молекуле которой с белком прочно (ковалентно) связан кофермент ФАД. В свою очередь сукцинатдегидрогеназа прочно связана с внутренней митохондриальной мембраной.
Седьмая реакция осуществляется под влиянием фермента фумаратгидратазы (фумаразы). Образовавшаяся при этом фумаровая кислота гидратируется, продуктом реакции является яблочная кислота (малат). Следует отметить, что фумаратгидратаза обладает стереоспецифичностью – в ходе реакции образуется L-яблочная кислота.
Наконец, в ходе восьмой реакции цикла трикарбоновых кислот под влиянием митохондриальной НАД-зависимой малатдегидрогеназы происходит окисление L-малата в оксалоацетат.
. Все ферменты, участвующие в реакциях цикла Кребса, локализованы в митохондриях, причем большинство из них растворимы, а сукцинатдегидрогеназа прочно связана с мембранными структурами.
Тесное сопряжение цикла Кребса с дыхательной цепью, особенно в митохондриях животных, а также ингибирование большинства ферментов цикла под действием АТФ, предопределяют снижение активности цикла при высоком фосфорильном потенциале клетки, т.е. при высоком соотношении концентраций АТФ/АДФ. У большинства растений, бактерий и многих грибов тесное сопряжение преодолевается развитием несопряженных альтернативных путей окисления, позволяющих поддерживать одновременно дыхательную активность и активность цикла на высоком уровне даже при высоком фосфорильном потенциале.
Функции цикла трикарбоновых кислот многообразны:
Интегративная – цикл Кребса является центральным метаболическим путём, объединяющим процессы распада и синтеза важнейших компонентов клетки.
Анаболическая – субстраты цикла используются для синтеза многих других соединений: оксалацетат используется для синтеза глюкозы (глюконеогенез) и синтеза аспарагиновой кислоты, ацетил-КоА – для синтеза гема, α-кетоглутарат – для синтеза глютаминовой кислоты, ацетил-КоА – для синтеза жирных кислот, холестеролаа, стероидных гормонов, ацетоновых тел и др.
Катаболическая – в этом цикле завершают свой путь продукты распада глюкозы, жирных кислот, кетогенных аминокислот – все они превращаются в ацетил-КоА; глутаминовая кислота – в α-кетоглутаровую; аспарагиновая – в ЩУК и пр.
Собственно энергетическая – одна из реакций цикла (распад сукцинил-КоА) является реакцией субстратного фосфорилирования. В ходе этой реакции образуется 1 молекула ГТФ (реакция перефосфорилирования приводит к образованию АТФ).
Водороддонорная – при окислении 3-х НАД+-зависимых субстратов (изоцитрата, α-кетоглутарата и малата) и ФАД-зависимого сукцината образуются 3 НАДН∙Н+ и 1 ФАДН2. Эти восстановленные коферменты являются донорами водорода для дыхательной цепи митохондрий, энергия переноса водородов используется для синтеза АТФ. При этом за счёт окисления 3-х молекул НАДН∙Н+ образуется 3АТФ × 3 = 9 АТФ и за счёт окисления 1 молекулы ФАДН2 - 2 АТФ. Итого водороддонорная функция цикла Кребса обеспечивает образование 11 молекул АТФ, а, учитывая энергетическую функцию цикла, получаем за полный его оборот («сгорание» 1 молекулы ацетил-КоА) 12 молекул АТФ.
Анаплеротическая – восполняющая. Основным дефицитом при работе цикла является ЩУК. Её недостаток восполняется реакцией, катализируемой пируваткарбоксилазой
