
- •1. Антикоагулянты непрямого действия, образование 4-гидроксикумарина и дикумарола в природе, синтез варфарина.
- •2. Механизм антикоагулянтной активности структурных аналогов витамина к. Предполагаемый механизм выработки резистентности к варфарину,пути ее преодоления.
- •3. Антикоагулянтная активность индан-1,3-дионов. Получение дифенацина. Преимущества и недостатки ратицидов с острой и хронической токсичностью.
- •4. Эмпирический подход к оптимизации структуры ратицида на основе дифениламина. Получение брометалина – n-метил-2,4-динитро-2´,4´,6´-трибром-6-трифторметил-дифениламина.
- •5. Контактные и системные фунгициды, примеры, преимущества и недостатки. Получение дитиокарбаматов из аминов и сероуглерода. Соли дитиокарбаминовых кислот с катионами цинка и марганца.
- •6. Механизм действия азольных антимикотических средств, триазольные и имидазольные фунгициды. Синтез тебуконазола – третбутил-2-(4-хлорфенил)этил-триазол-1-илметил-карбинола.
- •7. Механизм токсичности циановодорода. Получение циановодорода в промышленности, использование в синтезе мономеров.
- •9. Химические реагенты, вызывающие отёк лёгких. Химические свойства дихлорангидрида угольной кислоты: реакции со спиртами, фенолами, первичными, вторичными и третичными аминами.
- •10. Инсектицидная активность фенвалерата. Получение эфира α-(4-хлорфенил)- изовалериановой кислоты и циангидрина 3-феноксибензальдегида.
- •11. Механизм токсичности монооксида углерода. Способы получения и токсичность карбонилов металлов, их участие в реакции оксосинтеза.
- •13.Фунгицидная активность бензимидазолил-метилкарбамата и бенлата. Способы их получения.
- •14.Химические свойства 2,2´-дихлордиэтилсульфида, реакции окисления (токсичность соответствующих сульфоксидов и сульфонов), хлорирование, реакции по атомам хлора 2-хлорэтильных групп.
- •15. Вещества раздражающего действия, общие представления о зависимости структура-активность для галогенидов и непредельных соединений. Индекс безопасности. Получение хлорацетофенона.
- •16.Агонисты ацетилхолина в м- и n-холинорецепторах, токсичность никотина. Неоникотиноиды, получение имидаклоприда: синтез 6-хлор-3-хлорметилпиридина и 2‑нитроиминоимидазолидина.
- •17. Роль ювенильных гормонов в жизненном цикле насекомых с полным метаморфозом. Способ получения метопрена – изопропилового эфира 11-метокси-3,7,11-триметилдодека-2,4-диеновой кислоты.
1. Антикоагулянты непрямого действия, образование 4-гидроксикумарина и дикумарола в природе, синтез варфарина.
Антикоагулянты непрямого действия блокируют редуктазу эпоксида витамина К, после чего начинается накопление эпоксидированного нафтохинонового витамина К и прекращается образование карбоксилированного протромбина, а образующийся из него тромбин не активируется ионами кальция. Из-за блокировки этих ферментативных превращений фибриноген больше не может превращаться в фибрин, из чего следует, что тромбы больше не образуются.
Антикоагулянты непрямого действия при добавлении их к донорской крови не влияют на её свёртываемость, т.к. в ней содержатся все факторы, которые вызывают превращение фибриногена в фибрин. Антагонисты витамина К блокируют образование карбоксилированного протромбина долгое время, когда неспособный к активации ионов кальция протромбин заменит активный протромбин, который образовался до начала действия блокаторов γ-карбоксилазы, это всё будет являться проявлением антикоагулятной активности.
Гликозилированная транс-о-гидроксикоричная кислота превращается в лактон цис-2-гидроксикоричной кислоты (кумарин), пахнущий сеном. После кумарин окисляется и превращется в 4-гидроксикумарин. Который конденсируется в дикумарол в реакции с формальдегидом:
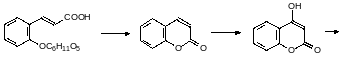
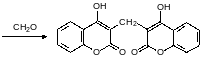
Вафарин получают по реакции 4-гидроксикумарина с бензилиденацетоном по реакции Михаэля, катализатором является кислый фосфат с аммонийными катионами:

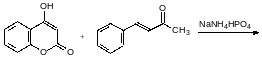
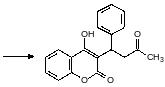
2. Механизм антикоагулянтной активности структурных аналогов витамина к. Предполагаемый механизм выработки резистентности к варфарину,пути ее преодоления.
Посттрансляцинное карбоксилирование молекулы протромбина:
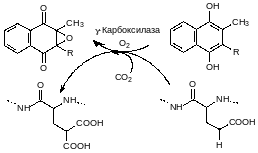
В данной реакции востановл. форма витамина К является косубстратом. Гидрохинон витамина К в посттрансляционном карбоксилирование дважды окисляется: сначала превращается в хинон, затем в эпоксид витамина К. Редуктаза витамина К восстанавливает это производное с образованием соответствующего хинона:
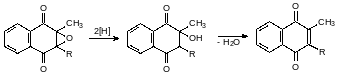
Далее хиноидный витамин К восстанавливается в гидрохинон:
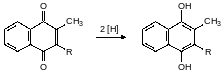
Редуктаза эпоксида витамина К блокируется его антиметаболитами, после чего прекращается образование карбоксилированного протромбина, а образующийся из него тромбин не активируется ионами кальция. После этого фибриноген не может превращаться в фибрин и тромбы прекращают своё образование.
После активного использования вафарина для борьбы с грызунами привело к резистентности крыс и мышей. Биохимический механизм резистентности:
После применения вафарина выживали особи с эффективными механизмами второй фазы биотрансформации ксенобиотиков превращающими, например, продукт таутомерии варфарина в неактивный и растворимый в воде глюкуронид по катализируемой глюкуронилтрансферазой реакции с уридиндифосфатглюкуроновой кислотой:
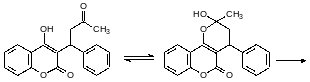
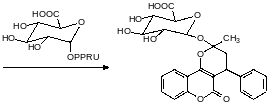
Доказательством данной схемы является - наличие антикоагулянтной активности у 3-замещённых 4-гидроксикумарино, в молекуле которых нет карбонильной группы в этом заместителе, например, у лекарственного средства маркумар :
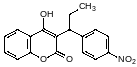
Куматетралил преодолевает резистентность к вафарину:
3. Антикоагулянтная активность индан-1,3-дионов. Получение дифенацина. Преимущества и недостатки ратицидов с острой и хронической токсичностью.
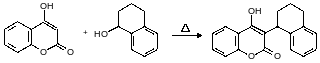
Антиноагулятная активность впервые была обнаружена у 2-фенилиндан-1,3-дион (фениндион, фениилин). Фениндион получают конденсацией фталида с бензальдегидом при сильных основаниях. Сначала образуется бензилиденфталид, но после перегруппировки образуется 2-фенилиндан-1,3-дин.
В результате циклизации диметилового эфира фталевой кислоты с кетонами (один из радикалов, связанных с карбонильной группой –СОН, явл-ся метильная группа).
Как пример, можно взять 2-пивалоилиндан-1,3-дион. По токсичности от близок к вафарину: для крыс составляет 230-330 мг/кг при хронической токсичности – пять раз по 2,0 мг/кг. Пивал образуется в реакции диметилфталата с пинаколином при сильных оснований.
Соединения с повышенной липофильностью заместителя отличаются бОльшей токсичностью. Дифенацин образуется циклизайией диметилфталата с 1,1-дифенилацетоном. Другой способ получения: синтез фенилацетона пиролизом смеси уксусной и фенилуксусной кислоты, катализатор - оксид бария. Разложение при всокой температуре бариевой соли уксусной и фенилуксусной кислот:
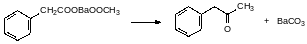

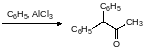
Далее дифенилацетон конденсируют с диметилфаталатом.
Антикоагулянты непрямого действия явлюятся идеальными ратициадами, т.к имеют отсроченный токсический эффект.
Высокая хроническая токсичность и невысокая острая токсичность делают эти препараты более безопасными, чем препараты с высокой острой токсичностью, тем более, что для лечения случайных отравлений антикоагулянтами можно использовать витамин К и викасол.
