
2793
.pdf7
Нумерацию атомов углерода начинают с карбоксильной группы. Названия кетокислот образуют подобным образом. Обозначать следует только те атомы углеродной цепи, у которых находятся оксиили кетогруппы, т.е. только в радикале кислоты.
CH3–C–COOH |
2-оксопропановая кислота |
|
|| |
|
|
O |
|
|
HOOC – CH – CH – COOH |
||
| |
| |
2,3 – диоксибутандиовая кислота |
OH |
OH |
|
|
|
O |
5 4 3 |
2 |
1 ⁄⁄ |
CH3–CH–CH2–C–C–OH 4-метил-2-оксопентановая кислота
| ||
CH3 O
СH3– C – COOH
||
О2-оксопропановая кислота
Для некоторых соединений со смешанными функциями часто используется тривиальная номенклатура.
HO – CH2 – COOH |
гликолевая кислота (Т) |
|
CH3 – CH – COOH |
молочная кислота (Т) |
|
| |
|
|
OH |
|
|
CH – COOH |
|
глиоксалевая кислота (Т) |
|| |
|
|
O |
|
|
HOOC–CH2–CH–COOH |
яблочная кислота (Т) |
|
|
| |
|
|
OH |
|
HOOC – CH – CH – COOH |
винная кислота (Т) |
|
| |
| |
|
OH |
OH |
|
|
8 |
HOCH2 – CH – CH=O |
глицериновый альдегид (Т) |
| |
|
OH |
|
СH3 – C – COOH |
пировиноградная кислота (Т) |
|| |
|
O |
|
Относительная и абсолютная конфигурация и номенклатура оптических изомеров
Для соединений с асимметрическим атомов углерода (имеющим 4 разных заместителя) характерна оптическая изомерия. Оптические изомеры могут иметь относительную и абсолютную конфигурацию. Относительная конфигурация определяет принадлежность к D или L генетическому ряду.
При написании формул оптических изомеров функциональные группы располагаются следующим образом: вверху помещают главную функциональную группу, атомы углерода записывают сверху вниз, а слева и справа от атома углерода располагают другие группы. По положению старшего заместителя у асимметрического атома углерода, наиболее удаленного от главной функциональной группы определяют D или L конфигурацию. Если
старший заместитель находится справа, то это D |
изомер, если слева – то L. |
|
За эталон был принят глицериновый альдегид. Ниже приведены D или |
||
L конфигурация глицеринового альдегида: |
|
|
O |
|
O |
// |
|
// |
C |
C |
|
| H |
| |
H |
H –C – OH |
HO–C– H |
|
| |
| |
|
CH2OH |
CH2OH |
|
D – глицериновый альдегид |
L – глицериновый альдегид |
|
Если у последнего асимметрического атома углерода от главной функ- |
||
циональной группы расположение заместителей соответствует D- |
||
глицериновому альдегиду, то оптический изомер |
относят к D-ряду. Если |
|
соответствует L-глицериновому альдегиду, то относят к L-ряду, например: |
||
COOH |
COOH |
|
| |
| |
|
H– C – Br |
H– C – Br |
|
| |
| |
|
H– C – OH |
HO – C – H |
|
| |
| |
|
COOH |
COOH |
|
D – бромяблочная кислота |
L –бромяблочная кислота |
|
9
Углеводы. Моносахариды
Простые углеводы, не подвергающиеся гидролизу, иначе называются моносахаридами или монозами, а также гликозами. Для моносахаридов характерно общее окончание – ОЗА. В зависимости от количества атомов углерода моносахариды делятся на триозы (С3Н5О3), тетрозы (С4Н6О4), пентозы (С5Н10О5), гексозы (С5Н12О5) и т.д. Моносахариды представляют собой многоатомные оксиальдегиды (альдегидоспирты) или оксикетоны (кетоноспирты). Моносахариды, содержащиеся в оксикарбонильной форме альдегидную или кетонную группу, называют соответственно альдозами или кетозами. В зависимости от числа углеродных атомов различают альдогексозы, кетогексозы, альдопентозы и т.д. Например:
⁄⁄ |
O |
CH2–OH |
CH2OH |
|
| |
| |
|
C |
C=О |
C=O |
|
|
H |
| |
| |
H–C–OH |
H– C –OH |
H–C–OH |
|
| |
|
| |
| |
H–C–OH |
H– C –OH |
H–C–OH |
|
| |
|
| |
| |
CH2OH |
CH2OH |
H–C–OH |
|
|
|
|
| |
|
|
|
CH2OH |
альдотетроза |
кетопентоза |
кетогексоза |
|
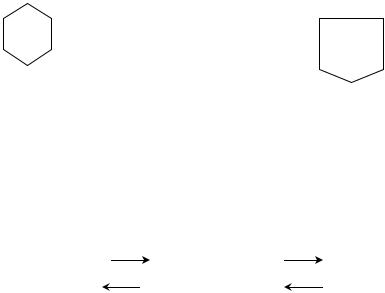
Пространственное строение моносахаридов выражают проекционными формулами (формулы Фишера). Наиболее распространенные моносахариды – гексозы:
O |
O |
O |
CH2OH |
// |
// |
// |
| |
С |
C |
C |
C=O |
| H |
| H |
| H |
| |
H–C–OH |
HO–C–H |
H–C–OH |
HO–C–H |
| |
| |
| |
| |
HO–C–H |
HO–C–H |
HO–C–H |
H–C–OH |
| |
| |
| |
| |
H–C–OH |
H–C–OH |
HO–C–H |
H–C–OH |
| |
| |
| |
| |
H–C–OH |
H–C–OH |
H–C–OH |
CH2OH |
| |
| |
| |
|
CH2OH |
CH2OH |
CH2OH |
|
D-глюкоза |
D-манноза |
D-галактоза |
D-фруктоза |
|
|
10 |
|
|
|
Пентозы: |
|
H |
O |
O |
O |
\ |
// |
// |
// |
C |
|
C |
C |
| |
|
| H |
| H |
H–C–OH |
HO–C–H |
H–C–OH |
|
| |
|
| |
| |
HO–C–H |
H–C–OH |
H–C–OH |
|
| |
|
| |
| |
H–C–OH |
H–C–OH |
H–C–OH |
|
| |
|
| |
| |
CH2OH |
CH2OH |
CH2OH |
|
D- ксилоза |
D- арабиноза |
D-рибоза |
|
Приведены тривиальные названия моноз. Кроме открытой (оксикарбонильной) формы моносахариды могут существовать в виде циклических полуацетальных форм.
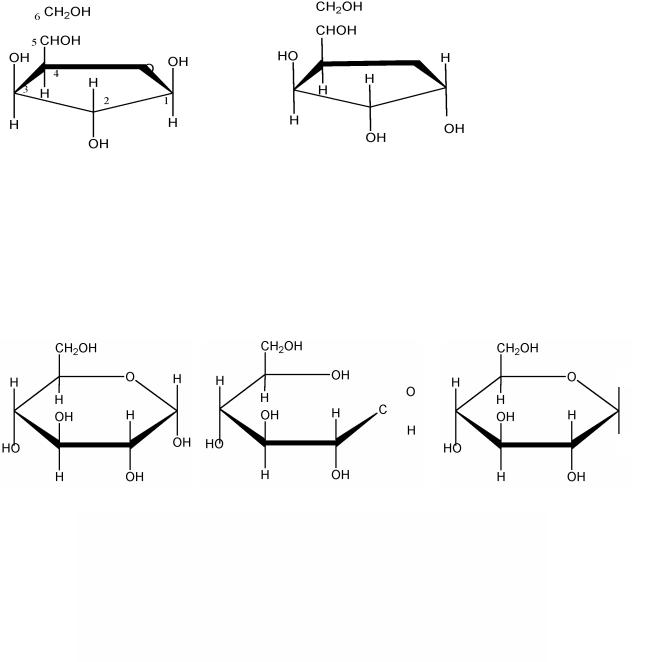
Образование полуацетальной формы в альдозах происходит при взаимодействии альдегидной группы со спиртной группой 5-го или 4-го атома углерода. При этом образуется кислотосодержащие кольцо (цикл), а кислород карбонильной группы образует гидроксил (полуацетальный, гликозидный). Шестичленное кольцо с кислородом носит название пираноза. Пятичленное
– фураноза. Эти названия происходят от названий соответствующих гетероциклических соединений.
|
|
СН2 |
|
|
|
|
|
|
|
|
|
|
|||||||
HC |
|
|
|
|
СH |
|
HC |
|
|
|
CH |
||||||||
|
|
|
|
|
|
||||||||||||||
|
|
|
|||||||||||||||||
НС |
|
|
|
|
СН пиран |
|
|
|
|
|
|
|
фуран |
||||||
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
О |
|
HC |
|
|
|
CH |
||||||||||
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
||||||
ОН |
Н |
⁄⁄ |
О |
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||
С–––––– |
|
|
C |
|
|
|
|
CH2OH |
|||||||||||
|
|
|
|
|
|||||||||||||||
| |
|
|
|
|
|
|
|
|
| Н |
| |
|
|
|
|
|||||
Н–C–ОН |
|
|
Н–C–OН |
|
НО–C |
|
|
|
|||||||||||
|
|
|
|
|
|||||||||||||||
| |
|
|
|
|
|
|
|
|
| |
|
| |
|
|
|
|
||||
HO–C–H |
|
|
HO–C–H |
|
HO–C–H |
|
|||||||||||||
|
|
||||||||||||||||||
| |
|
|
|
О |
| |
|
| |
|
|
|
|
||||||||
|
|
|
|
||||||||||||||||
H–C–OH |
|
|
H–C–OH |
|
H–C–OH О |
||||||||||||||
|
|
||||||||||||||||||
| |
|
|
|
|
|
|
|
|
| |
|
| |
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||
H–C–––––– |
|
|
H–C–OH |
|
H–C |
|
|
||||||||||||
|
|
|
|
|
|||||||||||||||
| |
|
|
|
|
|
|
|
|
| |
|
| |
|
|
|
|
||||
CH2ОН |
CH2OH |
|
|
|
CH2OH |
||||||||||||||
полуацетальная |
альдогексоза |
полуацетальная форма |
форма альдозы |
оксикарбонильная |
альдозы (фураноза) |
(пираноза) |
(альдоза) |
|
11
Полуацетальные формы кетоз также имеют либо шестичленное, либо пятичленное кислородосодержащие кольцо. Шестичленное кольцо (пираноза) образуется в результате взаимодействия кетонной группы при втором атоме углерода со спиртовой группой при шестом атоме углерода, а пятичленное (фураноза) – за счет взаимодействия со спиртовой группой 5-го углерода:
|
|
CH2OH |
|
CH2OH |
|
CH2OH |
||||||||||
HO |
|
|
|
|
|
|
|
|
С==O |
HO |
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
||||||
HO |
|
|
|
H |
|
HO |
|
|
|
Н |
Н |
|
|
OH |
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
О |
|
Н |
|
|
|
OH О |
Н |
|
|
|
OH |
H |
|
|
OH |
|
||
|
|
|
|
|
|
|
|
|||||||||
Н |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
OH |
|
Н |
|
|
|
OH |
H |
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2OH |
|
|
|
CH2OH |
|
CH2OH |
||||||||
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
||||||||||||
полуацетальная |
кетоза |
|
полуацетальная |
|||||||||||||
(пиранозная) |
фруктоза |
|
(фуранозная) |
|||||||||||||
форма кетозы |
оксикарбонильная форма |
|
форма кетозы |
|||||||||||||
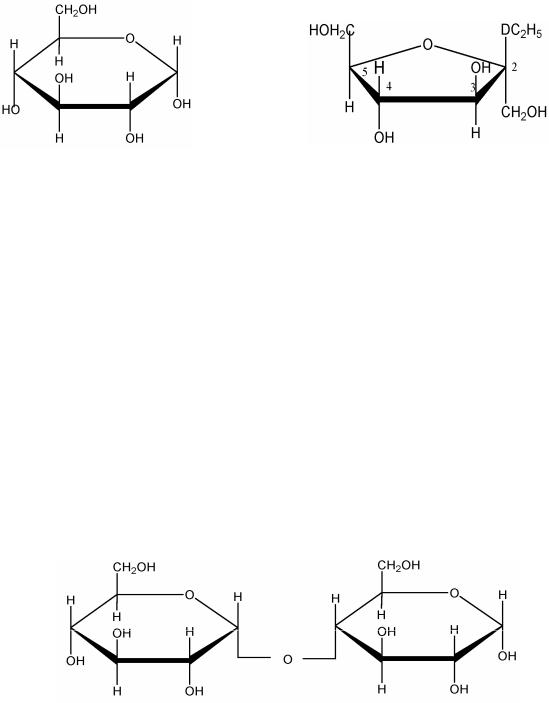
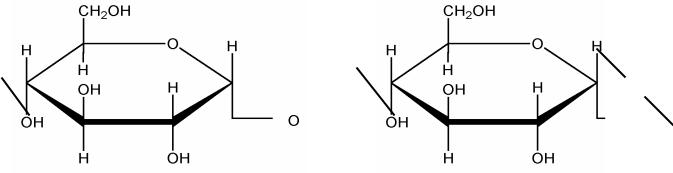
По предложению английского химика Хеуорса, полуацетальные формы моносахаридов изображают в виде перспективных форм. Углеродные атомы в этих формулах нумеруют так же, как и в оксикарбонильных. Атомы и группы при асимметричных углеродах, которые у Фишера пишут слева, в перспективных формулах ориентированы вверх от плоскости кольца, а группы, расположенные справа, в перспективных формулах направлены вниз.
ОН
Н
α-D глюкопираноза |
D-глюкоза (оксикарбонильная форма) |
β-D глюкопираноза |
О |
|
О |
|
|
|
β-D –глюкофураноза |
α-D -глюкофураноза |
12
По расположению полуацетального гидроксила относительно плоскости кольца различают α- и β-формы. α –форма для моносахаридов D –ряда считается в том случае, когда гидроксил обращен по отношению к плоскости кольца вправо ( по Хеуорсувниз), β-форма-гидроксил обращен влево от плоскости кольца ( по Хеуорсувверх).
Производные моносахаридов , образующие в результате взаимодействия полуацетального гидроксила со спиртами называются гликозидами. Гликозиды, образованные α - и β -пиранозными формами, называются α и β - пиранозидами, α и β - фуранозным формам - α и β - фуранозидами.
метил – α –D-глюкопиранозид |
этил–β –D–фруктофуранозид |
Дисахариды
Дисахариды (биозы) – это сложные углеводы (олигосахариды), молекулы которых при гидролизе распадаются на две молекулы моносахаридов.Тривиальные названия дисахаридов происходят преимущественно от названий тех продуктов, из которых впервые были выделены (тростниковый сахар, молочный сахар).
Моносахариды входят в состав дисахаридов в циклических полуацетальных формах и соединяются друг с другом в результате выделения воды за счет гидроксильных групп. В зависимости от того, какой ее гидроксилов участвует в образовании дисахарида, различают дисахариды двух типов:
а) гликозил – гликозы (восстанавливающие дисахариды), б) гликозил – гликозиды (невосстанавливающие дисахариды).
Гликозил – общее название остатков моносахаридов без полуацетального гидроксила (по аналогии с названиями “ацил”– для кислотных радикалов). Остаток глюкозы называется гликозилом, галактозы – галактозилом и т.д.
Примеры названий дисахаридов
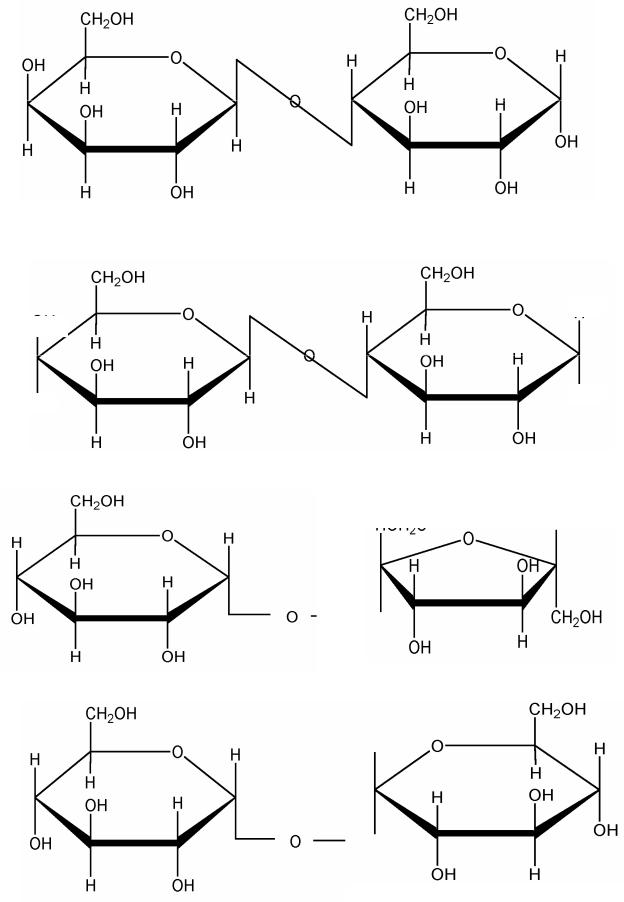
мальтоза (Т); солодовый сахар.Гликозил–глюкоза, точнее 4-(α-D глюкопиранозил)-глюкоза
13
лактоза (Т); молочный сахар,
галактозил-глюкоза, точнее 4-(β-D галактопиранозил) D-глюкоза (М)
ОН
Н
Н
ОН
целлобиоза (Т); 4(β-D глюкопиранозил) D-глюкоза (М)
НОН2С |
Н |
сахароза (Т), тростниковый сахар (Т); α-D–глюкопиранозил - β–D-фруктофуранозид (М)
Трегалоза (Т), грибной сахар (Т), α-D – глюкопиранозил– α-D глюкопиранозид (М)
14
Полисахариды
Высшие полисахариды являются высокомолекулярными веществами, по характеру связей – полигликозидами, продуктами поликонденсации моносахаридов.В природе встречаются полисахариды, образованные пентозами (пентозаны и гексозами (гексозаны). Важнейшие представители гексо- занов-крахмал, гликоген (животный крахмал),целлюлоза (клетчатка).Их молекулы построены из пиранозных звеньев D глюкозы. Для крахмала и гликогена характерна α -форма, для целлюлоз β -форма. Растворимая часть крахмала называется амилозой, нерастворимая - амилопектином.
|
|
|
|
|
|
|
|
|
|
|
О |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
n |
|
|
|
Н |
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
крахмал |
|
|
целлюлоза |
|
|
|
|
n |
||
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Азотсодержащие соединения
Амины
Амины по рациональной и по международной номенклатуре рассматривают как производные аммиака, в которых один или несколько атомов водорода замещены на углеводородные радикалы. В зависимости от количества радикалов различают амины первичные, у которых атом азота связан с одним радикалом, вторичные – с двумя радикалами, третичные –с тремя радикалами. Такая номенклатура очень удобна для обозначения так называемых моноаминов, являющихся производными только одной молекулы аммиака. Названия аминов производят указывая количество и названия радикалов и добавляя окончание –АМИН, Например:
H |
CH3 |
CH3 |
CH3 |
/ |
/ |
/ |
/ |
N – H |
N – H |
N – CH3 |
N – CH3 |
\ |
\ |
\ |
\ |
H |
H |
H |
CH3 |
аммиак |
метиламин |
диметиламин |
триметиламин |
|
(первичный) |
(вторичный) |
(третичный) |

15
Название может складываться из названия соответствующего углеводорода по международной номенклатуре с прибавлением приставки амино- и цифры, указывающей местоположение аминогруппы - NH2.
Например:
СН3 |
– СН – СН – СН3 2-метил-3-аминобутан |
|
|
|
|
|
NН2 |
СН3 |
Ди- и полиамины
Первичные диамины и полиамины рассматривают как углеводороды, в которых два или несколько атомов водорода замещены остатками аммиака или аминогруппой –NH2. В зависимости от количества аминогрупп различают также моноамины, диамины, триамины и т.д. Названия их производят, присоединяя окончание -ДИАМИН, -ТРИАМИН и т.д., либо к названию основного углеводорода, либо к названиям двух-, трех-, и поливалентных радикалов, например: –СН2–СН2– этилен, –СН2–СН2–СН2– триметилен, –СН2–СН2–СН2–СН2 – тетраметилен и т.д.
СН2 – СН2 |
СН2 – СН2 – СН2 |
|
NH2 NH2 |
NH2 |
NH2 |
этандиамин 1,2 (М) |
пропандиамин 1,3 |
|
Ароматические амины
Ароматические амины можно рассматривать как производные бензола, в которых один или несколько атомов водорода замещены на аминогруппу.
|
NH2 |
NH2 |
|
|
NH2 |
аминобензол (М) |
метадиаминобензол |
анилин (Т) |
|
Двухвалентный ароматический радикал называют фенилен. Третично-
му амину С6Н5 |
– N – СН3 |
можно дать три равнозначных названия: |
|
| |
а) диметилфениламин; |
|
СН3 |
б) N.N –диметиламинобензол; |
|
|
в) диметиланилин |

16
Аминопроизводные толуола называют толуидинами, аминопроизводные ксилола – ксилидинами. Например:
СН3 |
– |
– NH2 |
паратолуидин (Т) |
СН3 |
– |
– NH2 |
1-амино 2,4-диметилбензол |
|
|
|
|
|
|
CH3 |
|
Азотсодержащие соли и основания
Четырехзамещенные основания – производные катиона аммония рассматривают как производные либо солей, либо гидроксида аммония, в котором все четыре атома водорода замещены на радикалы, например:
[NH4]+Cl- |
[N(CH3)4]+OH |
[NH4]+OH |
[N(CH3)4]+OH- |
хлорид |
хлорид |
гидроксид |
гидроксид |
аммония |
тетраметиламмония |
аммония |
тетраметиламмония |
Диазосоединения
Ароматические диазосоединения отвечают общей формуле Ar–N2–X, где X – Cl, Br, SO4H, OH, CN и т.д. Они могут иметь вид истинных диазосоединений Ar – N = N – X или солей диазония [Ar–N+≡N]X– .
Названия солей диазония складываются из названия кислотного остатка,ароматического радикала и оканчиваются словом «диазоний», например:
– N ≡ N Cl |
HO3S |
–N ≡ N Cl |
хлорид фенилдиазония |
хлорид парасульфофенилдиазония |
|
Название диазониевого основания образуют из названия ароматического радикала, слова «диазо», заканчивают название словом «гидрат». Например,
СН3 – |
– N ≡ N OH |
HSO3 – |
–N=N–OH |
n-толлилдиазогидрат |
n-сульфобензолдиазогидрат |
||
