
Le cours 11. Lа bioénergétique
L'énergie chimique est extraite des substances, qui se trouvent dans la nourriture, et elle est utilisée pour la garantie des fonctions nécessaires de l'organisme.
L`assurance énergétique de la cellule peut se passer dans les conditions sans oxygène (l`exécution d'oxygène):
![]()
L'énergie des substances s`oxydantes est utilisée pour la synthèse de l`АТP de АDP. L`АТP – la source universelle de l'énergie dans l'organisme.

Si l'énergie, qui se libère à l'hydrolyse de la substance, excède 30 kJ/mole, la liaison hydrolisée s`appelle énergétique (macroérgique). L'énergie de l'hydrolyse de l`АТP 50 kJ/mole. La liaison macroérgique dans la formule est désigné par le signe ~ (le tilde).
L`une des voies de la synthèse de l`AТP de l`АDP – la phosphorylation du substrat (la formation de l`АТP à l`aide de l'énergie d`une autre combinaison macroérgique):
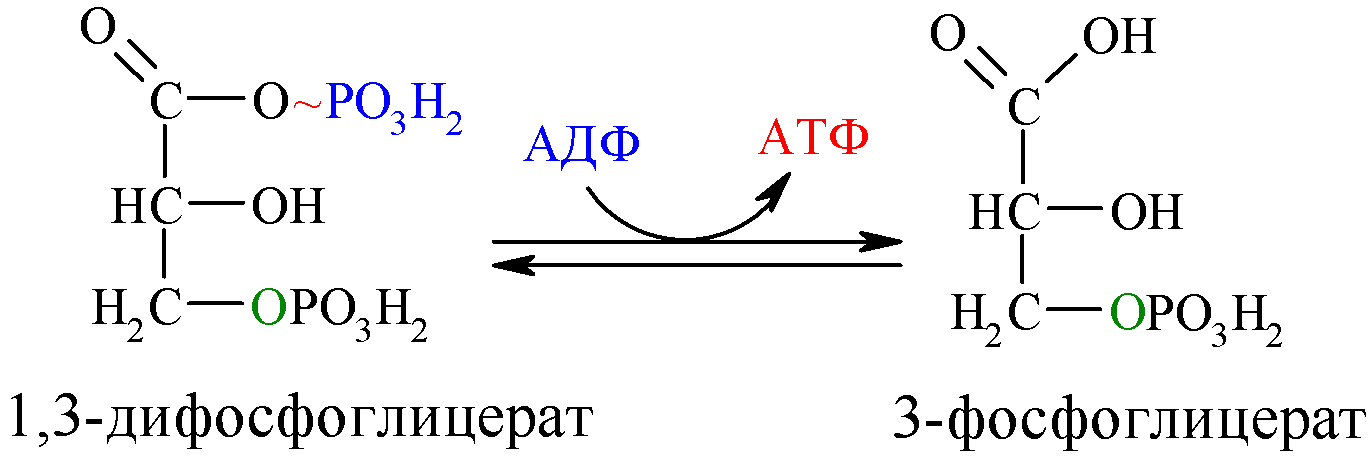
L'utilisation de l'oxygène par les cellules ouvre les possibilités pour l'oxydation plus complète des substrats.
La respiration tissulaire - l'ensemble des réactions de l'oxydation du substrat dans les cellules vivantes, accompagnées par la consommation de l'oxygène moléculaire et amenant au dégagement du gaz carbonique, l'eau et la formation des types biologiques de l'énergie.
Pour la première fois l'essence d'un phénomène de la respiration a été expliquée par Antoine Laurent de Lavoisier (1777), qui a fait attention à la ressemblance de la combustion des matières organiques en dehors de l'organisme et la respiration des animaux. Dans l'organisme l'oxydation passe à la température assez basse en présence de l'eau, et sa vitesse est réglée par le métabolisme.
Nous examinerons la réaction de l'oxydation du glucose:
![]()
Dans l'organisme ce processus passe par plusieurs stades. Le carbone se transforme au dioxyde du carbone à l`aide de l'oxygène de la substance oxydée elle-même et l'oxygène de l'eau. À la réaction participent les accepteurs de l'hydrogène, qui le transfèrent à l'oxygène. L'oxygène est utilisé pour la synthèse de l'eau à l`aide de l'hydrogène des substrats oxydés.

Par le même moyen s`oxydent d'autres substances.
Les reins, le cerveau, le foie ont la plus grande vitesse de la respiration tissulaire; la peau, le tissu musculaire (dans le repos) - la plus petite.
La voie principale de la synthèse de l`АТP de l`АDP – la phosphorylation oxydative – la synthèse de l`АТP de l`АDP et du phosphate inorganique, qui se passe grâce à l'énergie se sécrétant à l'oxydation des matières organiques en train de la respiration cellulaire, c.a.d. la conjugaison de la respiration et de la phosphorylation.
![]()
La chaîne respiratoire
L'oxydation des substrats dans le procès - le transfert des électrons et des protons des matières organiques sur l'oxygène. Une série des transporteurs intermédiaires participent au processus, en formant la chaîne respiratoire.
La chaîne respiratoire (la chaîne du transport des électrons) - le système des protéines transmembranaires et des transporteurs des électrons, qui transmettent les électrons des substrats à l'oxygène.
Dans les cellules eucaryotes la chaîne respiratoire est située dans la membrane intérieure des mitochondries.
NAD réduit sert du donneur universel des atomes de l'hydrogène pour la chaîne respiratoire. À la coopération de NAD + et NADPH + avec les atomes de l'hydrogène il y a une adjonction réversible des atomes de l'hydrogène. De plus, la molécule NAD + (NADPH +) contient 2 électrons et un proton, mais le deuxième proton reste dans le milieu:

Une autre source primaire des atomes de l'hydrogène et des électrons – c`est la flavoprotéine réduite FAD ou FMN:

Les formes réduites de ces cofacteurs sont capables de transporter l'hydrogène et les électrons vers la chaîne respiratoire des mitochondries.
Les composants de la chaîne respiratoire sont insérés à la membrane mitochondriale en forme de 4 complexes péptido-lipidiques.
Le complexe I (NADN- déshydrogénase) comprend FMN et la protéine FeS (le fer non-hèmatique). La protéine FeS participe au processus d`oxydo-réduction. Le complexe I oxyde NADN, en transférant de lui 2 électrons sur KoQ (l`ubiquinone). Le complexe I pompe 4 protons du matrixe à l'espace intermembranaire de la mitochondrie.
KoQ (l`ubiquinone) – le dérivé du benzoquinone. C'estla moléculemoyenne lipophile. En se déplaçant dans la couche lipidique de la membrane, l`ubiquinone assure la transmission des électrons entre les complexes I - III et II - III.
Le complexe II (succinate-déshydrogénase) comprend FAD et la protéine FeS. Assure l'entrée à la chaîne des électrons supplémentaires pour le compte de l'oxydation du succinate.
Le complexe III (QН2- déshydrogénase) compred les cytochromes b, с1, et la protéine FeS. Le complexe III transfère les électrons de l`ubiquinone sur le cytochrome avec et pompe 2 protons à l'espace intermembranaire.
Le complexe IV (le cytochrome c - oxydase) comprend les cytochromes a et a3, qui, à part de l`hème, contiennent les ions du cuivre. Le complexe IV catalyse le transfert des électrons des molécules du cytochrome sur O2, et pompe 4 protons à l'espace intermembranaire.
Le cytochrome а3 représente le terrain terminal de la chaîne respiratoire - cytochromeoxydase, qui réalise l'oxydation du cytochrome c et la formation de l'eau. Dans l'organisme de l`homme la chaîne respiratoire mitochondriale forme 300-400 ml de l'eau par jour (l'eau métabolique).
Les composants de la chaîne respiratoire des mitochondries sont rangés en ordre de la diminution du potentiel d'oxydoréduction.
Le déplacement des électrons se passe par le gradient du potentiel d'oxydoréduction et est la source de l'énergie pour le transfert des protons. Le transfert de deux électrons à travers tous les complexes assure le transfert de quatre protons.
Finalement de tous les côtés de la membrane il y a une différence des concentrations des protons et la différence des potentiels électriques avec le signe «plus» sur la surface extérieure. Le potentiel électrochimique incite les protons à avancer dans le sens inverse - de la surface extérieure à l'intérieur. Cependant la membrane leur est imperméable, à l'exception des terrains, où s'installe l`enzyme ATP- synthase de proton. Elle comprend deux parties – le stator et le rotor.
Le stator comprend trois α – sous-unités et 3 β - sous-unités – elles participent directement à la synthèse de l`АТP de l`АDPH et le phosphate. Leur adhère δ - sous-unité, et tous ensemble ils forment F1- sous-unité.
Le stator se tient dans la membrane, mais le rotor tourne aux frais de l'énergie des protons.
Le rotor se compose de - et - sous-unités.
Le stator se tient dans la membrane, et le rotor tourne à l`aide de l'énergie des protons.
Dans le stator il y a un canal de proton (F0). Il comprend deux semi-canaux, qui sont déplacés l`un par rapport à l'autre. Le proton passe une moitié du canal, puis sur le rotor tournant se trouve dans la deuxième moitié du canal. La différence des potentiels électrochimiques, qui apparaît au mouvement des protons à travers le canal met en marche l`ATP- synthase, qui catalyse la réaction:
![]()
La conception chémiosmotique de la transformation de l'énergie dans les cellules vivantes était proposée par P. Mitchell en 1960 pour l'explication du mécanisme moléculaire de la conjugaison du transport des électrons et la formation de l`АТP dans la chaîne respiratoire. Pour les recherches dans le domaine de la bioénergétique P. Mitchell en 1978 a reçu le prix Nobel.
Dans la chaîne respiratoire il y a seulement 3 terrains, où le transfert des électrons est associé avec l'accumulation de l'énergie, suffisant pour la formation de l`АТP.
Le coefficient de phosphorylation – le rapport de la valeur de l`ATP formé à l'oxygène absorbé : ATP/O ou Р/О.
La valeur maxima du coefficient de phosphorylation est 3, si la réaction de l'oxydation passe avec la participation de NAD; et 2, si l'oxydation du substrat passe par FAD. Les valeurs réellement reçues sont plus petites (2,5 et 1,5). C.a.d. le procès de la respiration n'est pas entièrement associé avec la phosphorylation. Le degré de la conjugaison dépend de l'intégrité de la membrane mitochondriale.
L`ATP formée avec la participation de ADP-ATP-translocase est transporté de matrixe sur la partie extérieure de la membrane et se trouve au cytosole. Simultanément même translocase transfère l`АDPH dans la direction inverse.
Le contenu total de l`АТP dans l'organisme 30-50 gr, mais la durée de vie de la molécule de l`АТP est moins qu`une minute. 40-60 kg de l`АТP est synthétisé chez l`homme par jour et autant se désagrège.
A chaque contraction du myocarde se dépense près de 2 % de l`ATP qui y se trouve. Tout l`АТP serait dépensé pendant 1 minute, s'il n'y avait pas de régénérescence. À la formation du thrombus dans l'artère coronaire l'entrée de l'oxygène aux cellules cesse, en conséquence la régénérescence de l`АТP cesse aussi, et les cellules périssent (l'infarctus du myocarde).
L'augmentation de la concentration de l`АDP amène à l'accélération de la respiration et la phosphorylation.
La dépendance de l'intensité de la respiration des mitochondries de la concentration de l`АDPH s`appelle le contrôle respiratoire.
Pour l`évaluation de l'influence des nucléotides adénylés aux processus du métabolisme, on utilise la charge énergétique de la cellule (ECC):
![]()
Dans la norme ECC=0,7-0,8: la vitesse de la formation de l`ATP est égale à la vitesse de son emploie, le système adénylique est saturé de l'énergie.
À la ECC <0,7 la formation de l`АТP s'accélère par voie de l`augmentation de vitesse des réactions de la voie totale du catabolisme.
Si ECC=1, les processus de la synthèse de l`ATP sont freinés, et son utilisation s'accélère.
Les états hypoénergétiques se subdivisent en:
- аlimentaires (le jeûne, l'avitaminose);
- hypotoxiques:
- Les troubles de l'entrée de l'oxygène au sang (l'hypoxie pulmonaire),
- Les troubles du transport de l'oxygène aux tissus - hémodynamique (la perte sanguine, le choc, l`affection valvulaireles) et hémoglobinique (la pathologie de l'hémoglobine, le blocage par les poisons, l'hypoxie),
- mitochondriales (la difficulté de l'utilisation de l'oxygène dans les cellules) – les troubles des fonctions des mitochondries par les inhibiteurs des enzymes de la chaîne respiratoire, les découpleurs de l`oxydation et de phosphorylation, les substances membranotropes.
Au jeûne complet les réserves alimentaires de l'organisme sont suffisants pour quelques semaines, et l'oxygène - pour 2-3 minutes. L'hypoxie - la raison la plus fréquente des états hypoénergétiques, et l'hypoxie du cerveau - la raison directe de la mort. C'est pourquoi parmi les procédures de réanimation la place principale est prise par les mesures dirigées à la réactivation de l'approvisionnement des organes par l'oxygène.
