
Молекулярная физика и термодинамика
Методические указания по решению задач
Омск 2004
Составители:
Ласица Александр Михайлович;
Кондратьева Тамара Николаевна;
Павловская Ольга Юрьевна.
Печатается по решению редакционно-издательского совета Омского государственного технического университета.
Молекулярная физика и термодинамика – разделы физики, в которых изучаются макроскопические процессы, связанные с огромным числом содержащихся в телах атомов и молекул. Для исследования этих процессов применяются два качественно различных метода: статистический и термодинамический. Первый лежит в основе молекулярной физики, второй – термодинамики.
Основные положения молекулярной физики
Молекулярная физика – раздел физики, изучающий строение и свойства вещества, исходя из молекулярно–кинетических представлений, основывающихся на том, что все тела состоят из молекул, находящихся в непрерывном движении.
Наиболее полное описание любой системы состояло бы в определении уравнений движения всех тел, входящих в нее, однако из-за большого числа частиц входящих в макроскопическую систему, данная задача является принципиально неразрешимой. Состояние системы в молекулярной физике определяется небольшим набором величин, называемых параметрами состояния (термодинамическими параметрами) характеризующих свойства системы в целом. В качестве основных параметров состояния выбирают температуру Т, давление р и объем V. Если система находится во внешнем поле, то к параметрам состояния добавляются характеристики поля.
Параметры состояния в большинстве случаев не являются независимыми, они связаны между собой некоторым уравнением, называемым уравнением состояния. Одной из основных задач молекулярной физики является установление явного вида уравнения состояния и установление связи между параметрами состояния и усредненными характеристиками движения частиц, входящих в систему. Для решения такой задачи приходится прибегать к рассмотрению различных физических моделей вещества. Одной из самых простых моделей является модель идеального газа.
Идеальным называют газ, удовлетворяющий следующим условиям:
-
собственный объем молекул газа пренебрежимо мал по сравнению с объемом сосуда;
-
потенциальной энергией взаимодействия молекул можно пренебречь;
-
столкновения молекул между собой и со стенками сосуда абсолютно упругие.
Модель идеального газа можно использовать при изучении реальных газов, так как в условиях, близких к нормальным, а также при низких давлениях и высоких температурах они близки к идеальному газу. Кроме того, внеся поправки на собственный размер молекул и действующие молекулярные силы, можно перейти к теории реальных газов.
Уравнение состояния идеального газа носит название уравнение Менделеева -Клапейрона и имеет вид
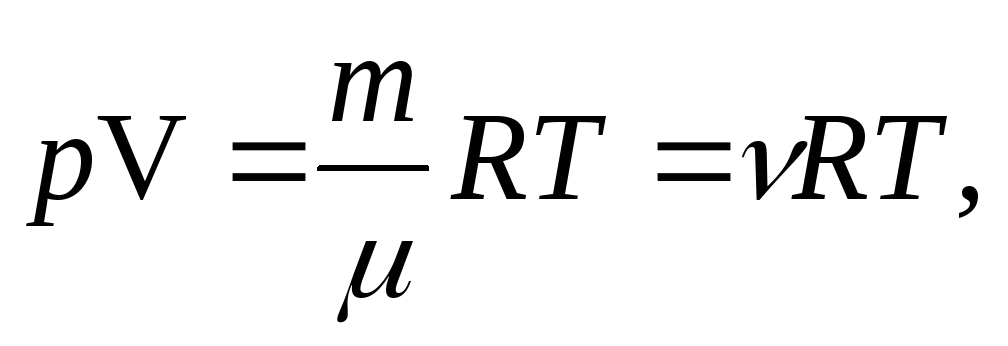
где =m/число молей газа, R=8,31 Дж/(мольК)универсальная газовая постоянная. Данное уравнение является обобщением установленных экспериментально законов поведения идеального газа к которым относятся законы:
-
Бойля-Мариотта: pV = const при Т, m = const;
-
Шарля:
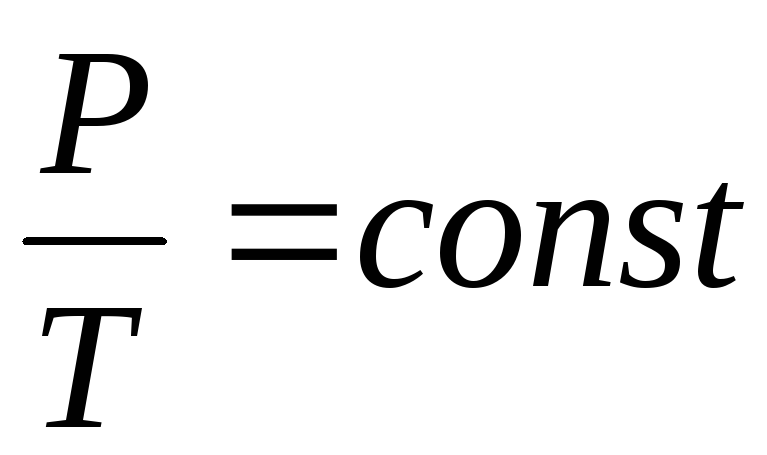 при V,
m=const;
при V,
m=const; -
Гей-Люссака:
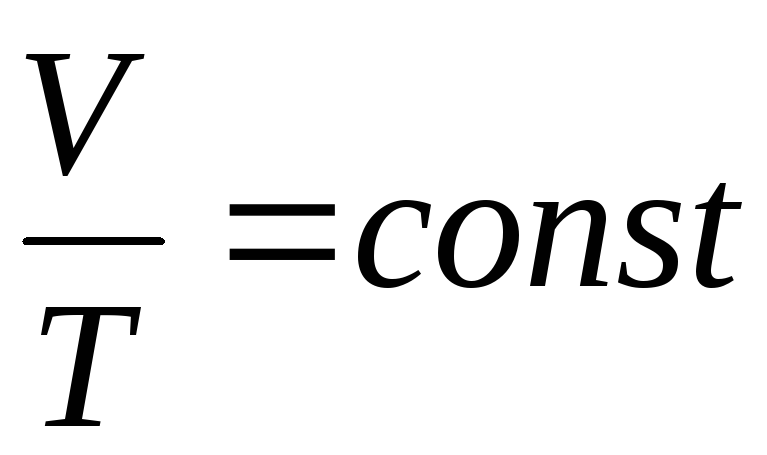 при P,
m=const;
при P,
m=const; -
Дальтона давление смеси идеальных газов равно сумме парциальных давлений входящих в нее газов:
p = p1 + p2 + p3 +,
(р1, р2,…- парциальные давления – давления, которые оказывали бы газы смеси, если бы они одни занимали объем, равный объему смеси при той же температуре);
-
Авогадро - моли любых газов при одинаковых температуре и давлении занимают одинаковые объемы (при нормальных условиях p = 1,013105 Па, Т = 273,15 К, для одного моля этот объем V = 22,4110-3 м3).
По определению, в одном моле различных веществ содержится одно и то же число молекул, называемое постоянной Авогадро: NA = 6,0221023 моль-1.
Уравнение Менделеева - Клапейрона может быть переписано в другом виде:
![]() ,
,
где
n
– концентрация молекул газа,![]() –
постоянная Больцмана.
–
постоянная Больцмана.
Основным уравнением молекулярно кинетической теории идеального газа называется уравнение связывающее давление, оказываемое идеальным газом на стенки сосуда с характеристиками его молекул:
![]()
(m0
– масса молекулы газа;
![]() - средняя квадратичная скорость молекул,
- средняя квадратичная скорость молекул,
![]() -средняя
кинетическая энергия поступательного
движения одной молекулы).
Принимая во внимание уравнение
Менделеева–Клапейрона, получаем
-средняя
кинетическая энергия поступательного
движения одной молекулы).
Принимая во внимание уравнение
Менделеева–Клапейрона, получаем
![]() .
.
Средняя кинетическая энергия поступательного движения одной молекулы идеального газа пропорциональна термодинамической температуре и зависит только от нее.
Более детальное описание системы заключается в определении не только средней скорости, но и закона распределения молекул по скоростям. Этот закон теоретически выведен Максвеллом. Закон Максвелла описывается некоторой функцией f(), называемой функцией распределения молекул по скоростям. Если разбить диапазон скоростей молекул на малые интервалы, то на каждый интервал скорости будет приходиться некоторое число молекул dN(), имеющих скорости в интервале от до +d , пропорциональное ширине интервала d.
![]() и
и
![]() ,
где N – число молекул
газа.
,
где N – число молекул
газа.
Таким образом,
функция f()
определяет относительное число молекул
![]() ,
скорости которых лежат в интервале от
до +d.
Можно также сказать, что функция f()
определяет вероятность попадания
скорости молекулы в интервал от
до +d.
,
скорости которых лежат в интервале от
до +d.
Можно также сказать, что функция f()
определяет вероятность попадания
скорости молекулы в интервал от
до +d.
![]() .
.
Г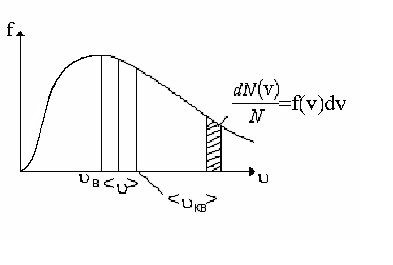 рафик
функции представляет собой немонотонную
кривую обращающуюся в ноль при
= 0 и = .
При увеличении температуры максимум
функции распределения становится более
пологим и смещается в область больших
скоростей. Скорость при которой
достигается максимум функции распределения
называется наиболее вероятной скоростью
В.
Этой скоростью и близкой к ней обладает
наибольшее число молекул. Кривая
несимметрична относительно В.
Расчеты показывают, что
рафик
функции представляет собой немонотонную
кривую обращающуюся в ноль при
= 0 и = .
При увеличении температуры максимум
функции распределения становится более
пологим и смещается в область больших
скоростей. Скорость при которой
достигается максимум функции распределения
называется наиболее вероятной скоростью
В.
Этой скоростью и близкой к ней обладает
наибольшее число молекул. Кривая
несимметрична относительно В.
Расчеты показывают, что
![]() .
.
С помощью функции распределения можно установить среднее значение любой величины X зависящей от скорости
![]()
Например, среднее значение скорости
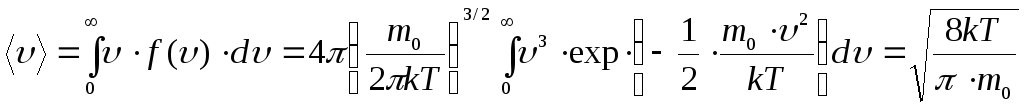 ,
,
среднее значение квадрата скорости
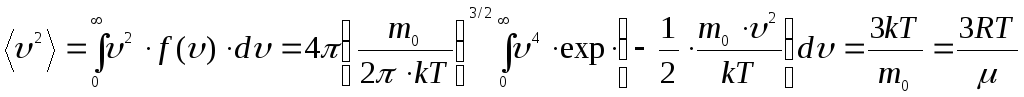 .
.
Если газ находится в поле внешних сил, то кроме распределения по скоростям устанавливается распределение по координатам. В случае поля тяготения Земли это приводит к тому, что концентрация молекул и давление газа изменяются с высотой. Закон изменения установлен Больцманом для изотермической атмосферы:
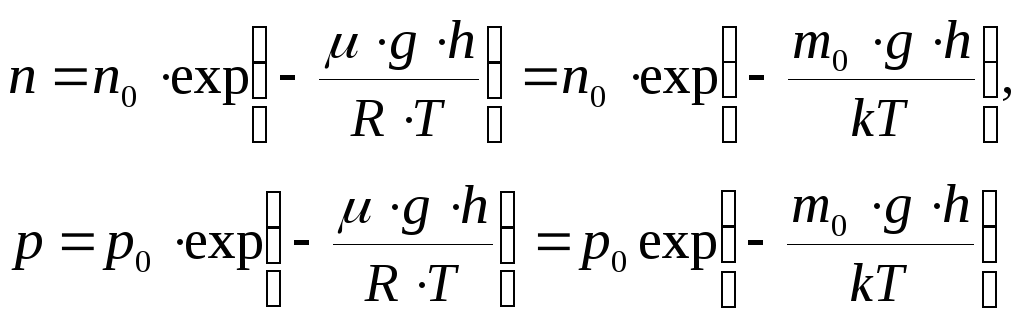
где p0 и n0-давление и концентрация молекул на высоте h = 0. Первая из формул называется распределением Больцмана, вторая - барометрической формулой.
Молекулы газа,
находясь в состоянии хаотического
движения, непрерывно сталкиваются друг
с другом. Между двумя последовательными
столкновениями молекулы проходят
некоторый путь ,
который называется длиной свободного
пробега. В общем случае длина пути между
последовательными столкновениями
различна, поэтому можно говорить о
средней длине свободного пробега молекул
<
>. За
единицу времени молекула проходит путь,
равный <>
и, если <z>
- среднее число столкновений за единицу
времени, то
![]() .Расчеты
показывают, что
.Расчеты
показывают, что
![]()
(d эффективный диаметр молекулы).
В термодинамически неравновесных системах возникают особые необратимые процессы, называемые явлениями переноса, в результате которых происходит пространственный перенос энергии (теплопроводность), массы (диффузия), импульса (внутреннее трение). Уравнения, описывающие явления переноса называются:
-
законом теплопроводности Фурье:
![]()
(![]() коэффициент
теплопроводности, сV
удельная теплоемкость при постоянном
объеме),
коэффициент
теплопроводности, сV
удельная теплоемкость при постоянном
объеме),
-
законом диффузии Фика:
![]()
(![]()
коэффициент диффузии),
коэффициент диффузии),
-
законом внутреннего трения Ньютона:
![]()
(![]() коэффициент
внутреннего трения (вязкость)).
коэффициент
внутреннего трения (вязкость)).
Знак минус в уравнениях показывает, что перенос энергии, массы и импульса идет в направлении противоположном направлению возрастания температуры, плотности и скорости соответственно. Коэффициенты , D и связаны простыми соотношениями:
![]()
