
- •Связь линейных и угловых характеристик движения:
- •2) Инерциальные системы отсчета. Понятия силы и инертной массы. Законы динамики. Силы в природе. Фундаментальные взаимодействия. Свойства сил упругости и тяготения. Свойства сил трения.
- •3) Центр инерции. Закон сохранения импульса системы материальных точек.
- •4) Работа переменной силы. Кинетическая энергия и ее связь с работой внешних и внутренних сил.
- •6) Закон сохранения механической энергии. Диссипация энергии.
- •Работа при вращении твердого тела ()
- •8)Колебания математического и физического маятников.
- •9) Преобразования Галилея. Механический принцип относительности. Нарушение классического закона сложения скоростей. Опыты по определению скорости света. Опыт Майкельсона.
- •11) Статистический и термодинамический методы исследования. Термодинамические параметры. Идеальный газ. Термодинамическая система. Равновесные и неравновесные состояния и процессы.
- •Термодинамические параметры: объём , температура , давление и масса , концентрации составляющих систему веществ , химические потенциалы составляющих веществ , внутренняя энергия , энтропия .
- •12. Среднеквадратичная скорость молекул. Молекулярно-кинетическое толкование абсолютной температуры.
- •13. Основное уравнение молекулярно-кинетической теории (вывод). Число степеней свободы молекулы. Закон распределения энергии по степеням свободы. Внутренняя энергия идеального газа.
- •14. Работа газа при расширении. Количество теплоты. Первое начало термодинамики.
- •15. Классическая молекулярно-кинетическая теория теплоемкости. Удельная и молярная теплоемкости. Формула Майера. Границы применимости теории.
- •Формула Майера ()
- •16. Изопроцессы идеального газа. Зависимость теплоемкости от вида процесса. Адиабатический процесс.
- •17. Тепловые двигатели и холодильные машины. Кпд. Обратимые и необратимые процессы. Круговой процесс. Цикл Карно для идеального газа и его кпд.
- •19. Закон Максвелла для распределения молекул идеального газа по скоростям теплового движения. Вероятностное толкование закона распределения Максвелла.
- •20. Барометрическая формула. Закон Больцмана для распределения частиц идеального газа во внешнем потенциальном поле.
- •Одной молекулы газа
- •Потенцирование:
- •21. Среднее число столкновений и средняя длина свободного пробега молекул идеального газа. Эффективный диаметр молекулы.
- •22. Явления переноса. Теплопроводность, диффузия, вязкость.
- •23. Реальные газы. Силы и потенциальная энергия межмолекулярного взаимодействия. Уравнение Ван-дер-Ваальса. Изотермы реального газа. Критическое состояние. (Внутренняя энергия реального газа.)
- •Уравнение Ван-дер-Ваальса – уравнение, связывающее основные термодинамические величины в модели газа Ван-дер-Ваальса.
14. Работа газа при расширении. Количество теплоты. Первое начало термодинамики.
Работа газа при расширении
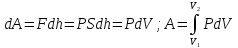
При изохорном процессе
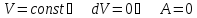 ;
;
При изобарном процессе
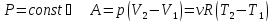 ;
;
При изотермическом процессе
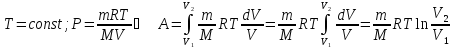 ;
;
При адиабатическом процессе

Количество теплоты [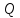 ]=[Дж]
– энергия, которую получает или теряет
тело при теплопередаче.
]=[Дж]
– энергия, которую получает или теряет
тело при теплопередаче.
Первое начало термодинамики:

15. Классическая молекулярно-кинетическая теория теплоемкости. Удельная и молярная теплоемкости. Формула Майера. Границы применимости теории.
Теплоемкость ( )
[Дж/К] – величина, равная отношению
количеству тепла
)
[Дж/К] – величина, равная отношению
количеству тепла
 ,
сообщенного системе, к изменению
температуры системы
,
сообщенного системе, к изменению
температуры системы
 .
.
Удельная теплоёмкость (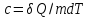 )
[Дж/кг*К] – это отношение теплоёмкости
к массе.
)
[Дж/кг*К] – это отношение теплоёмкости
к массе.
Молярная теплоёмкость (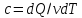 )
[Дж/моль*К] – отношение теплоёмкости к
количеству вещества.
)
[Дж/моль*К] – отношение теплоёмкости к
количеству вещества.
Формула Майера ()
Границы применимости:
для 1-атомных
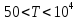 ,
когда начинается ионизация атомов;
,
когда начинается ионизация атомов;
для 2-атомных от
 .
При
.
При
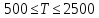 теплоемкость медленно растет и при
теплоемкость медленно растет и при
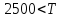 обращается в бесконечность. При этой
температуре наступает диссоциация
двухатомных молекул на отдельные атомы.
Тепло расходуется на совершение работы
по разрыву межатомных связей. После
диссоциации молярная теплоемкость
двухатомного газа переходит в молярную
теплоемкость одноатомного газа с
удвоенным числом частиц.
обращается в бесконечность. При этой
температуре наступает диссоциация
двухатомных молекул на отдельные атомы.
Тепло расходуется на совершение работы
по разрыву межатомных связей. После
диссоциации молярная теплоемкость
двухатомного газа переходит в молярную
теплоемкость одноатомного газа с
удвоенным числом частиц.
У двухатомных газов при
 теплоемкость падает до
теплоемкость падает до
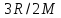 .
При
.
При
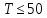 теплоемкость всех газов с понижением
температуры быстро убывает и при
теплоемкость всех газов с понижением
температуры быстро убывает и при
 стремится к нулю.
стремится к нулю.
16. Изопроцессы идеального газа. Зависимость теплоемкости от вида процесса. Адиабатический процесс.
Изопроцессы:
изотермический (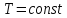 ),
изохорический (
),
изохорический (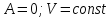 ),
изобарический (
),
изобарический (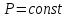 )
и адиабатический (
)
и адиабатический (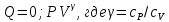 ).
).
Зависимость
теплоемкости от вида процесса:

17. Тепловые двигатели и холодильные машины. Кпд. Обратимые и необратимые процессы. Круговой процесс. Цикл Карно для идеального газа и его кпд.
Тепловой двигатель – машина, в которой внутренняя энергия топлива превращается в механическую энергию.
Холодильная машина – устройство, служащее для отвода теплоты от охлаждаемого тела при температуре более низкой, чем температура окружающей среды.
КПД ( )
– характеристика эффективности системы
(устройства, машины) в отношении
преобразования или передачи энергии.
)
– характеристика эффективности системы
(устройства, машины) в отношении
преобразования или передачи энергии.
Обратимый процесс – равновесный термодинамический процесс, который может проходить как в прямом, так и в обратном направлении, проходя через одинаковые промежуточные состояния, причем система возвращается в исходное состояние без затрат энергии, и в окружающей среде не остается макроскопических изменений.
Круговые процессы в термодинамике – такие процессы, в которых начальные и конечные параметры, определяющие состояние рабочего тела, совпадают.
Цикл Карно – это идеальный круговой
процесс, состоящий из двух адиабатических
и двух изотермических процессов. В цикле
Карно термодинамическая система
выполняет механическую работу за счёт
теплообмена с двумя тепловыми резервуарами.
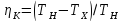
18. Второе начало термодинамики. Вечный двигатель второго рода. Статистическое толкование второго начала термодинамики. Энтропия в термодинамике. Изменение энтропии при изопроцессах. Статистическое толкование энтропии.
Второе начало термодинамики (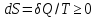 )
устанавливает существование энтропии
как функции состояния термодинамической
системы и вводит понятие абсолютной
термодинамической температуры. В
изолированной системе энтропия остаётся
либо неизменной, либо возрастает (в
неравновесных процессах), достигая
максимума при установлении термодинамического
равновесия (закон возрастания энтропии).
Второе начало термодинамики определяет
направление процессов, происходящих в
природе и связанных с превращением
энергии.
)
устанавливает существование энтропии
как функции состояния термодинамической
системы и вводит понятие абсолютной
термодинамической температуры. В
изолированной системе энтропия остаётся
либо неизменной, либо возрастает (в
неравновесных процессах), достигая
максимума при установлении термодинамического
равновесия (закон возрастания энтропии).
Второе начало термодинамики определяет
направление процессов, происходящих в
природе и связанных с превращением
энергии.
Формулировки постулата второго начала термодинамики:
-
Теплота не может переходить самопроизвольно от более холодного тела к более тёплому. (Постулат Клаузиуса)
-
Невозможно построить периодически действующую машину, вся деятельность которой сводится к поднятию тяжести и к охлаждению теплового резервуара. (Постулат Томсона (Кельвина) в формулировке М. Планка)
Термодинамическая энтропия [S]=[Дж/K] – физическая величина, функция состояния, используемая для описания термодинамической системы, одна из основных термодинамических величин.
Вечный двигатель второго рода – воображаемое неограниченно долго действующее устройство, позволяющее получать тепло от одного резервуара и полностью превращать его в работу.
Каждый из изопроцессов идеального газа
характеризуется своим изменением
энтропии
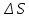 ,
а именно:
,
а именно:
-
изохорический:
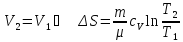 ;
; -
изобарический:
 ;
; -
изотермический:
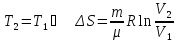 ;
; -
адиабатический:
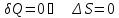 .
.
Адиабатический процесс называют
изоэнтропийным процессом, т.к.
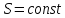 .
Изменение энтропии
.
Изменение энтропии
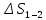 идеального газа при переходе его из
состояния 1 в состояние 2 не
зависит от вида перехода 1–2.
идеального газа при переходе его из
состояния 1 в состояние 2 не
зависит от вида перехода 1–2.
Статистический смысл энтропии
состоит в том, что увеличение энтропии
изолированной системы связано с переходом
этой системы из менее вероятного
состояния в более вероятное. Связь
энтропии с термодинамической вероятностью
установил Больцман:
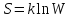 ,
где
,
где
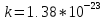 [Дж/К] ─ постоянная Больцмана,
[Дж/К] ─ постоянная Больцмана,
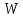 ─ число различных микросостояний,
соответствующих данному макроскопическому
состоянию
─ число различных микросостояний,
соответствующих данному макроскопическому
состоянию
