
- •Уфимский государственный нефтяной технический университет
- •1 Теоретические основы общей химии
- •Химическая кинетика и равновесие
- •Лабораторная работа
- •Контрольные вопросы
- •Гидролиз солей
- •Лабораторная работа
- •3.1 Окислительно-восстановительные
- •Лабораторная работа
- •Контрольные вопросы
- •1.4 Комплексные соединения
- •Лабораторная работа
- •Опыт 2. Получение гидроксокомплексов
- •Контрольные вопросы
- •1.5 Коррозия металлов
- •Лабораторная работа
- •Контрольные вопросы
- •2 Химия элементов
- •2.1 Подгруппа меДи
- •Лабораторная работа
- •Контрольные вопросы
- •2.2 Алюминий
- •Лабораторная работа
- •Контрольные вопросы
- •2.3 Азот
- •Лабораторная работа
- •Контрольные вопросы
- •2.4 Сера
- •Лабораторная работа
- •Контрольные вопросы
- •2.5 Галогены
- •Лабораторная работа
- •Контрольные вопросы
- •Список рекомендуемой литературы
- •Содержание
- •Редактор л.А. Матвеева
- •450062, Рб, г. Уфа, ул. Космонавтов,1.
МИНИСТЕРСТВО ОБРАЗОВАНИЯ И НАУКИ РОССИЙСКОЙ ФЕДЕРАЦИИ
ГОСУДАРСТВЕННОЕ ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ
ВЫСШЕГО ПРОФЕССИОНАЛЬНОГО ОБРАЗОВАНИЯ
Уфимский государственный нефтяной технический университет
Лабораторный практикум по общей
и неорганической химии
для студентов специальности 320700
«Охрана окружающей среды и рациональное использование
природных ресурсов»
Уфа 2004
В учебно-методическом пособии кратко описаны кинетика химических реакций, гидролиз растворов, комплексные соединения, окислительно-восстановительные и электрохимические процессы; приведены обзор свойств некоторых химических элементов и их соединений, а также руководство к выполнению лабораторных работ по данным темам. Пособие предназначено для студентов специальности 320700 «Охрана окружающей среды и рациональное использование природных ресурсов».
Составитель Бахонина Е.И., ассистент
Рецензент Елхова В.Д., доц., канд. техн. наук
ÓУфимский государственный нефтяной технический университет, 2004
1 Теоретические основы общей химии
-
Химическая кинетика и равновесие
Химическая кинетика – раздел химии, задача которого – объяснение качественных и количественных изменений химических процессов, происходящих во времени.
Основным понятием в химической кинетике является понятие о скорости химической реакции:
Скорость химической реакции определяется количеством вещества, прореагировавшего в единицу времени в единице объема.
Если при неизменных объеме и температуре концентрация одного из реагирующих веществ уменьшилась от с1 до с2 за промежуток времени от t1 до t2, то в соответствии с определением скорость реакции равна
= -(c2-c1)/(t2-t1) = - c/t.
Знак «-» в правой части уравнения обозначает следующее. По мере протекания реакции (t2-t1 > 0) концентрация реагентов убывает, следовательно, с2-с1<0, а так как скорость реакции всегда положительна, то перед дробью следует поставить знак «-».
Обычно концентрации реагентов выражают в моль/л, а скорость реакции – в моль/(л.с).
Скорость реакции зависит от природы реагирующих веществ и от условий, в которых реакция протекает. Важнейшим из них являются: концентрация. Температура и присутствие катализатора. Природа реагирующих веществ оказывает решающее влияние на скорость реакции. Так, например, водород с фтором реагирует очень энергично уже при комнатной температуре, тогда как с иодом значительно медленнее даже при нагревани и.
Количественно зависимость между скоростью реакции и молярными концентрациями реагирующих веществ описывается основным законом химической кинетики – законом действующих масс.
Скорость химической реакции при постоянной температуре пропорциональна произведению концентраций реагирующих веществ.
Для реакции, записанной в общем виде
a A
+ bB cC + dD + …,
A
+ bB cC + dD + …,
в соответствии с законом действующих масс зависимость скорости от концентрации реагирующих веществ может быть представлена в виде
= k[A]A[B]B. [1]
Здесь k – коэффициент, не зависящий от концентрации, называемый константой скорости; A и B – постоянные числа, называемые показателями порядка реакции по реагентам А и В. Сумма А+В= называется суммарным (общим) порядком реакции.
Зависимость типа [1] строго справедлива для газов или жидких веществ (гомогенные системы) и не распространяется на реакции с участием твердых веществ (гетерогенные системы). Скорость гетерогенной реакции зависит не только от рассмотренных выше факторов, но и от величины поверхности соприкосновения между реагирующими веществами. Всякое увеличение поверхности приводит к увеличению скорости реакции.
Для приближенной оценки изменения скорости широко используется температурный коэффициент скорости реакции Вант-Гоффа . Этот коэффициент показывает, во сколько раз изменяется скорость реакции при изменении температуры на определенную величину Т. В большинстве случаев при повышении температуры на 10 о скорость гомогенной реакции увеличивается в 2-4 раза (правило Вант-Гоффа), т.е.
=kт+10/kт.
Одно из наиболее сильных средств влияния на скорость реакции - присутствие в реагирующей системе катализатора.
Катализатором называется вещество, изменяющее скорость химической реакции, но остающееся неизменным после того, как химическая реакция заканчивается.
Влияние катализаторов на скорость реакции называется катализом. Когда реагенты и катализатор находятся в одном агрегатном состоянии, говорят о гомогенном катализе. При гетерогенном катализе реагенты и катализатор находятся в различных агрегатных состояниях: обычно катализатор – в твердом, а реагирующие вещества – в жидком или газообразном ( например, в случае окисления SO2 в SO3 в присутствии оксида ванадия (V) происходит гетерогенный катализ).
Механизм действия катализаторов является очень сложным. Основная гипотеза, объясняющая катализ, - предположение об образовании промежуточных продуктов при взаимодействии катализатора и реагирующего вещества. Если реакция А + В = АВ без катализатора происходит медленно, то при прибавлении катализатора К он реагирует с одним из исходных веществ, образуя непрочное и очень реакционноспособное промежуточное соединение АК (или ВК):
А(В) + К = АК(ВК).
Промежуточное соединение АК взаимодействует с другим исходным веществом В, образуя конечный продукт реакции АВ и выделяя катализатор в первоначальном виде:
АК + В = АВ + К.
О
t братимые
и необратимые реакции. Состояние
химического равновесия.
Необратимыми
реакциями
называют такие реакции, продукты которых
не взаимодействуют друг с другом с
образованием исходных веществ. Например:
братимые
и необратимые реакции. Состояние
химического равновесия.
Необратимыми
реакциями
называют такие реакции, продукты которых
не взаимодействуют друг с другом с
образованием исходных веществ. Например:
2 KCIO3
2KCI + 3O2
.
KCIO3
2KCI + 3O2
.
Необратимые реакции, как правило, «доходят до конца», т.е. до полного израсходования хотя бы одного из исходных веществ.
Химические реакции, которые при одних и тех же условиях могут идти в противоположных направлениях, называются обратимыми.
Н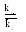 апример:
апример:
H2 + I2 2HI
Реакцию, протекающую слева направо, называют прямой (константа скорости прямой реакции k1), справа налево – обратной (константа скорости обратной реакции k2).
В обратимых реакциях скорость прямой реакции вначале имеет максимальное значение, а затем уменьшается вследствие уменьшения концентрации исходных веществ. И наоборот, обратная реакция в начальный момент имеет минимальную скорость, которая увеличивается по мере нарастания концентрации продуктов реакции. Наконец, наступает такой момент, когда скорости прямой и обратной реакции становятся равными.
Состояние, в котором скорость обратной реакции становится равной скорости прямой реакции, называется химическим равновесием.
С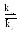 остояние
химического равновесия обратимых
процессов количественно характеризуется
константой
равновесия.
Так, для обратимой реакции, которую в
общем виде можно записать как
остояние
химического равновесия обратимых
процессов количественно характеризуется
константой
равновесия.
Так, для обратимой реакции, которую в
общем виде можно записать как
mA + nB pC + qD
согласно закону действующих масс скорости прямой реакции V1 и обратной V2 соответственно запишутся следующим образом:
V1 = k1[A]m[B]n,
V2 = k2[C]p[D]q.
В момент достижения состояния химического равновесия скорости прямой и обратной реакции равны, т.е.
k1[A]m[B]n = k2[C]p[D]q,
или
K = k1/k2 = ([C]p[D]q /([A]m[B]n),
где К – константа равновесия, представляющая собой отношение констант скорости прямой и обратной реакций. В правой части уравнения стоят те концентрации взаимодействующих веществ, которые устанавливаются при равновесии – равновесные концентрации.
Принцип Ле-Шателье (смещения равновесия). Состояние химического равновесия при неизменных внешних условиях теоретически может сохраняться бесконечно долго. В реальной действительности, при изменении температуры, давления или концентрации реагентов, равновесие может «сместиться» в ту или иную сторону протекания реакции.
Изменения, происходящие в системе в результате внешних воздействий, определяются принципом подвижного равновесия – принципом Ле-Шателье.
Внешнее воздействие на систему, находящуюся в состоянии равновесия, приводит к смещению этого равновесия в направлении, при котором эффект произведенного воздействия ослабляется.
Принцип Ле-Шателье универсален, так как применим не только к химическим процессам, но и к физическим, таким, как плавление, кипение и т.д.
Применительно к трем основным типам внешнего воздействия – изменению концентрации, температуры и давления – принцип Ле-Шателье трактуется следующим образом:
1. При увеличении концентрации одного из реагирующих веществ равновесие смещается в сторону расхода этого вещества, при уменьшении концентрации равновесие смещается в сторону образования этого вещества.
2. При увеличении давления равновесие смещается в сторону уменьшения количеств газообразных веществ, т.е. в сторону понижения давления; при уменьшении давления равновесие смещается в сторону возрастания количеств газообразных веществ, т.е. в сторону увеличения давления. Если реакция протекает без изменения числа молекул газообразных веществ, то давление не влияет на положение равновесия в этой системе.
3. При повышении температуры равновесие смещается в сторону эндотермической реакции, при понижении температуры – в сторону экзотермической реакции.
