
- •1. Важнейшие классы неорганических соединений (оксиды, гидроксиды, соли)
- •Сложные неорганические соединения
- •Диссоциацию кислой соли можно выразить уравнением
- •Лабораторная работа Получение и свойства оксидов, гидроксидов и солей Цель работы
- •Контрольные вопросы и упражнения
- •2. Скорость химической реакции. Катализ
- •Катализ
- •Лабораторная работа Химическая кинетика. Катализ
- •Опыт 2. Зависимость скорости гомогенной реакции от температуры
- •Контрольные вопросы и упражнения
- •3. Химическое равновесие
- •Лабораторная работа Химическое равновесие
- •Контрольные вопросы и упражнения
- •4. Растворы электролитов. Электролитическая диссоциация
- •Лабораторная работа Электролитическая диссоциация
- •Контрольные вопросы и упражнения
- •5. Растворы
- •5.1 Растворимость веществ в воде. Свойства растворов
- •Лабораторная работа Растворимость веществ в воде. Свойства растворов
- •5.2 Концентрация растворов. Приготовление водных растворов
- •Приготовление раствора заданной концентрации по правилу смешения из более концентрированного раствора и воды или из двух растворов с известным процентным содержанием
- •Лабораторная работа Приготовление растворов
- •Плотность растворов NaCl и kCl
- •Контрольные вопросы и упражнения
1. Важнейшие классы неорганических соединений (оксиды, гидроксиды, соли)
В настоящее время известно около 300 тыс. неорганических соединений. Их можно разделить на три важнейших класса: оксиды, гидроксиды и соли.
Сложные неорганические соединения

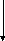

оксиды

 соли
соли

 несолеобразующие
гидроксиды
средние
несолеобразующие
гидроксиды
средние


 солеобразующие
основные
солеобразующие
основные

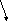

 (основания)
кислые
(основания)
кислые

 основные
амфотерные кислотные
основные
основные
амфотерные кислотные
основные
(кислоты)
кислотные
 амфотерные
амфотерные
(амфолиты)
Оксиды – сложные вещества, молекулы которых состоят из атомов кислорода и какого-нибудь другого элемента. Например, К2О, FeO, Cr2O3, SiO2, P2O5.
Оксиды делятся на солеобразующие и несолеобразующие. Последних довольно мало (CO, NO, N2O), они не образуют солей ни с кислотами, ни со щелочами. Солеобразующие оксиды делятся на основные (их гидраты – основания) кислотные (их гидраты кислоты), амфотерные (их гидраты проявляют свойства, как кислот, так и оснований).
По современной номенклатуре названия этого класса строятся следующим образом: к слову оксид добавляется название элемента с указанием его степени окисления, если она не постоянна. Например, CaO – оксид кальция, Fe2O3 - оксид железа (III), P2O5 – оксид фосфора (V).
К основным оксидам относятся оксиды щелочных и щелочно-земельных металлов, а также многие оксиды других металлов со степенью окисления +1, +2. Они взаимодействуют с водой с образованием оснований:
BaO + H2O = Ba(OH)2.
Непосредственно с водой при обычной температуре реагируют только оксиды металлов I и II групп главных подгрупп (кроме BeO и MgO) периодической системы Д. И. Менделеева.
Основные оксиды взаимодействуют с кислотными оксидами и кислотами, образуя соли:
CaO + CO2 = CaCO3;
CuO + 2 HCl = CuCl2 + H2O.
Кислотные оксиды образуют неметаллы (Cl2O, B2O3, CO2, N2O5, SO3, Cl2O7 и др.), а также металлы со степенью окисления +5, +6, +7 (V2O5, CrO3, Mn2O7, WO3).
Многие кислотные оксиды непосредственно взаимодействуют с водой, образуя кислоты:
SO2 + H2O = H2SO3;
CrO3 + H2O = H2CrO4.
С щёлочами кислотные оксиды образуют соль и воду:
N2O5 + 2 NaOH = 2 NaNO3 + H2O.
Амфотерные оксиды образуют металлы, имеющие степени окисления +3, +4, иногда +2. К амфотерным оксидам относятся, например, BeO, ZnO, Al2O3, Cr2O3, SnO, PbO, MnO2 и др. Они характеризуются реакциями солеобразования и с кислотами, и с основаниями, так как в зависимости от условий проявляют как основные, так и кислотные свойства.
Например, как основный оксид Cr2O3 реагирует с кислотой:
Cr2O3 + 6 HCl = 2 CrCl3 + 3 H2O,
как кислотный – с щёлочью:
Cr2O3 + 2 NaOH = 2 NaCrO2 + H2O.
+2 +3 +6
Если элемент образует несколько оксидов, например, CrO, Cr2O3, CrO3, то по мере увеличения его степени окисления усиливается кислотный характер оксида. Так, CrO – основный, Cr2O3 - амфотерный, а CrO3 – кислотный оксид.
Оксиды можно получить следующими способами.
-
При взаимодействии простых веществ с кислородом:
2 Mg + O2 = 2 MgO;
4 P + 5 O2 = 2 P2O5.
2. Разложением сложных веществ:
t
Cu(OH)2 = CuO + H2O;
t
CaCO3 = CaO + CO2;
t
2 Zn(NO3)2 = 2 ZnO + 4 NO2 + O2.
Гидроксиды продукты соединения оксидов с водой. Они бывают трех видов: основные (основания), кислотные (кислоты) и амфотерные (амфолиты).
Основания – электролиты, которые при диссоциации в качестве анионов образуют только гидроксид-ионы:
NaOH = Na+ + OH.
Кислотность основания определяется числом ионов OH- , образующихся при диссоциации. Многокислотные основания диссоциируют ступенчато:
Mg(OH)2 ⇄ (MgOH)+ + OH,
(MgOH)+ ⇄ Mg2+ + OH.
По растворимости в воде различают два вида основания:
а) основания, растворимые в воде, щёлочи. К ним относятся LiOH, NaOH, KOH, RbOH, CsOH, Ca(OH)2, Sr(OH)2, Ba(OH)2, а также TlOH;
б) основания, нерастворимые в воде, например Cu(OH)2, Fe(OH)3, Cr(OH)3 и др.
Названия оснований образуются из слова гидроксид и названия соответствующего металла с указанием его степени окисления, если она переменна. Например, Ca(OH)2 гидроксид кальция, Fe(OH)2 – гидроксид железа (II), Fe(OH)3 – гидроксид железа (III).
Водные растворы щелочей изменяют окраску индикаторов. В их присутствии фиолетовый лакмус синеет, бесцветный фенолфталеин становится малиновым, метиловый оранжевый – желтым.
Щёлочи образуют с кислотными оксидами соль и воду:
Ba(OH)2 + CO2 = BaCO3 + H2O.
Щёлочи взаимодействуют с кислотами с образованием соли и воды (реакция нейтрализации):
2 NaOH + H2SO4 = Na2SO4 + 2 H2O.
При действии щёлочей на растворы солей получаются новые соль и основание, при этом одно из полученных веществ должно выпадать в осадок:
2 KOH + CuSO4 = Cu(OH)2↓ + K2SO4;
Ca(OH)2 + Na2CO3 = CaCO3↓ + 2 NaOH.
С точки зрения электролитической диссоциации общие свойства щёлочей обусловлены гидроксид-ионами OH.
Нерастворимые в воде основания, так же как и щелочи, взаимодействуют с кислотами:
Fe(OH)3 + 3 HCl = FeCl3 + 3 H2O
и разлагаются при нагревании:
t
2 Fe(OH)3 = Fe2O3 + 3 H2O.
Получить щёлочи можно растворением в воде соответствующих оксидов:
CaO + H2O = Ca(OH)2
или разложением воды очень активными металлами (K, Na, Ca, Ba):
2 Na + 2 HOH = 2 NaOH + H2.
Общий способ получения нерастворимых в воде оснований – действие щёлочей на растворимые соли металлов, основания которых нерастворимы:
2 NaOH + FeSO4 = Fe(OH)2↓ + Na2SO4.
Кислоты – электролиты, при диссоциации которых в качестве катионов образуются только катионы водорода Н+ (точнее ионы гидроксония Н3О+):
HCl = H+ + Cl.
Основность кислоты определяется числом катионов водорода, которые образуются при диссоциации. Многоосновные кислоты диссоциируют ступенчато. Например:
H2CO3 ⇄ H+ + НCО3,
НCО3 ⇄ H+ + CО32.
Кислоты можно разделить на бескислородные (HCl, HBr, HCN, H2S) и кислородсодержащие (HNO3, H2SO4, H3PO4).
Названия кислородсодержащих кислот, в которых степень окисления кислотообразующего элемента (центрального атома) равна номеру группы в периодической системе элементов Д.И. Менделеева (высшая степень окисления), образуются от названия элемента с добавлением суффикса –н (-ов или -ев) и окончания –ая. Например, HNO3 - азот-н-ая кислота, H3AsO4 - мышьяк-о-ов-ая кислота, H2SiO3 - кремни-ев-ая кислота. При меньшей степени окисления центрального атома названия кислот образуются с суффиксом –ист. Например, HNO2 - азот-ист-ая кислота, H2SO3 - серн-ист-ая кислота.
В названиях бескислородных кислот к наименованию элемента добавляют слово водородная. Например, HCl - хлороводородная, H2S - сероводородная.
В растворах кислот индикаторы меняют свою окраску: лакмус становится красным, метиловый оранжевый – розовым.
Кислоты взаимодействуют с металлами, стоящими левее водорода в ряду стандартных электродных потенциалов, образуя соль и водород:
2 Al + 3 H2SO4 = Al2(SO4)3 + 3 H2↑.
Водород не выделяется при взаимодействии металлов с концентрированными азотной и серной кислотами.
Кислоты реагируют с основаниями и основными оксидами:
H2SO4 + Mg(OH)2 = MgSO4 + 2 H2O,
2 HNO3 + CaO = Ca(NO3)2 + H2O.
При взаимодействии кислот с солями могут образовываться новые соль и кислота:
 CO2
CO2
2 HCl + CaCO3
= CaCl2
+ H2CO3
HCl + CaCO3
= CaCl2
+ H2CO3
H2O,
H2SO4 + BaCl2 = BaSO4↓ + 2 HCl.
С точки зрения электролитической диссоциации общие свойства кислот обусловлены ионами водорода Н+. Кислоты получают следующими способами:
1) гидратацией кислотных оксидов
P2O5 + 3 H2O = 2 H2PO4;
2) обменной реакцией соли с кислотой
Ca3(PO4)2 + 3 H2SO4 = 3 CaSO4 + 2 H3PO4.
Амфолиты – это гидроксиды, которые проявляют как основные, так и кислотные свойства. К ним относятся, например, Cr(OH)3, Zn(OH)2, Be(OH)2, Al(OH)3 и др.
Амфотерные гидроксиды способны реагировать как с кислотами, так и с щёлочами. С кислотами они реагируют как основания, а с щёлочами – как кислоты. Чтобы установить амфотерность гидроксида, следует провести две реакции взаимодействия его с кислотой и со щелочью. Если обе реакции имеют место, то гидроксид амфотерен. Например,
Cr(OH)3 + 3 HCl = CrCl3 + 3 H2O;
Cr(OH)3 + 3 NaOH = Na3[Cr(OH)6].
Соли – электролиты, при диссоциации которых образуются катионы металлов (или ионы аммония NH4+), анионы кислотных остатков. Соли делятся на средние, кислые, основные.
Средние соли можно рассматривать как продукты полного замещения атомов водорода в кислоте атомами металла или как продукты полного замещения гидроксогрупп основания кислотными остатками. Например, Na2CO3, K2SO4, Ca3(PO4)2. Уравнения диссоциации средних солей можно записать так:
K3PO4 = 3 K+ + PO43,
NH4Cl = NH4+ + Cl.
Кислые соли (гидросоли) – продукты неполного замещения атомов водорода многоосновных кислот атомами металла. Их образуют только многоосновные кислоты. Например, NaHCO3 Ca(H2PO4)2, KHSO3.
