
Zadachi_dlya_42_g
.docxЗадания для группы 42 г
Задание №1 (Архипенко)
Задача 1
Рассчитайте, сколько мл соляной кислоты с массовой долей 0,38 и р=1,19 г/мл3 нужно взять для приготовления 5 л 0,1 М раствора?
Задача 2
Золь иодида серебра AgJ получен при добавлении к 0,02 л 0,01 М раствора КJ 0,028 л 0,005 М раствора АgNO3. Определите заряд частиц полученного золя и напишите формулу его мицеллы.
Задача 3
Увеличится, уменьшится или останется без изменения масса цинковой пластинки при взаимодействии ее с растворами: а) СuSО₄;б) МgSО₄; в) Рb(NО₃)₂? Почему? Составьте электронные и молекулярные уравнения соответствующих реакций.
Задача 4
При электролизе раствора соли кадмия израсходовано 3434 Кл электричества. Выделилось 2 г кадмия. Чему равна эквивалентная масса кадмия?
Задача 5
Как происходит атмосферная коррозия луженого и оцинкованного железа при нарушении покрытий? Составьте электронные уравнения анодного и катодного процессов.
Задание №2 (Бургер)
Задача 1
Массовая концентрация сульфат-иона (SО₄²⁻) составляет 96,0 мг/дм3 . Какова молярность и молярность раствора?
Задача 2
Золь сульфида цинка был получен при взаимодействии растворов Zn(NO3)2 и Na2S . Определите, какой из электролитов был в избытке, если противоионы в электрическом поле движутся к аноду. Напишите формулу мицеллы золя.
Задача 3
Увеличится, уменьшится или останется без изменения масса цинковой пластинки при взаимодействии ее с растворами: а)АgN О₃;б) ZnSО₄; в) NiSО₄? Почему? Составьте электронные и молекулярные уравнения соответствующих реакций.
Задача 4
При электролизе соли некоего металла в течение 1,5 часа при силе тока 1,8 А на катоде выделилось 1,75 г этого металла. Чему равна эквивалентная масса этого металла?
Задача 5
Две железные пластинки, частично покрытые одна оловом, другая медью, находятся во влажном воздухе. На какой из этих пластинок быстрее образуется ржавчина? Почему? Составьте электронные уравнения анодного и катодного процессов коррозии этих пластинок. Каков состав продуктов коррозии железа?
Задание №3 (Голотяк)
Задача 1
Массовая концентрация гидроксида цинка составляет 80,0 мг/дм3. Какова молярность и нормальность раствора?
Задача 2
Вычислите константу диссоциации уксусной кислоты СН3СООН, зная, что в 0,1М растворе она диссоциирована на 1,32%.
Задача 3
Составьте схемы двух гальванических элементов, в одном из которых медь была бы катодом, а в другом-анодом. Напишите для каждого из этих элементов электронные уравнения реакций, протекающих на катоде и аноде.
Задача 4
При электролизе соли трехвалентного металла при силе тока 1,5 А в течение 30 мин на катоде выделилось 1,071 г металла. Вычислите атомную массу металла.
Задача 5
Какой металл целесообразно выбрать для протекторной защиты от коррозии свинцовой оболочки кабеля: цинк, магний или хром? Почему? Составьте электронные уравнения анодного и катодного процессов атмосферной коррозии. Каков состав продуктов коррозии?
Задание №4(Гребенников)
Задача 1
Молярная концентрация раствора гидроксида кальция равна 2 моль/л. Определите нормальность этого раствора.
Задача 2
Вычислите значение рН 0,1М раствора гидроксида аммония NH4OH, приняв степень диссоциации раствора равной 1%.
Задача 3
Составьте схемы двух гальванических элементов, в одном из которых никель был бы катодом, а в другом-анодом. Напишите для каждого из этих элементов электронные уравнения реакций, протекающих на катоде и аноде. Задача 4
При электролизе раствора сульфата меди на аноде выделилось 168 см³ кислорода (н.у.) сколько граммов меди выделилось на катоде?
Задача 5
Составьте электронные уравнения анодного и катодного процессов с кислородной и водородной деполяризацией при коррозии пары алюминий-железо. Какие продукты коррозии образуются в первом и во втором случаях?
Задание №5 (Иванов)
Задача 1
Вычислите массовую долю карбоната калия, молярность и нормальность раствора, содержащего 75 г карбоната калия в 300г воды.(р=1,25 г/мл3).
Задача 2
Растворимость AgCI при 25⁰,С равна 1,25 ·10⁻⁵ моль/л. Вычислить ПРAgCI.
Задача 3
Железная и серебряная пластины соединены внешним проводником и погружены в раствор серной кислоты. Составьте схему гальванического элемента и напишите электронные уравнения процессов, протекающих на аноде и на катоде.
Задача 4
При электролизе раствора сульфата меди на аноде выделилось 168 см³ кислорода (н.у.). Какая масса воды при этом разложилась? Составьте электронные уравнения процессов, протекающих на электродах.
Задача 5
Железное изделие покрыли кадмием. Какое это покрытие – анодное или катодное? Почему? Составьте электронные уравнения анодного и катодного процессов коррозии этого изделия при нарушении этого покрытия во влажном воздухе и в хлороводородной (соляной) кислоте. Какие продукты образуются в первом и во втором случае?
Задание №6 (Киселев)
Задача 1
Сколько граммов сульфата бария выпадет в осадок, если к 50 см3 0,2 М раствора серной кислоты прибавить избыток хлорида бария
Задача 2
На нейтрализацию 31 мл 0,16 н раствора щелочи требуется 217 мл раствора серной кислоты. Чему равна нормальность раствора кислоты?
Задача 3
Цинковую и железную пластины опустили в раствор сульфата меди. Составьте электронные и ионно-молекулярные уравнения реакций, протекающих на каждой из этих пластинок. Какие процессы будут проходить на пластинках, если наружные концы их соединить проводником?
Задача 4
При электролизе растворов Мg SО₄ и ZnСI₂ соединенных последовательно источником тока, на одном из катодов выделилось 0,25 г водорода. Сколько граммов вещества выделится на другом катоде; на анодах?
Задача 5
Железное изделие покрыли никелем. Какое это покрытие – анодное или катодное? Почему? Составьте электронные уравнения анодного и катодного процессов коррозии этого изделия при нарушении этого покрытия во влажном воздухе и в хлороводородной (соляной) кислоте. Какие продукты образуются в первом и во втором случае?
Задание №7 (Козин)
Задача 1
Вычислите молярную, нормальную концентрацию и моляльность раствора ортофосфорной кислоты, содержащего 49 г Н3РО4 в 100 г раствора (р=1,33 г/см3).
Задача 2
Вычислите константу диссоциации уксусной кислоты СН3СООН, зная, что в 0,1М растворе она диссоциирована на 1.32%.
Задача 3
Если погрузить в разбавленную серную кислоту пластинку из чистого железа, то выделение на ней водорода идет медленно и со временем почти прекращается. Однако, если цинковой палочкой прикоснуться к железной пластинке, то на последней начинается бурное выделение водорода. Почему? Какой металл при этом растворяется? Составьте электронные уравнения анодного и катодного процессов.
Задача 4
Составьте электронные уравнения процессов, протекающих на электродах при электролизе расплава КОН, раствора КОН.
Задача 5
Какое покрытие металла называют анодным и какое – катодным? Назовите несколько металлов, которые могут служить для анодного и катодного покрытия железа. Составьте электронные уравнения анодного и катодного процессов протекающих при коррозии железа, покрытого медью, во влажном воздухе и в кислой среде.
Задание №8 (Колесников)
Задача 1
Массовая концентрация хлорида натрия составляет 58,5 мг/дм3. Какова его молярность?
Задача 2
Смешивают попарно растворы: а) Сu(NОЗ)2 и Na2SО4; б) ВаCl2 и K2SO4; в) КNО3 и NaCl; г) АgNО3 и KCl; д) Са(ОН)2 и HCl. В каких из приведенных случаев реакция пройдет до конца? Составьте для этих реакций молекулярные и молекулярно-ионные уравнения.
Задача 3
В раствор хлороводородной (соляной) кислоты поместили цинковую пластинку и цинковую пластинку, частично покрытую медью. В каком случае процесс коррозии цинка протекает интенсивнее? Ответ мотивируйте, составив электронные уравнения соответствующих процессов.
Задача 4
Составьте электронные уравнения процессов, протекающих на электродах при электролизе расплава КСI, раствора КСI.
Задача 5
Составьте электронные уравнения анодного и катодного процессов с кислородной и водородной деполяризацией при коррозии пары магний – никель. Какие продукты коррозии образуются в первом и во втором случаях?
Задание №9 (Кузьмин )
Задача 1
В каком количестве воды необходимо растворить 70 г вещества, чтобы получить 10%-й раствор?
Задача 2
Выразите молекулярными и молекулярно-ионными уравнениями реакции взаимодействия между а) хлоридом бария и сульфатом алюминия; б) хлоридом аммония и гидроксидом калия при нагревании; в) гидроксидом стронция и соляной кислотой; г) фосфорной кислотой и нитратом кальция; д) ацетатом калия и серной кислотой.
Задача 3
Медь не вытесняет водород из разбавленных кислот. Почему? Однако если к медной пластинке, опущенной в кислоту, прикоснуться цинковой, то на меди начинает бурное выделение водорода. Дайте этому явлению объяснение, составьте электронные уравнения анодного и катодного процессов. Напишите уравнение протекающей химической реакции.
Задача 4
Составьте электронные уравнения процессов, протекающих на электродах при электролизе растворов АIСI₃, NiSО₄. В обоих случаях анод угольный.
Задача 5
Как влияет рН среды на скорость коррозии железа и цинка? Почему? Составьте электронные уравнения анодного и катодного процессов атмосферной коррозии этих металлов.
Задание №10 (Миролюбова)
Задача 1
Какой объем 96%-й серной кислоты, плотностью 1,84 г/см3 потребуется для приготовления 3л 0,4н раствора?
Задача 2
При смешении растворов Al2(SO4)3 и К2S в осадок выпадает А1(ОН)3, Укажите причину этого и составьте соответствующие молекулярные и молекулярно-ионные уравнения.
Задача 3
В два сосуда с голубым раствором медного купороса поместили в первый цинковую пластинку, а во второй серебряную. В каком сосуде цвет раствора постепенно пропадает? Составьте электронные и ионно-молекулярные уравнения соответствующих реакций.
Задача 4
Составьте электронные уравнения процессов, протекающих на электродах при электролизе раствора АI₂(SО₄)₃ в случае угольного анода; в случае алюминиевого анода.
Задача 5
Составьте электронные уравнения анодного и катодного процессов коррозии этого изделия при нарушении этого покрытия во влажном воздухе и в хлороводородной (солянй) кислоте. Какие продукты образуются в первом и во втором случае?
Задание №11 (Новиков)
Задача 1
Какой объем 0,3 н раствора кислоты требуется для нейтрализации раствора, содержащего 0,32 г едкого натра в 40 см3?
Задача 2
Произведение растворимости BaSO₄ равно 1·1010. Вычислить растворимость этой соли в воде (в моль/л).
Задача 3
При какой концентрации ионов Zn²⁺(в моль/л) потенциал цинкового электрода будет на 0,015 В меньше его стандартного электродного потенциала?
Задача 4
Составьте электронные уравнения процессов, протекающих на электродах при электролизе СuСI₂, если анод медный, если анод угольный
Задача 5
Как протекает атмосферная коррозия железа покрытого слоем никеля, если покрытие нарушено? Составьте электронные уравнения анодного и катодного процессов. Каков состав продуктов коррозии?
Задание №12 (Пугачев)
Задача 1
Нормальная концентрация серной кислоты составляет 4моль/л. Определите молярность этого раствора и его массовую долю ().
Задача 2
При смешении растворов AgNO3 и KJ протекает реакция: AgNO3 + KJ = AgJ + KNO3 . Напишите формулы мицелл при избытке как одного, так и другого из реагирующих веществ.
Задача 3
Марганцевый электрод в растворе его соли имеет потенциал – 1,23 В. Вычислите концентрацию ионов марганца Мn²⁺ (моль/л).
Задача 4
Составьте электронные уравнения процессов, протекающих на графитовых электродах при электролизе расплавов и водных растворов NаСI и КОН. Сколько литров (н.у.) газа выделится на аноде при электролизе гидроксида калия, если электролиз проводить в течение 30 мин при силе тока 0,5 А?
Задача 5
В чем сущность протекторной защиты металлов от коррозии? Приведите пример протекторной защиты железа в электролите, содержащем растворенный кислород. Составьте электронные уравнения анодного и катодного процессов.
Задание №13 (Пшеничников)
Задача 1
Какая масса азотной кислоты содержалась в растворе, если на нейтрализацию его требовалось 35 см3 0,4н раствора едкого натра? Каков титр раствора едкого натра?
Задача 2
Золь сульфида цинка был получен при взаимодействии растворов Zn(NO3)2 и Na2S . Определите, какой из электролитов был в избытке, если противоионы в электрическом поле движутся к аноду. Напишите формулу мицеллы золя.
Задача 3
Какие химические реакции протекают на электродах при зарядке и разрядке свинцового аккумулятора?
Задача 4
Электролиз раствора сульфата некоторого металла проводили при силе тока 6 А в течение 45 мин, в результате чего на катоде выделилось 5,49 г металла. Вычислите эквивалентную массу металла.
Задача 5
В раствор электролита, содержащего растворенный кислород опустили цинковую пластинку частично покрытую медью. В каком случае процесс коррозии цинка происходит интенсивнее? Составьте электронные уравнения анодного и катодного процессов.
Задание №14 (Тарасенко0
Задача 1
Смешали 247 г 62%-ного и 145 г 18%-ного раствора серной кислоты. Какова массовая доля полученного раствора?
Задача 2
Вычислите осмотическое давление раствора, содержащего в 1,4 л 63 г глюкозы С₆Н₁₂О₆ при 0⁰С.
Задача 3
Какие химические реакции протекают на электродах при зарядке и разрядке кадмий-никелевого аккумулятора?
Задача 4
Электролиз раствора нитрата серебра проводили при силе тока 2 А в течение 4 час. Сколько граммов серебра выделилось на катоде?
Задача 5
Хром находится в контакте с медью. Какой из металлов будет окисляться при коррозии, если эта пара металлов попадет в кислую среду (HCl)? Приведите схему образующегося при этом гальванического элемента.
Задание №15 (Тезекбаев)
Задача 1
На нейтрализацию 500 см раствора, содержащего 8 г едкого натра, потребовалось 250 см3 раствора кислоты. Вычислите молярность, нормальность кислоты.
Задача 2
Определите температуру кипения и замерзания раствора, содержащего 1 г нитробензола С₆Н₅NО₂ в 10 г бензола. Эбулиоскопическая и криоскопическая константы соответственно равны 2,57 и 5,1 ⁰С. Температура кипения чистого бензола 80,2⁰С, температура замерзания – 5,4⁰С.
Задача 3
Какие химические реакции протекают на электродах при зарядке и разрядке железо-никелевого аккумулятора?
Задача 4
Электролиз раствора К₂SО₄ проводили при силе тока 5 А в течение 3 час. Составьте электронные уравнения процессов, протекающих на электродах, вычислите объем выделяющихся на электродах веществ.
Задача 5
При нарушении целостности поверхностного слоя медного покрытия на алюминии будет протекать коррозия алюминия из-за образования гальванопары: (–) 2Al/Al³⁺|H₂SO₄|3H₂/6H⁺(Cu) (+)
За 45 с работы этой гальванопары на катоде выделилось 0,09 л водорода (измеренного при н. у.). Сколько граммов алюминия растворилось за это время и какую силу тока дает эта гальванопара?
Гальванический элемент дает ток Iсилой 17,2 А (0,002·96500 / 11,2).
Эквивалент алюминия равен 9 г/моль-экв.
Задание №16 (Титов)
Задача 1
Какой объем 10%-ного раствора карбоната натрия (р=1,105 г/см3) требуется для приготовления 5 л 2%-ного раствора (р=1,02г/см3).
Задача 2
Раствор камфоры массой 0,552 г в 17 г эфира кипит при температуре на 0,461⁰С выше, чем чистый эфир. Эбуллиоскопическая постоянная эфира 2,16⁰С. Определите молекулярную массу камфоры.
Задача 3
Вычислите электродный потенциал цинка, погруженного в раствор соли цинка с концентрацией ионов Zn2+ 0,001 моль/л.
Задача 4
Вычислите силу тока, зная, что при электролизе раствора КОН в течение 1 часа 15 мин 20 с на аноде выделилось 6,4 г кислорода. Какое вещество и в каком количестве выделяется на катоде?
Задача 5
Как происходит атмосферная коррозия луженого железа при нарушении целостности покрытия? Приведите уравнения реакций образования вторичных продуктов коррозии железа с учетом окисления гидроксида железа (II) до гидроксида железа (III), приводящего к образованию ржавчины.
Задание №17 (Туголуков)
Задача 1
Вычислите массовую долю серной кислоты в ее 5М растворе (р=1,29 г/см3).
Задача 2
Вычислите давление пара над раствором, содержащим 34,23 г сахара С₁₂Н₂₂О₁₁, в 45,05 г воды при 65⁰С, если давление паров воды при этой температуре равно 2,5 ∙10⁴ Па.
Задача 3
Исходя из величин
стандартных электродных потенциалов
и значения DG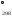 укажите, можно ли в гальваническом
элементе осуществить реакцию:Fe⁰
+Cd²⁺↔Fe²⁺+Cd⁰.
укажите, можно ли в гальваническом
элементе осуществить реакцию:Fe⁰
+Cd²⁺↔Fe²⁺+Cd⁰.
Задача 4
Сколько времени протекает электролиз раствора электролита при силе тока 5 А, если на катоде выделяется 0,1 эквивалентной массы вещества?
Задача 5
Алюминий склепан
с медью. Какой из металлов будет
подвергаться коррозии, если эти металлы
попадут в кислотную среду? Составьте
схему гальванического элемента,
образующегося при этом. Подсчитайте
ЭДС и DG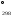 этого элемента для стандартных условий.
этого элемента для стандартных условий.
Задание №18 (Фадин)
Задача 1
Какой объем 20,01%-ного раствора соляной кислоты (р=1,10 г/см3) требуется для приготовления 1 л 10,17%-ного раствора (р=1,050 г/см3)?
Задача 2
Золь сульфида цинка был получен при взаимодействии растворов Zn(NO3)2 и Na2S . Определите, какой из электролитов был в избытке, если противоионы в электрическом поле движутся к аноду. Напишите формулу мицеллы золя.
Задача 3
Составьте схему
и разберите работу гальванического
элемента, который описывается схемой:
Mg
| MgSO4
|| Zn(NO3)2
| Zn,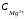 =
10–2
моль/л,
=
10–2
моль/л,
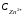 =
1 моль/л. Вычислите значение ЭДС.
=
1 моль/л. Вычислите значение ЭДС.
Задача 4
Какой объем водорода (н. у.) выделится при пропускании электрического тока силой 2А в течение 42 мин через раствор серной кислоты? Напишите соответствующие уравнения реакций.
Задача 5
Железо покрыто
медью. Какой из металлов будет подвергаться
коррзии в случае разрушения поверхности
покрытия? Коррозия происходит в
нейтральной среде.Составьте схему
гальванического элемента, образующегося
при этом. Подсчитайте ЭДС и DG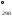 этого элемента для стандартных условий.
Напишите соответствующие уравнения
реакций, поясните ответ рисунком.
этого элемента для стандартных условий.
Напишите соответствующие уравнения
реакций, поясните ответ рисунком.
Задание №19 (Хавтаси)
Задача 1
Из 10 кг 20%-ного раствора при охлаждении выделилось 400 г соли. Чему равна массовая доля охлажденного раствора?
Задача 2
Коагулирование коллоидных примесей в технической воде осуществляется добавлением к ней сульфата алюминия. Образующийся хлопьевидный гидроксид алюминия обволакивает коллоидные частицы и вызывает их осаждение. Объясните образование гидроксида алюминия в результате реакции, проходящей в жесткой воде:
АI₂(SО₄)₃ + 2Са(НСО₃)₂=3СаSО₄+2АI(ОН)₃+6СО₂
Задача 3
Составьте схему работы гальванического элемента, образованного железом и свинцом, погруженными в 0,005 M растворы их солей. Напишите анодный и катодный процессы, токообразующую реакцию. Рассчитайте ЭДС этого элемента и изменение величины энергии Гиббса.
Задача 4
На электролиз раствора СаСI₂ израсходовано 10722,2 Кл электричества. Вычислите массу выделяющихся на угольных электродах и образующихся возле катода веществ.
Задача 5
Если на стальной предмет нанести каплю воды, то коррозии подвергается средняя, а не внешняя часть смоченного металла. После высыхания капли в ее центре появляется пятно ржавчины. Чем это можно объяснить? Какой участок металла, находящийся под каплей воды, является анодным и какой катодным? Составьте уравнения соответствующих процессов.
Задание №20 (Чередник)
Задача 1
Какой объем 50%-ного раствора едкого кали (р=1,538 г/см3) требуется для приготовления 3л 6%-ного раствора (р=1,048 г/см3)?
Задача 2
К растворам Nа₂SО₄, СrСI₃ , Fе(NО₃)₃ добавили раствор соды Nа₂СО₃. В каких случаях наблюдается выделение СО₂? Почему? Составьте ионно-молекулярные и молекулярные уравнения соответствующих реакций.
Задача 3
Вычислите ЭДС и изменение величины энергии Гиббса для гальванического элемента, образованного магнием и цинком, погруженными в растворы их солей с концентрациями ионов (моль/л):СMg2+= 10–4, СZn2+ = 10–2. Сравните полученное значение ЭДС с ЭДС гальванического элемента, образованного стандартными электродами тех же металлов.
Задача 4
Электролиз раствора К2SО4 проводили при силе тока 5 A в течение 3 ч. Составьте электронные уравнения процессов, происходящих на электродах. Какая масса воды при этом разложилась и чему равен объем газов (н. у.), выделившихся на катоде и аноде?
Задача 5
Железо покрыто
оловом. Какой из металлов будет
корродировать в случае разрушения
поверхности покрытия? Коррозия происходит
в кислотной среде. Составьте схему
коррозийного гальванического элемента,
образующегося при этом. Подсчитайте
ЭДС и DG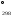 этого элемента для стандартных условий.
Напишите соответствующие уравнения
реакции.
этого элемента для стандартных условий.
Напишите соответствующие уравнения
реакции.
Задание №21 (Шевелев)
Задача 1
Вычислите молярную концентрацию и молярную концентрацию эквивалента 20%-ного раствора хлорида кальция плотностью 1,178 г/см3.
Задача 2
В какой цвет будет окрашен лакмус в водных растворах NН₄СI, Nа₂СО₃, NаNО₃? Ответ обоснуйте.
Задача 3
Какие процессы
происходят у электродов медного
концентрационного гальванического
элемента, если у одного из электродов
СCu2+
равна 1 моль/л, а у другого – 10 –3
моль/л? В каком направлении движутся
электроны во внешней цепи? Ответ дайте,
исходя из значений ЭДС и DG этой цепи.
этой цепи.
Задача 4
Какой силы ток должен быть использован для того, чтобы выделить из раствора AgNO3 серебро массой 108 г за 6 мин? Составьте схему электролиза этого раствора при использовании графитовых электродов.
Задача 5
Гальванический элемент
(–) 2 Cr/2Cr³⁺| H₂SO₄| 3H₂/6H⁺(Pb)(+),
образовавшийся при коррозии хрома, спаянного со свинцом, дает ток силой 6 А. Сколько граммов хрома окислится и сколько литров водорода выделится за 55 с работы этого элемента? Напишите соответствующие уравнения реакций, поясните ответ рисунком.
Задание №22 (Шеменкова)
Задача 1
К 120 мл раствора хлорида натрия с массовой долей вещества 16% (р=1,12 г/см3) прилили 80 мл воды (р=1,0 г/см3). Рассчитайте массовую долю хлорида натрия в полученном растворе и молярность этого раствора.
Задача 2
В какую сторону сместится равновесие гидролиза NаСN, Если к раствору добавить: а) щелочь, б) кислоту?
Задача 3
Гальванический элемент, образованный никелем, погруженным в раствор нитрата никеля с концентрацией, равной 10–4 моль/л, и серебром, погруженным в раствор нитрата серебра, имеет значение ЭДС равное 1,108 В. Определите концентрацию ионов Ag+ в растворе соли.
Задача 4
Через раствор сульфата железа (II) пропускали ток силой 13,4 А в течение одного часа. Определите массу железа, выделившегося на катоде, если выход по току составляет 70 %. Составьте схему электролиза этого раствора при использовании угольных электродов.
Задача 5
Медь покрыта оловом. При нарушении оловянного покрытия работает гальванический элемент
( –) 2Sn/Sn²⁺| HCl | 2H⁺/H₂ (Cu) (+)
который дает ток силой 7,5 А. Сколько граммов олова растворится и сколько литров водорода выделится на медном катоде за 25 мин? Напишите соответствующие уравнения реакций, поясните ответ рисунком.
