
- •1 Массопередача, Массообменные процессы. Движущая сила диффузионных процессов. Понятие о расчетах массообменных аппаратов
- •2 Понятие о ступени изменении концентрации. Схема процесса массообмена на тарелке
- •3 Процесс конденсации. Материальный баланс процесса однократной и фракционарованной конденсации
- •4 Процесс ректификации, схема, материальный и тепловой баланса
- •5 Понятие о процессе абсорбции. Схема и материальных потоков в абсорбере. Материальный и тепловой баланс абсорбера
- •6 Понятие о процессе десорбции. Схема материальных потоков в десорбере. Тепловой баланс десорбера
- •7 Конструкция абсорбера и десорбера
- •8 Конструкция тарелок: колпачковых, клапанных и балластных, ситчатых пятислойных щелевых, решетчатых, трубчатых
- •10 Компрессорный способ переработки газа
- •11 Абсорбционный способ переработки газа. Масло абсорбционные газобензиновые установки
- •12 Расчет процесса абсорбции с предварительным насыщением тощего абсорбента и отбензиниванием сырого газа
- •13 Абсорбционная система с рециркуляцией газов десорбции
- •14 Установка двухступенчатой абсорбции
- •15 Принципиальная технологическая схема многоступенчатой абсорбции
- •18 Технологические схемы переработки газа методом низкотемпературной конденсации. Краткая классификация схем нтк.
- •26 Принципиальная схема промысловой установки нтк с турбодетандером для переработки пр.Газа
- •32 Переработка газа методом низкотемпературной ректификации. Схема ректификационно – отпарной колонны. Схема – конденсационно – отпарной колонны.
- •33 Схема нтр с двумя вводами. Схема нтр с турбодетандером
1 Массопередача, Массообменные процессы. Движущая сила диффузионных процессов. Понятие о расчетах массообменных аппаратов
Процессы физической переработки природных газов, процессы конденсации (сжижения), абсорбции, ректификации, адсорбции связаны с переходом вещества из одной фазы в другую, с явлением массообмена или диффузии и поэтому получили название массообменных или диффузионных процессов.
Переход вещества из одной фазы в другую, или массопередача, совершается в направлении достижения равновесия между обеими фазами (рисунок 1).

а) из фазы Г в фазу Ж; б) из фазы Ж в фазу Г
Рисунок 1 – Направления перехода распределяемого вещества
Любой концентрации вещества х в жидкой фазе (Ж) соответствует равновесная концентрация yр в газовой фазе (Г) и наоборот, любой концентрации y в газовой фазе (Г) соответствует равновесная концентрация хр в жидкой фазе (Ж), т.е. и (1)
![]() и
и
![]()
Движущая сила диффузионных процессов
Движущей силой процесса массопередачи Δ является разность между рабочей и равновесной концентрациями или наоборот в зависимости от того, какая из них больше.
Количество вещества, переходящее из одной фазы в другую за единицу времени, равно (2)
![]()
где k – коэффициент массопередачи;
dF – элемент поверхности фазового контакта.
Движущая сила процесса Δ в уравнении (2) может быть выражена через концентрации в одной из фаз:
![]() (3)
(3)
![]() (4)
(4)
Понятие о расчетах массообменных аппаратов
Процессы абсорбции и ректификации осуществляются обычно в противоточных аппаратах, где участвующие в массообмене фазы протекают одна навстречу другой. Обозначим весовую скорость паровой фазы через V, а жидкой – через L.
Допустим,
что распределяемый между фазами компонент
переходит из газовой фазы Г в жидкую
фазу Ж. Для элемента поверхности dF
фазового контакта имеем
![]() (5)
(5)
Для
всей поверхности фазового контакта
![]() (6)
(6)
где хн и хк – начальная и конечная концентрации компонента в жидкой фазе;
yн и yк - начальная и конечная концентрации компонента в газовой фазе.
Для участка аппарата выше любого произвольно взятого сечения, в котором концентрация фаз равна у и х, это уравнение можно написать в следующем виде:
![]()
или
![]() (7)
(7)
Уравнение (7) передает зависимость между концентрациями вещества в обеих фазах в данном сечении колонны, между так называемыми рабочими концентрациями. В координатах х-у уравнение (7) изображается линией или линией рабочих концентраций процесса. Если величины L и V постоянны по высоте аппарата, то постоянными являются и коэффициенты А и В и рабочая линия в координатах х-у является прямой линией.
При изменении L и V по высоте аппарата рабочая линия является кривой. Приведем различные варианты определения движущей силы процессов массопередачи отрезком между линией равновесных концентраций и линией рабочих концентраций процесса (рисунок 2).
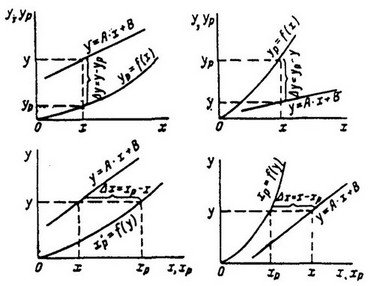
Рисунок 2 – Варианты выражения движущей силы диффузионных процессов
На
основании уравнений (3), (4) и (6) основное
уравнение массопередачи для всей
поверхности фазового контакта F будет
![]() (8)
(8)
где Δуm Δхm - средняя движущая сила.
Определим их значение.
На
основании уравнений (3) и (5) имеем
![]() (9)
(9)
откуда
![]() (10)
(10)
или
![]() (11)
(11)
Подставляя
значение V из уравнения (6), и меняя пределы
интегрирования, найдем
![]() (12)
(12)
или  (13)
(13)
Выражая
движущую силу через концентрацию х,
аналогично предыдущему получим
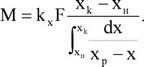 (14)
(14)
Сравнивая
эти уравнения с уравнением (8), найдем,
что средняя движущая сила равна
 (15)
(15)
и  (16)
(16)
Отсюда
находим общее число единиц переноса mу
и mх ![]() (17)
(17)
![]() (18)
(18)
Величины mу и mх показывают на сколькоединиц изменяет рабочую концентрацию на данной поверхности единица движущей силы.
Количество
вещества, перемещающегося в каждой фазе
к поверхности (или от поверхности)
раздела фаз выражается следующими
уравнениями:для газовой фазы
![]() (19)
(19)
для
жидкой фазы
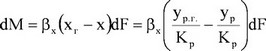 (20)
(20)
Где у и х – коэффициенты массоотдачи, характеризующие интенсивность переноса вещества в каждой фазе;
у и х – концентрации вещества в газовой и жидкой фазах (в ядре потока);
уг и хг – то же у поверхности раздела фаз;
у р.г. – концентрация вещества в газовой фазе у поверхности раздела фаз, равновесная концентрация хг;
Кр – равновесное отношение, равное
Из
уравнений (19) и (20) имеем
![]() (21)
(21)
и ![]() (22)
(22)
Складывая
левые и правые части при уr = у р.г. получаем
 (23)
(23)
откуда
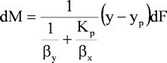 (24)
(24)
Сравнивая
уравнение (24) с уравнением (3), найдем
соотношение между общим коэффициентом
массопередачи и коэффицентами
массопередачи в каждой фазе:  (25)
(25)
Метод расчета массообменных аппаратов (абсорберов, ректификационных колонн), исходя из коэффициентов массопередачи, является наиболее правильным и прогрессивным.
При определении высоты аппарата, необходимой для проведения заданного процесса массопередачи, исходят из понятия ступени изменения концентрации.
