
- •Лабораторная работа №1 Определение равновесных концентраций
- •Лабораторная работа №2 Перегонка двух взаимно нерастворимых жидкостей
- •Лабораторная работа №3 Определение эффективности лабораторной ректификационной колонны периодического действия
- •Лабораторная работа №6 Адсорбционное разделение двухкомпонентной смеси синтетическими цеолитами
Лабораторная работа №1 Определение равновесных концентраций
Цель работы:
Ознакомление с одним из методов исследования равновесия между жидкостью и паром бинарной смеси жидкостей, смешивающихся между собой во всех отношениях;
Сравнение экспериментальных данных с вычисленными теоретически.

1 - колба; 2 – центральная трубка; 3 – термометр; 4 – пробка;
5 – воронка с пробкой; 6 – карман для термометра;
7 – конденсатор-холодильник; 8 – трубка; 9 – сборник; 10-11 – краны
12 – гидрозатвор; 13 – кипятильник; 14 - воздушка
Рисунок 1 – Схема лабораторной установки
1 Методика проведения эксперимента
Сырье – предварительно подготовленная смесь гептана и толуола в количестве 180 см3 заливается в прибор Отмера через воронку 5. Пуск установки начинается с подачи воды в конденсатор-холодильник 7. Затем включается кипятильник, и обогрев верхней части прибора Отмера. Интенсивность кипения регулируется автотрансформатором так, чтобы в трубке 8 образовывалось 2-3 капли конденсата в секунду (напряжение на ЛАТРах не должно превышать 60 В). Если первые капли конденсата, собравшиеся в сборнике 9, окажутся мутными, их следует удалить из прибора. В течение первых двух часов работы прибора состав жидкости в кипятильнике и сборнике меняется. После наступления равновесия, момент которого определяется по показания термометра, отбираются пробы из кипятильника и сборника.
Полученные пробы анализируются на рефрактометре и по зависимости «показатель преломления – состав» определяются объемные доли гептана.
2 Обработка результатов эксперимента
Объемные составы паровой и жидкой фаз, полученные в ходе эксперимента, пересчитываются в мольные.
Для паровой фазы:
![]()
![]()
![]()

где
![]() - удельная плотность соответственно
НКК и ВКК, кг/м3;
- удельная плотность соответственно
НКК и ВКК, кг/м3;
М1 М2 – молекулярная масса вышеуказанных компонентов;
УV1 У1 У1’ – содержание гептана в паре соответственно в объемных,
массовых и мольных долях.
![]()
![]()
![]()

![]() м.д.
м.д.
Для жидкой фазы:
![]()
![]()
![]()
![]()
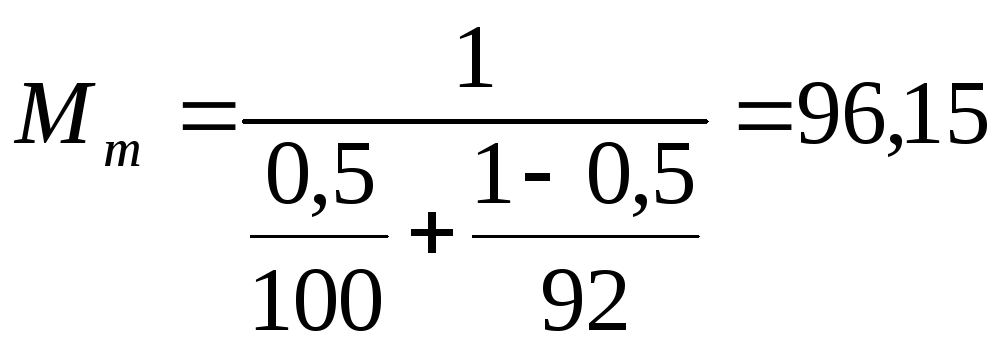
Найдем погрешность:
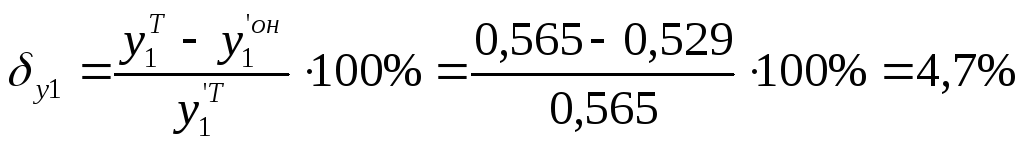

Вывод:
Исследовали равновесие бинарной смеси гептан-толуол смешивающихся между собой во всех отношениях. Данные опыта показали, что система полностью не достигла равновесия.
Лабораторная работа №2 Перегонка двух взаимно нерастворимых жидкостей
Цель работы:
Определение температуры кипения смеси взаимно нерастворимых жидкостей.
Убедиться, что температура кипения смеси не зависит от состава смеси.
Найти удельный массовый расход водяного пара на перегонку углеводородов.

1 - перегонная колба; 2 – термометр; 3 – конденсатор – холодильник;
4 – приемник; 5 – электроплитка
Рисунок 2 – Схема лабораторной установки
1 Методика проведения эксперимента
В колбу 1 загружается жидкий углеводород, в колбу 2 - вода, включается электроплитка 5. вода закипает, и пары воды нагревают углеводород, частично конденсируется, образуя смесь жидкостей. Водяной пар вместе с парами углеводорода поступают в конденсатор – холодильник 3, а после поступает в приемник 4. В процессе опыта через каждые 2-3 минуты замеряют и записывают температуру в перегонной колбе.
2 Обработка результатов эксперимента
Объем воды - 7 мл.
Объем толуола – 29 мл.
Температура в перегоночной колбе – 800С
Общий объем вод – 100 мл.
Вычислим массу испарившегося толуола:
![]()
![]()
![]()
Вычислим массу испарившейся воды:
![]()
![]()
![]()
Найдем соотношение масс испарившегося толуола и воды:
![]()
Из графика РG=44 кПа и РZ=55 кПа.
![]()
где МG и MZ – молекулярные массы компонентов смеси.
![]()
Из диаграммы найдем теоретическую температуру кипения смеси:
tтеор =83,50С
tпр = 800С
Вычислим погрешности:
![]()
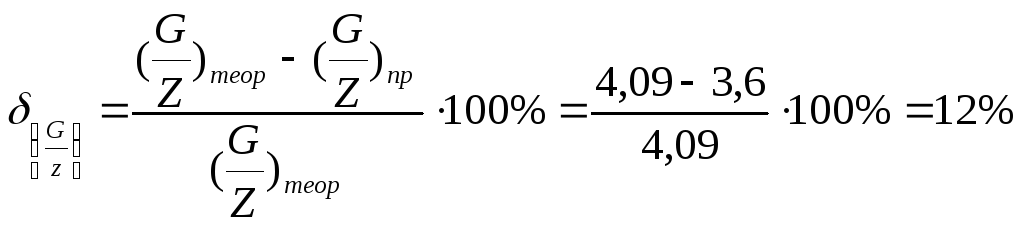
Вывод:
По
экспериментальным данным определили,
что температура кипения смеси двух
нерастворимых жидкостей равна 800С
![]() 20С
и убедились, что она не зависит от состава
смеси, т.к. температуры кипения отдельных
компонентов выше, чем температура
кипения смеси.
20С
и убедились, что она не зависит от состава
смеси, т.к. температуры кипения отдельных
компонентов выше, чем температура
кипения смеси.
